O egyenlet kiegyensúlyozása lehetővé teszi számunkra, hogy összehangoljuk a kémiai egyenletben jelen levő atomok számát úgy, hogy az valósággá váljon és kémiai reakciót képviseljen.
Az alábbi kérdések segítségével tesztelje tudását, és ellenőrizze a visszajelzés után kommentált válaszokat a kérdések megválaszolásához.
1. kérdés
(Mackenzie-SP)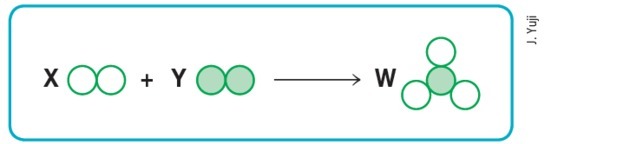
Feltételezve, hogy az üres és a kitöltött kör különböző atomokat jelent, akkor a séma A fentiek kiegyensúlyozott kémiai reakciót képviselnek, ha az X, Y és W betűket helyettesítjük a értékek:
a) 1, 2 és 3.
b) 1, 2 és 2.
c) 2, 1 és 3.
d) 3, 1 és 2.
e) 3, 2 és 2.
D) 3., 1. és 2. alternatíva.
1. lépés: Betűket rendelünk az egyenlet könnyebb megértése érdekében.
2. lépés: összeadjuk az indexeket, hogy megtudjuk, kinek van a legtöbb atomja az egyenletben.
| A | |
| B |
A és B az egyenlet minden tagjában csak egyszer jelenik meg. Ha azonban összeadjuk az indexeket, akkor azt látjuk, hogy A-nak van a legnagyobb értéke. Ezért elkezdtük neki az egyensúlyozást.
3. lépés: Kiegyenlítjük az A elemet az indexek átültetésével és együtthatókká alakításával.
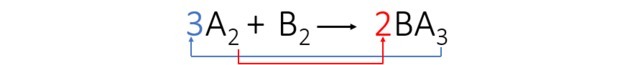
Megfigyeltük, hogy a B elem automatikusan kiegyensúlyozott és az egyenlet együtthatói: 3, 1 és 2.
2. kérdés
(Unicamp-SP) Olvassa el a következő mondatot, és alakítsa át (kiegyensúlyozott) kémiai egyenletgé szimbólumok és képletek segítségével: „egy gáznemű nitrogén molekula, amely két atomot tartalmaz. molekulánként nitrogén, három diatomiás, gáznemű hidrogénmolekulával reagál, két molekula gáznemű ammóniát eredményezve, amely három hidrogénatomból és egy nitrogén".
Válasz:
A kérdésben leírt atomokat ábrázolva megérthetjük, hogy a reakció a következőképpen történik:
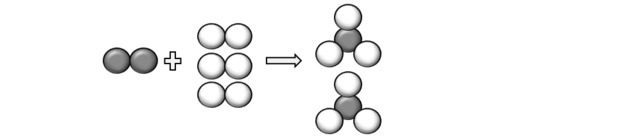
Tehát elérkeztünk az egyenlethez:
3. kérdés
A hidrogén-peroxid egy kémiai vegyület, amely bomlik, víz és oxigén képződhet az alábbi kémiai egyenlet szerint.
Ezzel a reakcióval a helyesen kiegyensúlyozott egyenlet a következő:
a) H2O2 → A2 + H2O
b) 2 óra2O2 → A2 + 2H2O
c) H2O2 → 2O2 + H2O
d) 2 óra2O2 → 2O2 + 2H2O
Helyes alternatíva: b) 2H2O2 → A2 + 2H2O
Ne feledje, hogy a hidrogén-peroxid egy vegyi anyag, amely két kémiai elem atomjából áll: hidrogén és oxigén.
A bomlási reakció után a két elem azonos számú atomjának kell lennie mind a reagensekben, mind a termékekben. Ehhez ki kell egyensúlyoznunk az egyenletet.
Megjegyezzük, hogy a reagensben 2 hidrogénatom van (H2O2) és a termékben két atom (H2O). Az oxigén azonban két atomot tartalmaz a reagensben (H2O2) és a termékekben három atom (H2O és O2).
Ha a 2-es együtthatót a hidrogén-peroxid elé tesszük, megduplázzuk az elemek atomszámát.
Vegye figyelembe, hogy ha ugyanazt az együtthatót vesszük a víz képletével együtt, akkor mindkét oldalon azonos mennyiségű atom van.
Ezért a megfelelően kiegyensúlyozott kémiai egyenlet 2H2O2 → A2 + 2H2O.
4. kérdés
(UFPE) Vegye figyelembe az alábbi kémiai reakciókat.
Mondhatjuk, hogy:
a) mindegyik kiegyensúlyozott.
b) 2, 3 és 4 kiegyensúlyozottak.
c) csak 2 és 4 kiegyensúlyozott.
d) csak 1 kiegyensúlyozatlan.
e) egyik sem megfelelő egyensúlyban, mert a reagensek és a termékek fizikai állapota eltér.
A b) 2., 3. és 4. alternatíva kiegyensúlyozott.
Az 1. és az 5. alternatíva helytelen, mert:
- Az 1. egyenlet kiegyensúlyozatlan, a helyes egyensúly a következő lenne:
- Az 5. egyenlet helytelen, mert a reakcióban képződött vegyület H lenne2CSAK3.
A H kialakításához2CSAK4 be kell vonni az egyenletbe az SO oxidációját2.
5. kérdés
(Mackenzie-SP) 800 ° C-ra melegítve a kalcium-karbonát kalcium-oxiddá (szűz mész) és szén-dioxiddá bomlik. A megfelelően kiegyensúlyozott egyenlet, amely megfelel a leírt jelenségnek, a következő:
(Adva: Ca - alkáliföldfém.)
C) alternatíva
A kalcium alkáliföldfém, és a stabilitás érdekében a kalciumnak 2 elektronra van szüksége (Ca2+), amely az oxigéntöltés (O2-).
Tehát egy kalciumatom oxigénatomhoz kötődik, és a képződött vegyület CaO, amely oltatlan mész.
A másik termék a szén-dioxid (CO2). Mindkettőt kalcium-karbonát (CaCO3).
Egy egyenletbe foglalva:
Megjegyezzük, hogy az atomok mennyisége már helyes, és nincs szükség kiegyensúlyozásra.
6. kérdés
(UFMG) Az egyenlet nem kiegyensúlyozott. A lehető legkisebb számokkal kiegyensúlyozva a sztöchiometriai együtthatók összege a következő lesz:
a) 4
b) 7
c) 10
d) 11
e) 12
E) alternatíva 12
A próbamódszer alkalmazásával az egyensúlyozási sorrend a következő lesz:
1. lépés: Mivel az elem, amely minden tagban csak egyszer jelenik meg és a legmagasabb indexű, a kalcium, elkezdtünk egyensúlyozni érte.
2. lépés: A radikális PO egyensúlyát követjük43-, amely szintén csak egyszer jelenik meg.
3. lépés: kiegyensúlyozzuk a hidrogént.
Ezzel megfigyelhetjük, hogy automatikusan beállítottuk az oxigén mennyiségét, és az egyenlet egyensúlya a következő:
Ne feledje, hogy ha az együttható 1, akkor nem kell beírnia az egyenletbe.
Összeadva a meglévő együtthatókat:
7. kérdés
Az égés egyfajta kémiai reakció, amelyben az energia hő formájában szabadul fel.
A szén és hidrogén által képződött anyag teljes égésekor szén-dioxid és víz képződik.
Figyelje meg a szénhidrogén égési reakcióit, és válaszolja meg, hogy az alábbi egyenletek közül melyik van hibásan kiegyensúlyozott:
a) CH4 + 2O2 → CO2 + 2H2O
időszámításunk előtt3H8 +502 → 3CO2 + 4H2O
c) C4H10 + 13 / 3O2 → 4CO2 + 5 óra2O
d) C2H6 + 7 / 2O2 → 2CO2 + 3H2O
Helytelen válasz: c) C4H10 + 13 / 3O2 → 4CO2 + 5 óra2O
A kémiai egyenletek kiegyensúlyozásához először nézzük meg, melyik elem jelenik meg csak egyszer az egyenlet minden tagjában.
Megjegyezzük, hogy a szén és a hidrogén minden bemutatott egyenletben csak egy reagenst és egy terméket alkot.
Kezdjük tehát az egyensúlyt a hidrogénnel, mivel nagyobb az atomszám.
Ezért az egyensúlyozás sorrendje a következő lesz:
- Hidrogén
- Szén
- Oxigén
Hidrogén
Mivel a terméknek 2 hidrogénatomja van, beírunk egy olyan együtthatót, amely szorozva 2-vel a hidrogénatomok számát eredményezi a reagensben.
a) CH4 + O2 → CO2 + 2H2O
időszámításunk előtt3H8 + O2 → CO2 + 4H2O
c) C4H10 + O2 → CO2 + 5H2O
d) C2H6 + O2 → CO2 + 3H2O
Szén
A kiegyensúlyozást úgy végezzük, hogy a reaktánsban a szénindexet transzponáljuk, és együtthatóként alkalmazzuk az adott elem atomjaival rendelkező termékre.
a) CH4 + O2 → 1CO2 + 2H2O
időszámításunk előtt3H8 + O2 → 3CO2 + 4H2O
c) C4H10 + O2 → 4CO2 + 5 óra2O
d) C2H6 + O2 → 2CO2 + 3H2O
Oxigén
Ha összeadjuk a képződött termékek oxigénatomjainak számát, megkapjuk az elem atomjainak számát, amelyeknek reagálniuk kell.
Ehhez egy olyan együtthatót kell beírnunk, amely 2-gyel megszorozva eredményezi a termékek oxigénatomjainak számát.
a) CH4 + O2 → 1CO2 + 2H2O
2x = 2 + 2
2x = 4
x = 2
Tehát a helyes egyenlet: CH4 + 2O2 → 1CO2 + 2H2O.
időszámításunk előtt3H8 + O2 → 3CO2 + 4H2O
2x = 6 + 4
2x = 10
x = 5
Tehát a helyes egyenlet: C3H8 + 5O2 → 3CO2 + 4H2O
c) C4H10 + O2 → 4CO2 + 5 óra2O
2x = 8 + 5
2x = 13
x = 13/2
Tehát a helyes egyenlet: C4H10 + 13/2O2 → 4CO2+ 5 óra2O
d) C2H6 + O2 → 2CO2 + 3H2O
2x = 4 + 3
2x = 7
x = 7/2
Tehát a helyes egyenlet: C2H6 + 7/2O2 → 2CO2 + 3H2O
Helyesen kiegyensúlyozott egyenletek:
a) CH4 + 2O2 → CO2 + 2H2O
időszámításunk előtt3H8 +502 → 3CO2 + 4H2O
c) C4H10 + 13 / 2O2 → 4CO2 + 5 óra2O
d) C2H6 + 7 / 2O2 → 2CO2 + 3H2O
Így a c) C alternatíva4H10 + 13 / 3O2 → 4CO2 + 5 óra2Ennek oka az, hogy nincs megfelelő egyensúlya.
8. kérdés
(Enem 2015) A mészkövek olyan anyagok, amelyek kalcium-karbonátból állnak, és amelyek a kén-dioxid (SO2), fontos légszennyező anyag. A folyamatban résztvevő reakciók a mészkő kalcinálás útján történő aktiválása és az SO rögzítése2 kalcium-só képződésével, amit az egyszerűsített kémiai egyenletek szemléltetnek.
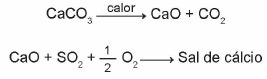
Figyelembe véve a kéntelenítési folyamatban résztvevő reakciókat, a kalcium-só kémiai képlete megfelel:
B) alternatíva
Mivel a reakció kiegyensúlyozott, a reagensekben lévő atomoknak azonos mennyiségben kell lenniük a termékekben. Így,
A képződött só a következőkből áll:
1 kalciumatom = Ca
1 kénatom = S
4 oxigénatom = O4
Ezért a kalcium-só kémiai képlete megfelel a CaSO-nak4.
9. kérdés
(UFPI) X reakciója Y-val az alábbiakban látható. Határozza meg, melyik egyenlet képviseli a legjobban a kiegyensúlyozott kémiai egyenletet.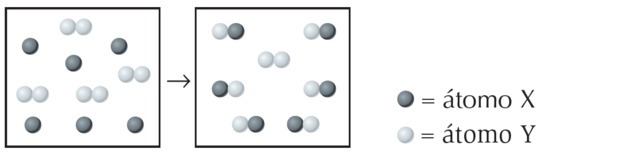
A) alternatíva
Az ábrán megfigyelhetjük, hogy az X faj egyetlen atom, míg Y kova, vagyis 2 atom összekapcsolódásával jön létre. Tehát X reagál Y-val2.
A képződött terméket XY képviseli, az egyenlet kiegyensúlyozatlan:
Kiegyenlítjük az egyenletet a következőképpen:
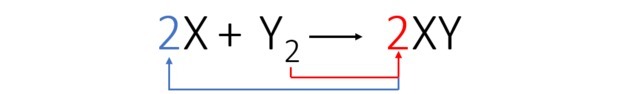
A kiegyensúlyozott egyenlet szerint az alábbi ábra megmutatja, hogyan történik a reakció és annak aránya.
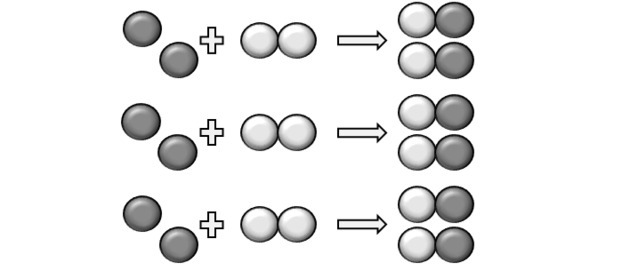
A reakció kialakulásához rögzített aránynak kell lennie, ezért előfordulhat, hogy egyes vegyületek nem reagálnak. Ezt mutatja az ábra, mert a termékben azt látjuk, hogy egy Y2 nem reagált.
10. kérdés
(Enem 2010) Egy egyre jobb bolygót népszerűsítő mobilizációk a következő generációk számára egyre gyakoribbak. A legtöbb tömegközlekedési eszköz jelenleg egy fosszilis üzemanyag elégetésével működik. Ennek a gyakorlatnak a terhére példaként elegendő tudni, hogy egy autó átlagosan körülbelül 200 g szén-dioxidot termel megtett kilométerenként.
Globális felmelegedés magazin. 2., 8. év. Az Instituto Brasileiro de Cultura Ltda kiadványa.
A benzin egyik fő alkotóeleme az oktán (C8H18). Az oktánszám égése révén lehetséges az autó elindulása. A folyamat kémiai reakcióját bemutató egyenlet azt mutatja, hogy:
a) oxigén szabadul fel a folyamat során, O formájában2.
b) a víz sztöchiometriai együtthatója 8–1 oktán.
c) a folyamatban vízfogyasztás van, tehát az energia felszabadul.
d) az oxigén sztöchiometriai együtthatója 12,5–1 oktán.
e) a szén-dioxid sztöchiometriai együtthatója 9-1 oktán
D) alternatíva: az oxigén sztöchiometriai együtthatója 12,5–1 oktán.
Az egyenlet kiegyensúlyozásakor a következő együtthatókat találjuk:
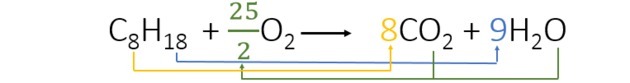
- Az egyensúlyt hidrogénnel kezdtük, amely minden tagban csak egyszer jelenik meg, és amelynek indexe magasabb. Mivel 18 reakcióképes hidrogénatom van, a termékben 2 van, ezért hozzá kell adnunk egy számot, amely 2-gyel megszorozva 18-at ad. Tehát a 9 az együttható.
- Ezután hozzáadjuk a 8 együtthatót a CO elé2 hogy az egyenlet minden egyes tagjában 8 szén legyen.
- Végül csak hozzá kell adni a termék oxigénmennyiségét, és meg kell találni azt az értéket, amelyet megszorozva 2-vel 25 oxigénatomot kapunk. Tehát a 25/2 vagy 12,5 lehetőséget választottuk.
Így 1 oktán elégetéséhez 12,5 oxigént fogyasztanak.
11. kérdés
(Fatec-SP) A műtrágyák alapvető jellemzője vízben való oldhatóságuk. Ezért a műtrágya-ipar átalakítja a kalcium-foszfátot, amelynek vízben való oldhatósága nagyon alacsony, sokkal oldhatóbb vegyületté, amely a kalcium-szuperfoszfát. Ezt a folyamatot az egyenlet képviseli:
ahol x, y és z értékei rendre:
a) 4, 2 és 2.
b) 3, 6 és 3.
c) 2, 2 és 2.
d) 5, 2 és 3.
e) 3, 2 és 2.
E) 3., 2. és 2. alternatíva.
Az algebrai módszer segítségével egyenleteket alkotunk minden elemre, és egyenlővé tesszük a reaktáns atomjainak számát a termék atomjainak számával. Ebből kifolyólag:
Kiegyensúlyozott egyenlet:
12. kérdés
Kiegyenlítse az alábbi egyenleteket a próbamódszer segítségével.
Válasz:
Az egyenlet a hidrogén és a klór elemeiből áll. Kiegyenlítjük az elemeket csak úgy, hogy a szorzót a termék elé adjuk.
Az egyenletet nem kellett egyensúlyba hozni, mivel az atomok mennyisége már ki van igazítva.
A foszfornak két atomja van a reagensekben, így ennek az elemnek az egyensúlyához a termékben lévő foszforsav mennyiségét 2H-ra állítjuk.3POR4.
Ezt követően megfigyeltük, hogy a hidrogén 6 atomot tartalmaz a termékben, kiegyenlítettük ennek az elemnek a mennyiségét, hozzáadva a 3 együtthatót az azt tartalmazó reaktánshoz.
Az előző lépésekkel rögzítettük az oxigén mennyiségét.
Az egyenletet megnézve azt látjuk, hogy a termékekben a hidrogén és a bróm mennyisége kétszerese ha van a reagensekben, akkor a HBr-hez hozzáadjuk a 2-es együtthatót, hogy egyensúlyba hozzuk ezt a kettőt elemek.
A klór 3 atomot tartalmaz a termékekben és csak 1 atomot tartalmaz a reagensekben, ezért egyensúlyba hozzuk a 3-as együtthatót a HCl elé.
A hidrogén 3 atomot tartalmaz a reagensekben és 2 atom a termékekben. A mennyiségek beállításához átalakítjuk a H indexet2 együtthatóban megszorozzuk a 3-mal, amely már a HCl-ben volt, és megkapjuk a 6HCl eredményét.
A termékek klórmennyiségét úgy állítjuk be, hogy 6 atomja is legyen és 2AlCl-t kapjunk3.
Az alumínium 2 atomot tartalmaz a termékekben, a reagensekben lévő mennyiséget 2Al-re állítottuk be.
A termék hidrogénmennyiségét 3H-ra egyensúlyozzuk2 és az elem 6 atomjának mennyiségét illesztjük az egyenlet minden tagjába.
Az egyenletben a nitrátgyök (NO3-) indexe 2 van a termékben, az indexet a reaktánsban a 2AgNO együtthatójává alakítjuk3.
Az ezüst mennyiségét módosítani kellett, mivel most 2 atom van a reagensekben, így 2Ag van a termékben.
A reaktánsokban 4 hidrogénatom van, és ennek az elemnek a kiegyensúlyozásához a 2-es együtthatót adjuk a HCl-termékhez.
A klór most 4 atomot tartalmaz a termékekben, ezért a reagens mennyiségét 2Cl-ra állítjuk2.
A reagensekben 6 hidrogénatom van, és ennek az elemnek az egyensúlyához a víz mennyiségét 3H-ra állítjuk2O.
2 szénatom van a reagensekben, és ennek az elemnek az egyensúlyához a szén-dioxid mennyiségét 2CO-ra állítjuk2.
Az oxigénnek 7 atomnak kell lennie a reaktánsokban, és ennek az elemnek az egyensúlyához a molekuláris oxigén mennyiségét 3O-ra állítjuk2.
Az egyenletet tekintve a nitrátgyök (NO3-) indexe 2 a termékben. Az indexet az AgNO reagensben 2-es együtthatóvá alakítjuk3.
2 ezüstatom van a reagensekben, és ennek az elemnek az egyensúlyához a termékben lévő ezüst-klorid mennyiségét 2AgCl-ra állítjuk.
A termékben 3 kalciumatom van, és az elem kiegyensúlyozásához a reagensben lévő kalcium-nitrát mennyiségét 3Ca-ra (NO3)2.
Ezután 6 NO gyökök maradnak3- a reagensekben és ennek a gyököknek az egyensúlyára a termékekben található salétromsav mennyiségét 6HNO-ra állítjuk3.
Most 6 hidrogénatom van a termékekben, és ennek az elemnek az egyensúlyához a foszforsav mennyiségét a reagensben 2H-ra állítjuk.3POR4.
Tudjon meg többet a kémiai egyenletekkel végzett számításokról:
- A kémiai egyenletek kiegyensúlyozása
- Sztöchiometria
- Sztöchiometriai számítások
- Sztöchiometriai gyakorlatok
- Periódusos gyakorlatok

