Hess törvényét Germain H. svájci vegyész hozta létre. Hess (1802-1850), akit a termokémia egyik alapítójának tartanak. Törvénye így szólt:

Vagyis a ΔH csak a reagensek és termékek entalpia-értékeitől függ, ahogyan a következő kifejezésben:
| ΔH = ΔHreagensek + ΔHTermékek |
Például vegyük figyelembe azt a reakciót, ahol 1 mol víz (H2O) gáz halmazállapotú vízzé alakul. Ezt a reakciót kétszer hajtjuk végre; azonban különböző utakat választottunk:
(1.) Egyetlen lépésben hajtották végre:
H2O(1) → H2Ov. ΔH = +44 kJ
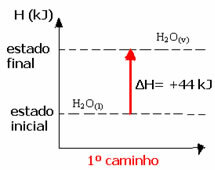
(2.) Két szakaszban hajtották végre:
1. lépés: H2O(1) → H2. g) + ½ a2. g) ΔH = +286 kJ
2. szakasz: H2. g) + ½ a2. g) → H2Ov. ΔH = -242 kJ
H2O(1) → H2Ov. ΔH = +44 kJ
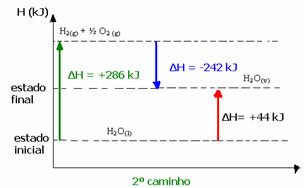
Megjegyezzük, hogy függetlenül attól, hogy egy vagy két lépést végrehajtottak-e, az entalpia változás (ΔH) mindig 44 kJ. Ez azért van, mert a ΔH a folyamatot alkotó lépések, vagyis a köztes folyamatok valoresH-értékeinek algebrai összege:
| ΔH = ΔH1 + ΔH2 + ΔH3 + ... |
Például a második esetben a reakció teljes ΔH értéke az első lépés ΔH (ΔH = +286 kJ) és a második (ΔH = -242 kJ) összege volt. Így egyetlen lépésben ugyanazt a reakcióértéket kaptuk:
ΔH = (+286 + (-242)) kJ
ΔH = (+286 -242) kJ
ΔH = +44 kJ
Ezért csak a kezdeti és a végső értékek érdekelnek minket. Ebben az esetben a kezdeti állapot megfelel H-nak2O(1) és a H vége2Ov..
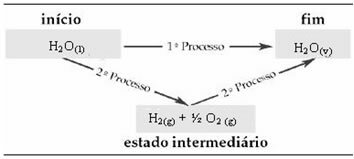
Ez a törvény nagyon fontosá vált a termokémiában, mert bizonyos kémiai reakciók cannotH-ját nem lehet kísérletileg meghatározni. Hess-törvény szerint azonban az ilyen típusú reakciók entalpiája kiszámítható más reakciók (közbenső reakciók) entalpiáiból.
Írta: Jennifer Fogaça
Kémia szakon végzett
Brazil iskolai csapat

