Elektrolízis egy fizikai-kémiai folyamat, amely bármilyen forrásból származó elektromos energiát felhasznál (pl akkumulátor vagy elem) egy kémiai reakció bekövetkezésének kényszerítésére olyan egyszerű vagy összetett anyagok előállítására, amelyek a természetben nem találhatók, vagy amelyek nem találhatók meg nagy mennyiségben.
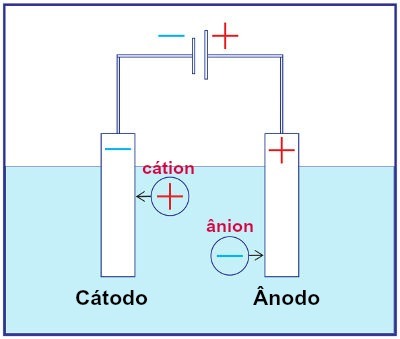
Bármely elektrolízis rendszer összeállításának ábrázolása
Az elektrolízis során a kation a katódon redukción megy keresztül, az anion pedig az anódon oxidálódik. Ez egy külső forrás által biztosított elektromos kisülés révén történik. Így az elektrolízis során nem spontán oxidációs és redukciós reakciónk van.
Most értse meg az elektrolízis kétféle módját:
Az ilyen típusú elektrolízis során a ionos anyag folyékony állapotban, elektrolitikus tartályban. Amikor az ionos anyag (XY) fúzión megy keresztül, átmegy a folyamaton elhatárolódás, az alábbiak szerint:
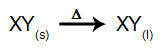

Ezután, amikor az áramforrás be van kapcsolva, a kation (X+) mozog a katód felé, és az anionok (Y-) haladjon az anód felé. Ezáltal:
A katódnál: a kationok elektronokat kapnak (redukción mennek keresztül) és stabil anyaggá (X) alakulnak át, amelyet a következő egyenlet képvisel:
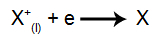
Az anódnál: az anionok elveszítik az elektronokat (oxidálódnak) és stabil anyaggá (X) válnak, ezt a folyamatot a következő egyenlet képviseli:

a) Példa a magmás elektrolízisre
Példaként kövesse most a magmintás elektrolízist nátrium-klorid (NaCl). Amikor a nátrium-klorid (NaCl) fúzión megy keresztül, a disszociációs folyamaton megy keresztül, az alábbiak szerint:
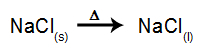
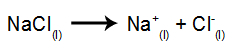
Ezután, amikor az áramforrás be van kapcsolva, a kation (Na+) mozog a katód felé, és az anionok (Cl-) haladjon az anód felé. Ezáltal:
A katódnál: a kationok+ elektronokat kapnak (redukción mennek keresztül) és stabil anyaggá (Na, ami szilárd fém) válnak, ezt a folyamatot az alábbi egyenlet képviseli:

Az anódnál: a Cl anionok- elektronokat veszítenek (oxidálódnak) és stabil anyaggá válnak (Cl2, amely gáznemű), az alábbi egyenlet által képviselt folyamat:

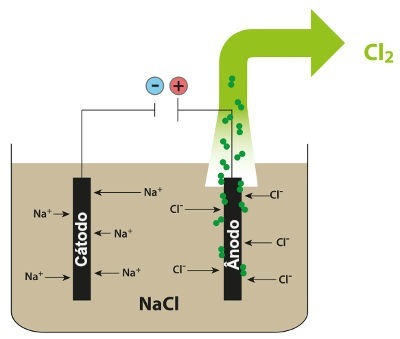
A NaCl magmás elektrolízisét bemutató séma
Így a nátrium-klorid magmás elektrolízisében fémes nátrium (Na) és klórgáz (Cl2).
Az ilyen típusú elektrolízis során az elektrolitartály belsejében vízben oldott ionos anyagot használunk. Tehát az elektrolízis elvégzése előtt először összekeverjük az anyagot (általában egy sót szervetlen) vízben, hogy disszociációját okozza (kation és anion felszabadulása), az ábra szerint ordít:
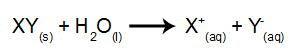
A magmás elektrolízissel kapcsolatban az a különbség, hogy a disszociációból származó ionok mellett a víz önionizálásából származó ionok is vannak. Önionizálásakor a víz hidronium-kationt (H+) és egy hidroxid-anion (OH-), az alábbi egyenlet szerint:
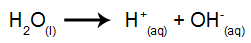
Így az elektrolitikus tartályban két kation van jelen (az egyik az anyagból ionos és egy vízből) és két anion (az egyik az ionos anyagból, a másik a Víz).
Ahhoz, hogy tudjuk, melyik kation mozog a katódhoz, és melyik anion mozog az anódhoz, ismerni kell a kationok és az anionok kisülési sorrendjét.
Kationokhoz:
Au> Pt> Hg> Ag> Cu> Ni> Cd> Pb> Fe> Zn> Mn> hidronium> IIIA család> IIA család> IA család
anionokhoz
Nem oxigénmentes anionok és HSO4 > hidroxid> oxigenizált anionok és F
Majd az áramforrás bekapcsolásakor kation (X+) mozog a katód felé, és az egyik anion (Y-) az anód felé halad.
A katódnál: a kationok elektronokat kapnak (redukción mennek keresztül) és stabil anyaggá (X) alakulnak át, amelyet az alábbi egyenlet képvisel:

Az anódnál: az anionok elveszítik az elektronokat (oxidálódnak) és stabil anyaggá (Y) válnak, ezt a folyamatot az alábbi egyenlet képviseli:
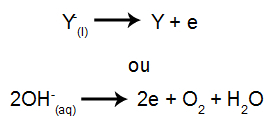
a) Példa vizes elektrolízisre
Példaként nátrium-klorid (NaCl) vizes elektrolízisét alkalmazzuk. Ha a nátrium-kloridot (NaCl) vízben oldjuk, az disszociációs folyamaton megy keresztül, az alábbiak szerint:
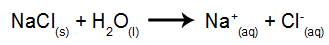
A NaCl disszociációja mellett megvan a víz önionizációja is:
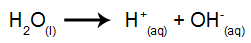
Tehát megvan a H kation+ és tovább+ és az OH anionjai- és Cl-. Ezután, amikor az áramforrás be van kapcsolva, a következők vannak:
katódnál: a H kationok+ elektronokat kap (redukált) és stabil anyaggá válik (H2, ami gáz). Ennek oka, hogy a hidronium elsőbbséget élvez az IA család elemeivel (ebben az esetben Na) szemben. A folyamatot az alábbi egyenlet képviseli:
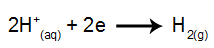
anódnál: a Cl anionok- elektronokat veszítenek (oxidálódnak) és stabil anyaggá válnak (Cl2, amely gáznemű). Ennek oka, hogy a Cl- ez egy oxigénmentes anion, és kisülési prioritása van a hidroxiddal szemben, amelyet az alábbi egyenlet képvisel:


A NaCl vizes elektrolízisét bemutató séma
Így a nátrium-klorid vizes elektrolízisében hidrogéngáz képződik (H2) és klórgáz (Cl2).
Általam. Diogo Lopes Dias
Forrás: Brazil iskola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-eletrolise.htm

