A periódusos rendszer fontos tanulmányi eszköz, amely információkat gyűjt az összes ismert kémiai elemről.
Tesztelje tudását ezzel a listával 17 kérdés a téma különböző megközelítéseivel, és oldja meg kétségeit a visszajelzés után kommentált állásfoglalásokkal.
A kérdések megértéséhez használja a periódusos táblázat teljes és naprakész.
Periódusos rendszer szervezése
1. kérdés
(UFU) A 19. század elején több kémiai elem felfedezésével és elkülönítésével szükségessé vált azok ésszerű osztályozása a szisztematikus vizsgálatok elvégzése érdekében. Számos hozzászólás érkezett a kémiai elemek jelenlegi periodikus osztályozásának eléréséig. A jelenlegi időszakos besorolással kapcsolatban válaszoljon:
a) Hogyan szerepelnek a periódusos rendszer egymás után felsorolt elemei?
A periódusos rendszer kémiai elemek szekvenciáiba rendeződik növekvő sorrendben atomszám. Ez a szám megfelel az atom magjában lévő protonok számának.
Ezt a szervezési módszert Henry Moseley javasolta, amikor átalakította a Dmitri Mendeleiev által javasolt táblázatot.
Egy elem elhelyezhető a táblázatban annak a családnak és periódusnak megfelelően, amelybe beillesztették. Ez az eloszlás a következőképpen történik:
| csoportok vagy családok | 18 függőleges szekvencia |
| Hasonló jellemzőkkel rendelkező elemcsoportok. |
| Időszakok | 7 vízszintes szekvencia |
| Az elem rendelkezésére álló elektronikus rétegek száma. |
b) A periódusos rendszer mely csoportjai találhatók: halogén, alkálifém, alkáliföldfém, kalkogén és nemesgáz?
Az elemek csoportokba sorolása a tulajdonságok szerint történik. Az azonos csoportba tartozó elemek hasonló jellemzőkkel rendelkeznek, és a megadott osztályozáshoz:
| Osztályozás | Csoport | Család | Elemek |
| halogén | 17 | 7A | F, Cl, Br, I, At és Ts |
| alkálifém | 1 | 1A | Li, Na, K, Rb, Cs és Fr |
| alkáliföldfém | 2 | 2A | Be, Mg, Ca, Sr, Ba és Ra |
| kalkogén | 16 | 6A | O, S, Se, Te, Po és Lv |
| nemesgáz | 18 | 8A | Ő, Ne, Ar, Kr, Xe, Rn és Og |
2. kérdés
(PUC-SP) Oldja meg a problémát az alábbi állítások elemzése alapján.
I - A jelenlegi modern periódusos rendszer az atomtömeg növekvő sorrendjében van elrendezve.
II - Minden elem, amelynek 1 elektronja és 2 elektronja van a vegyértékhéjban, alkálifémek és alkáliföldfémek, feltéve, hogy a fő kvantumszám ennek a rétegnek (n 1).
III - Ugyanebben az időszakban az elemek ugyanannyi szintet (réteget) mutatnak be.
IV - Ugyanabban a csoportban (családban) az elemek azonos számú szinttel (réteggel) rendelkeznek.
Arra a következtetésre jutottak, hogy a kémiai elemek jelenlegi periódusos rendszerét tekintve helyesek:
a) I és IV (csak).
b) I. és II. (csak).
c) II. és III. (csak).
d) II. és IV. (csak).
e) III és IV (csak).
Helyes alternatíva: c) II. És III. (Csak).
Minden alternatívát elemezve meg kell tennünk:
I - ROSSZ. Az elemek az atomszám növekvő sorrendjében vannak elrendezve.
II - Helyes. A vegyértékhéj elektronjai meghatározzák azt a csoportot, amelyben az elem található.
| alkálifémek | 1 elektron a vegyértékhéjban |
| 3olvas | 2-1 |
| 11Nál nél | 2-8-1 |
| 19K | 2-8-8-1 |
| 37Rb | 2-8-18-8-1 |
| 55Cs | 2-8-18-18-8-1 |
| 87Fr | 2-8-18-32-18-8-1 |
| alkáliföldfémek | 2 elektron a vegyértékhéjban |
| 4lenni | 2-2 |
| 12mg | 2-8-2 |
| 20Itt | 2-8-8-2 |
| 38úr | 2-8-18-8-2 |
| 56Ba | 2-8-18-18-8-2 |
| 88Béka | 2-8-18-32-18-8-2 |
A fő kvantumszám megfelel annak a héjnak, amelyben az elektron található, különbözik az 1-től, mivel az elektronikus terjesztés által észrevesszük, hogy az elektron helye a második héjból származik, ill n = 2.
III - Helyes. Egy elem elhelyezkedése egy bizonyos periódusban az elektronikus terjesztés során a rétegek számának köszönhető.
| Időszakok | 7 vízszintes szekvencia |
| 1. periódus | 1 réteg: K |
| 2. periódus | 2 réteg: K, L |
| 3. periódus | 3 réteg: K, L, M |
| 4. periódus | 4 réteg: K, L, M, N |
| 5. periódus | 5 réteg: K, L, M, N, O |
| 6. periódus | 6 réteg: K, L, M, N, O, P |
| 7. időszak | 7 réteg: K, L, M, N, O, P, Q |
Példa: a második periódusban található kémiai elem.
IV - ROSSZ. Az ugyanahhoz a csoporthoz tartozó elemek hasonló tulajdonságokkal rendelkeznek, és ez annak a ténynek köszönhető, hogy a vegyértékű héjban azonos számú elektron van.
Példa:
| Berillium | Magnézium |
|
2 elektron be vegyértékréteg. |
2 elektron be vegyértékréteg. |
Ezért a berillium és a magnézium a periódusos rendszer 2. csoportjának része.
3. kérdés
(Unitins) Az elemek modern periodikus osztályozását illetően határozza meg az igaz állítást:
a) egy családban az elemek általában ugyanannyi elektronot tartalmaznak az utolsó héjban.
b) a periódusos rendszeren a kémiai elemeket az atomtömegek csökkenő sorrendjében helyezzük el.
c) egy családban az elemek nagyon eltérő kémiai tulajdonságokkal rendelkeznek.
d) egy időszakban az elemek hasonló kémiai tulajdonságokkal rendelkeznek.
e) minden reprezentatív elem a periódusos rendszer B csoportjába tartozik.
Helyes alternatíva: a) egy családban az elemek általában ugyanannyi elektronot tartalmaznak az utolsó héjban.
a) HELYES. Ugyanazon család kémiai elemeinek azonos számú elektronja van az utolsó héjban, és ez hasonló tulajdonságokkal bír.
b) ROSSZ. Az atomtömegek az elem atomszámának növekedésével nőnek.
c) ROSSZ. Az elemek kémiai tulajdonságai hasonlóak, ezért ugyanazon családba vannak csoportosítva.
d) ROSSZ. Egyszerre az elemek elektronjainak elosztása azonos számú héjban történik.
e) Rossz. A reprezentatív elemek az A csoportba tartoznak, amely megfelel a családoknak: 1A, 2A, 3A, 4A, 5A, 6A, 7A és 8A. A B csoportba tartozó elemek átmeneti elemek.
4. kérdés
(Vunesp) Figyelembe véve a kémiai elemek tulajdonságait és a periódusos rendszert, helytelen kijelenteni:
a) a fém olyan anyag, amely elektromos áramot vezet, képlékeny és alakítható.
b) a nem fém olyan anyag, amely nem vezet elektromos áramot, sem nem hajlékony, sem alakítható.
c) egy félmetál fizikai megjelenése fém, de kémiai viselkedése hasonló a nem féméhez.
d) a legtöbb kémiai elem nem fémből áll.
e) a nemesgázak monoatomosak.
Helytelen alternatíva: d) a legtöbb kémiai elem nem fém.
Vegye figyelembe a periódusos rendszerben található kémiai elemek besorolását fémekre, nemfémekre és félméretekre.

Mint láthatjuk, a legtöbb elem fém.
a) HELYES. A fémek a szabad elektronok által létrehozott elektronfelhők miatt vezetik az áramot, amelyek szerkezetükre jellemzőek. Rugalmasak, mert huzalokká vagy lapokká válhatnak, attól függően, hogy a nyomás milyen régióban érvényesül. Ezek is alakíthatók, mivel nagyon vékony lemezek készíthetők ilyen típusú anyagból.
b) Helyes. A nemfémeknek ellentétes tulajdonságaik vannak a fémekkel. Vezetékek helyett jó hőszigetelők, és mivel törékenyek, nincsenek huzalokká vagy lapokká formálva, mivel nem jó a hajlékonyságuk és a alakíthatóságuk.
c) Helyes. A szemimetálok jellemzői a fémek és a nem fémek között vannak. Mivel az elektromosság félvezetői, fémes fényűek, de törékenyek, mint a nemfémek.
d) ROSSZ. A legtöbb elem a fémek közé tartozik. A periódusos rendszerben a fémek osztályai a következők: alkáli, alkáliföld, átmeneti belső és külső.
e) Helyes. A nemesgázak egyatomosak, ezért csak a kezdőbetűk jelentik őket.
Példa:
| nemesgáz | kalkogén |
| Hélium (ő) | Oxigén (O2) |
| monoatomikus: atom alkotja | kovafélék: két atom alkotja |
A nemesgázok stabilitása miatt ennek a családnak az elemei alacsony reaktivitással rendelkeznek, és inertnek is nevezik őket.
5. kérdés
A jelenlegi periódusos rendszer felépítéséről válaszoljon:
a) Mik az oszlopok?
b) Melyek a vonalak?
c) Milyen módszerrel szervezik a kémiai elemeket?
Válaszok:
a) az oszlopok a Periódusos rendszer azon csoportjai, amelyeket korábban családoknak neveztek, és amelyek hasonló tulajdonságú kémiai elemeket hoznak össze.
b) A vonalak a periódusos rendszer periódusai, és az alapállapotban lévő atom elektronikus rétegeinek számát jelzik.
c) Az aktuális periódusos rendszer kémiai elemei az atomszám növekvő sorrendjében vannak elrendezve, amely az atom magjában lévő protonok számát jelzi.
Periódusos rendszerű családok
1. kérdés
(CESGRANRIO) Társítva az alábbi oszlopokat, amelyek a periódusos rendszer szerint megfelelnek az elemcsaládoknak, a numerikus sorrend a következő lesz:
| 1. nemesgázok | • 1A csoport |
| 2. alkálifémek | • 2A csoport |
| 3. alkáliföldfémek | • 6A csoport |
| 4. Kalkogenek | • 7A csoport |
| 5. Halogének | • 0. csoport |
a) 1, 2, 3, 4, 5.
b) 2, 3, 4, 5, 1.
c) 3, 2, 5, 4, 1.
d) 3, 2, 4, 5, 1.
e) 5, 2, 4, 3, 1.
Helyes alternatíva: b) 2, 3, 4, 5, 1.
| csoportok | elektronikus konfiguráció |
| • 1A. Csoport: 2. alkálifémek | minket1 (n-vel |
| • 2A. Csoport: 3. alkáliföldfémek | minket2 (n-vel |
| • 6A. Csoport: 4. Kalkogenek | minket2np4 |
| • 7A. Csoport: 5. Halogének | minket2np5 |
| • 0. csoport: 1. nemesgázok | 1s2 (Ő) vagy mi2np6 (ha n> 1) |
2. kérdés
A Z = 54 vegyi elem vegyértékrétegében az 5s konfiguráció található2 5p6. A Z = 52 és Z = 56 elemek a következők családjába tartoznak:
a) kalkogének és alkáliföldek
b) halogének és lúgok
c) halogének és alkáliföldfémek
d) kalkogének és lúgok
Helyes alternatíva: a) kalkogének és alkáliföldek.
Az atomszámok alapján elvégeztük az elektronikus terjesztést, és a következő eredményeket találtuk:
| 54X és | 52Ön | 56Ba |
|
8 elektron be vegyértékréteg |
6 elektron be vegyértékréteg |
2 elektron be vegyértékréteg |
| Nemesgázok: 8A család | Chalcogens: 6A család | Alkáli Föld: 2A család |
3. kérdés
(F. Ibero-Americana-SP) A periódusos rendszer csoportja, amelyet a mesterséges elemek túlsúlya jellemez, a következő:
a) lantanidok
b) nemesgázok
c) átmenetifémek
d) alkáliföldfémek
e) aktinidek
Helyes alternatíva: e) aktinidek.
A mesterséges elemek azok, amelyek a természetben nem léteznek, és amelyeket a laboratóriumban szintetizáltak nukleáris reakciók útján.
Transzurán elemeknek is nevezik őket, mivel ezen radioaktív elemek atomszáma nagyobb, mint 92, amely megfelel az uránnak.
Általában ezek az elemek rövid életűek, a másodperc töredékéig tartanak.
Ezen információk szerint:
A természetben található elemek a következők: lantanidok, nemesgázok, átmenetifémek és alkáliföldfémek. A mesterséges technécium és a prometium kivételével.
A mesterséges elemek túlsúlya az aktinidek, amelyeket belső átmenetifémeknek minősítenek, és amelyeket a periódusos rendszerbe beillesztenek a lantanidok alá. Ebből a sorozatból csak az aktinium, a tórium, a protactinium és az urán természetes.
4. kérdés
(U. Salvadori Katolikus Egyház-BA) Az X faj2- 8 elektron van a legkülső héjban (valens héj) az X elemből származhat, amely a periódusos rendszerben a következő csoportba tartozik:
a) 7A
b) 6A
c) 2A
d) 1A
e) 8A
Helyes alternatíva: b) 6A.
Az oktett-szabály szerint ahhoz, hogy egy elem stabilitást szerezzen, egy nemesgáz elektronikus konfigurációját feltételezi, amelynek vegyértékhéjában 8 elektron van.
Töltsön 2-et az X fajokra2- azt jelzi, hogy az elem 2 elektronra tett szert.
A legkülső héjban 8 elektronot tartalmazó fajok elektronkonfigurációja ns2np6.
Két elektron elvesztése esetén az elem ns elektronkonfigurációval visszatér alapállapotába2np4.
A vegyértékes héjban található 6 elektron a kalkogénekre, a 6A család elemeire jellemző.
Például:
| Elem: oxigén | elektronikus konfiguráció |
| 8O | 1s22s22p4 |
| faj O2- | 1s22s22p6 |
Tudj meg többet Periódusos rendszerű családok.
Kémiai elemek
1. kérdés
(CESGRANRIO) Tekintettel a 3., 9., 11., 12., 20., 37., 38., 47., 55., 56. és 75. atomszám elemeire, csak alkálifémeket tartalmazó lehetőség:
a) 3, 11, 37 és 55
b) 3, 9, 37 és 55
c) 9, 11, 38 és 55
d) 12, 20, 38 és 56
e) 12, 37, 47 és 75
Helyes alternatíva: a) 3, 11, 37 és 55
Az alkálifémek azoknak a kémiai elemeknek felelnek meg, amelyek az elektronikus elosztást az s alszint elektronjával fejezik be.
A megadott atomszámok elektronikus eloszlása a következő alkálifémekkel rendelkezik:
| Z = 3 | Z = 11 | Z = 37 | Z = 55 |
| Lítium | Nátrium | Rubídium | Cézium |
A többi atomszám a következő csoportok elemeinek felel meg:
Alkáliföldfémek: megszünteti az elektronikus terjesztést az alszinteken2.
| Z = 12 | Z = 38 | Z = 56 |
| Magnézium | Stroncium | Bárium |
Átmeneti fémek: az elektronikus terjesztést a d. Alszinten kell befejezni.
| Z = 30 | Z = 47 | Z = 75 |
| Cink | Ezüst | Rénium |
Halogének: az elektronikus terjesztés befejezése az alszintnél p5.
| Z = 9 |
2. kérdés
(Unirio) „Az Eloiban elhelyezett műszívet négy évvel ezelőtt kezdték kifejleszteni az Egyesült Államokban, és már körülbelül 500 ember használja. A Heartmate névre hallgató készlet három fő darabból áll. A legfontosabb egy négy kilós, 12 centiméter átmérőjű és 3 centiméter vastag kerek táska, amely titánból készül - ezüstfehér fémből, könnyű és erős. ” Veja Magazine, 1999. július.
Az alábbi fémek közül az egyik, amelynek az utolsó rétegében a titánéval megegyező számú elektron van:
a) C
kuka
c) Ga
d) Mg
alkalmazás
Helyes alternatíva: d) Mg.
| Titán | elektronikus konfiguráció | Réteg eloszlás |
| 22Ön | 1s2 2s2 2p6 3s2 3p6 4s2 3d2 | 2, 8, 10, 2 |
A titán elektronikus eloszlásából azt látjuk, hogy ennek az elemnek az utolsó héjában 2 elektron van.
| Elem | elektronikus konfiguráció | Réteg eloszlás |
| 6Ç | 1s2 2s2 2p2 | 2, 4 |
| 11Nál nél | 1s2 2s2 2p6 3s1 | 2, 8, 1 |
| 31Ga | 1s2 2s2 2p6 3s2 3p6 4s2 3d104p1 | 2, 8, 18, 3 |
| 12mg | 1s2 2s2 2p6 3s2 | 2, 8, 2 |
| 54X és | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 | 2, 8, 18, 18, 8 |
Az az elem, amelynek az utolsó héjában 2 elektron is van, a magnézium.
3. kérdés
(UFPA) Tekintsünk egy bizonyos kémiai elemet, amelynek legenergiásabb alszintje az 5s2. Atomszáma és az a csoport, amelyben a periódusos rendszerben található:
a) 20; 1A
b) 20; 2A
c) 38; 2A
d) 38; 1A
e) 39; 2A
Helyes alternatíva: c) 38; 2A
Az elektronikus terjesztés során megállapítottuk, hogy:
- A kémiai elem a családban található 2A, mivel a legenergikusabb alszinttel rendelkezik az s2
- Atomszáma van 38, amely megfelel az elosztott elektronok teljes számának.
- Az ötödik periódusban található, mivel az elektronikus terjesztést az ötödik rétegig végezték.
Ezeket az információkat a periódusos rendszerben ellenőrizve megerősíthetjük, hogy ez a stroncium elem.
4. kérdés
(UFC) Egy x atomnak még egy protonja van, mint egy y atomjának. Ezen információk alapján határozza meg a helyes állítást.
a) Ha y alkáliföld, x alkálifém.
b) Ha y nemesgáz, x halogénatom.
c) Ha y átmeneti fém, x nemesgáz.
d) Ha y nemesgáz, x alkálifém.
e) x ugyanabban az időszakban helyezkedik el a periódusos rendszerben az y atom előtt.
Helyes alternatíva: d) Ha y nemesgáz, akkor x alkálifém.
A periódusos rendszer az atomszám növekvő sorrendjében van elrendezve.
Ha Y-nek z atomszáma van, és X-nek még egy protonja van, akkor ez azt jelenti, hogy ez a két elem azonos periódusban van, és X Y után van.
Példa:
| Elem | következő elem |
| zY | z + 1x |
| 11Nál nél | 12mg |
A két elem a 3. periódusban van, és a magnéziumnak még egy protonja van, mint nátriumnak.
Ezen érvelés szerint:
a) Rossz. Az alkálifém egy alkáliföldfém elé kerül a periódusos rendszerben. A helyes állítás a következő lenne: Ha y alkálifém, akkor x alkáliföld.
b) ROSSZ. A periódusos rendszerben található nemesgáz elé halogén kerül. A helyes állítás a következő lenne: Ha y halogénatom, akkor x nemesgáz.
c) ROSSZ. Az átmenetifémeket és a nemesgázokat más kémiai elemek választják el egymástól, ezért nem egymást követik.
d) Helyes. A nemesgázok az utolsó csoport a periódusos rendszerben, az alkálifémek pedig az első, tehát egymás után következnek.
Példa:
| nemesgáz | alkálifém |
| zY | z + 1x |
| 2ő | 3olvas |
A lítiumnak, amely egy alkálifém, még egy protonja van, mint a héliumnak, amely nemesgáz.
e) Rossz. X ugyanabban az időszakban van, mint Y, de utána nem korábban, mint az alternatív állapotok.
5. kérdés
Egy kémiai elem atomszámából meg lehet tudni:
a) a neutronok száma a magban
b) az elektroszférában lévő elektronok száma
c) a mag tömege
Válasz: b) az elektroszférában lévő elektronok száma
Az alapállapotban lévő atom elektromosan semleges. Tehát, ismerve az atomszámot, amely megfelel a protonok (pozitív töltésű részecskék) számának, ismerjük az elektronok (negatív töltésű részecskék) számát az elektroszférában.
Például a vas atomszáma 26, tehát alapállapotban 26 elektron van a sejtmag körül.
Tudj meg többet kémiai elemek ez a atomszám.
Periodikus és aperiodikus tulajdonságok
1. kérdés
(UFSM) Döntse el, hogy az elemek periodikus tulajdonságaira vonatkozó állítások igazak-e (T) vagy hamisak (F).
() Az elemek atomtömegétől függ.
() Többé-kevésbé szabályos időközönként megismétlik őket az atomszám növekedésével kapcsolatban.
() Hasonlóak ugyanabban az elemcsoportban.
() Az elemek azonos időszakában hasonlóak.
() Ugyanabban a csoportban a periodikus tulajdonságok számértékei mindig növekednek, ha az elemek atomszámának növekedése tapasztalható.
A helyes sorrend:
a) V - F - V - F - F
b) V - F - F - V - V
c) F - V - V - F - F
d) F - V - F - V - V
e) V - F - F - V - F
Helyes alternatíva: c) F - V - V - F - F
(HAMIS) Az elemek atomi tömegétől függ.
Moseley periodicitási törvénye szerint a kémiai elemek számos fizikai és kémiai tulajdonsága atomszám szerint változik.
(IGAZ) Többé-kevésbé szabályos időközönként megismétlik őket az atomszám növekedésével kapcsolatban.
Az olyan tulajdonságok, mint az atom sugara, az atom térfogata, a sűrűség, az olvadáspont és a forráspont, példák azokra a tulajdonságokra, amelyek rendszeresen visszatérnek a periódusos rendszerbe.
(IGAZ) Hasonlóak ugyanabban az elemcsoportban.
A periódusos csoportokat hasonló tulajdonságokkal rendelkező elemekkel rendeztük el.
(HAMIS) Az elemek azonos időszakában hasonlóak.
A tulajdonságok hasonlóak a családokban, nem pedig a periódusokban. Periódusokban az elemeket az elektronikus rétegek száma osztja el.
(HAMIS) Ugyanabban a csoportban a periodikus tulajdonságok számértékei mindig növekednek, ha az elemek atomszámának növekedése tapasztalható.
A tulajdonságok az atomszámtól függően növekedhetnek vagy csökkenhetnek. Erre példa az elektronegativitás, amely az atomszám növekedésével csökken egy adott csoportban.
Olvassa el: Periódusos tulajdonságok
2. kérdés
(FAESP) Az elemek aperiodikus tulajdonságai a következők:
a) sűrűség, atomtérfogat és atomtömeg.
b) olvadáspont, elektronegativitás és fajhő.
c) atomtérfogat, atomtömeg és olvadáspont.
d) atomtömeg, fajlagos hő és olvadáspont.
e) atomtömeg és fajlagos hő.
Helyes alternatíva: e) atomtömeg és fajlagos hő.
Az aperiodikus tulajdonságokat rendszeres időközönként megismételjük.
Az atomtömeg az atom tömegének atomtömeg-egységekben kifejezett mértéke, amely megfelel szén-12 tömeg.
A fajlagos hő határozza meg a hőmennyiséget, amely szükséges az elem 1 g-os hőmérsékletének 1 ° C-kal történő növeléséhez.
Ez a két tulajdonság nem függ össze az elem periódusos rendszerben elfoglalt helyével.
A többi tulajdonság periodikusnak minősül, mivel az atomszámmal együtt növekszik vagy csökken. Vannak:
- Sűrűség: az elem tömegének és térfogatának hányadosa.
- Atomtérfogat: egy atomkészlet térfogatát képviseli és befolyásolja a köztük lévő távolságot.
- Olvadáspont: az a hőmérséklet, amelynél a szilárdból folyadékba való átmenet megtörténik.
- Elektronegativitás: az atom azon képessége, hogy magához vonzza azt az elektronpárt, amelyben kovalens kötésben van.
Olvassa el: elektronegativitás és Elektronikus affinitás
3. kérdés
(PUC-PR) Az alábbi, a periódusos rendszerre vonatkozó diagramok közül melyik helyes?
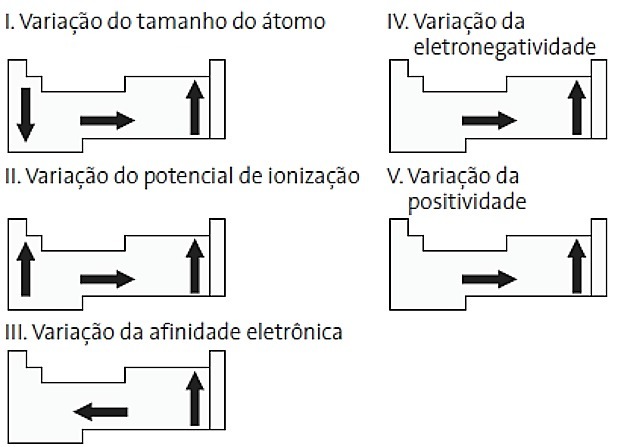
a) II és V
b) II. és III
c) én és V.
d) II. és IV
e) III. és IV
Helyes alternatíva: d) II. És IV.
ÉN. ROSSZ. Az atom méretének változását a mag és a legkülső elektron közötti átlagos távolsággal mérjük. A legnagyobb atomok a táblázat alján helyezkednek el, így a növekedés az atomszám szerint történik, és a helyes ábrázolás:
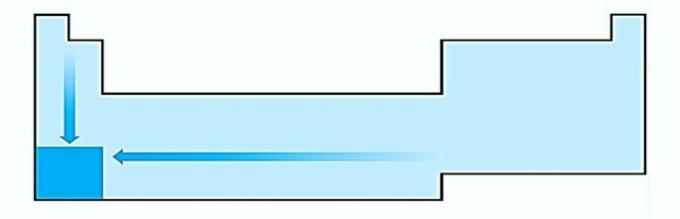
II. HELYES Az energiát, amely ahhoz szükséges, hogy az elektron atom gázállapotban leváljon egy izolált atomról, ionizációs potenciálnak nevezzük. Növeli, ahogy az utasításdiagram mutatja.
III. ROSSZ. Az elektronikus affinitás azt az energiát fejezi ki, amikor egy semleges atom gáz halmazállapotú elektront kap, amely a nemfémek nagyon fontos tulajdonsága. A legnagyobb elektronikus affinitás a halogénekben és az oxigénben figyelhető meg.
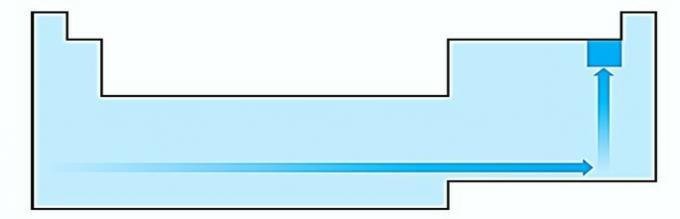
IV. HELYES Az elektronegativitás összefügg az ionizációs potenciállal és az elektron affinitással. Mint ilyen, a halogének a legtöbb elektronegatív elem a periódusos rendszerben.
V. ROSSZ. Az elektropozitivitás az elektronegativitással ellentétes irányban történik. Ez az atom azon képességét képviseli, hogy feladja az elektronokat.
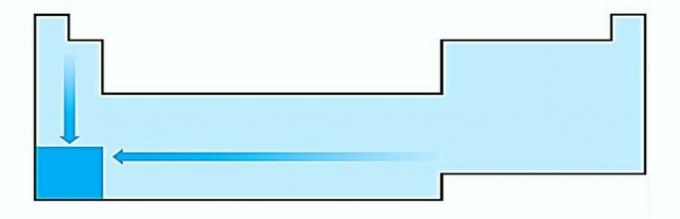
Ezért az alkálifémek rendelkeznek a legnagyobb elektropozitivitással.
Tesztelje tudását folyamatosan a listákkal:
- Gyakorlatok a kémiai kötésekről
- Gyakorlatok az elektronikus terjesztésről
- Gyakorlatok atommodelleken
- Gyakorlatok a termokémiáról
