A szervetlen kémia a kémia azon ága, amely a nem szénvegyületeket vizsgálja. Ennek oka, hogy a szénből készült anyagokat a szerves kémia tanulmányozza.
Kezdetben a szervetlen kémia a kémia azon része volt, amely az ásványi vegyületeket tanulmányozta. Emiatt ásványi kémiának is nevezték.
Eközben a szerves kémia tanulmányozása növényi és állati eredetű vegyületekre irányult.
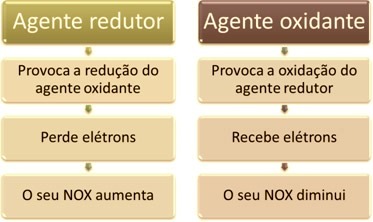
A szervetlen vegyületek fő jellemzője, hogy összetételükben nincs szén. Ezen túlmenően a legtöbb ilyen vegyület fizikai tulajdonsága az, hogy szilárdak. Kémiai tulajdonságként kiemelkedik az a tény, hogy ionosak, ami azt jelenti, hogy elektronokat nyernek vagy veszítenek.
Szervetlen funkciók
Arrhenius javasolta a szervetlen vegyületek csoportosítását. Ez a vízben oldódó és villamos részecskékre, ionokra bomló komponensek felfedezése alapján történt.
Arrhenius elméletéből (1887) a szervetlen vegyületeket a közöttük fennálló hasonlóság szerint csoportosítottuk. Ez megkönnyítette a szervetlen kémia tanulmányozását.
A fő szervetlen funkciók a savak, bázisok, sók és oxidok.
A savak olyan vegyületek, amelyek bázisokkal reagálva sókat és vizet képeznek (semlegesítés). Savanykás ízűek, pH-ja kevesebb, mint 7, vizes oldatban ionizálódnak és keletkeznek, az egyik ion, a H kation+.
Néhány példa savakra: Kénsav (H2CSAK4), Sósav (HCN), sósav (HF).
A savakkal ellentétben a bázisok olyan anyagok, amelyek pH-ja nagyobb, mint 7, és összehúzó, keserű ízűek. Vizes oldatban úgynevezett "ionos disszociáción" megy keresztül, mivel felszabadítja az OH anionját- (Hidroxid).
Néhány példa az alapokra: Nátrium-hidroxid (NaOH), magnézium-hidroxid (Mg (OH)2), Kálium-hidroxid (KOH).
A sók sós ízű ionos vegyületek, amelyek sókkal, savakkal, hidroxidokkal és fémekkel reagálva más sókat képeznek.
Néhány példa a sókra: nátrium-klorid (NaCl), nátrium-bikarbonát (NaHCO3), Nátrium-nitrát (NaNO3).
Az oxidok olyan bináris vegyületek, amelyek oxigént (O) tartalmaznak: sav- vagy anhidrid-oxidok, bázikus oxidok és peroxidok.
Néhány példa az oxidokra: kalcium-oxid (CaO), szén-monoxid (CO), kén-dioxid (SO2).
Tudjon meg többet ezekről a funkciókról: Szervetlen funkciók.
Ban ben szervetlen funkciók gyakorlása felvételi vizsga kérdésekkel is tesztelheti tudását!
Most, hogy tudja, mi a szervetlen kémia, olvassa el azt is:
- Arrhenius-elmélet
- Szerves kémia
- Sav-bázis indikátorok