Mit jelent azt mondani, hogy egy gáz gáznemű átalakuláson ment keresztül?
A kezdeti kérdés megválaszolásához fontos megjegyezni, hogy a gáz vagy a gáz halmazállapotát az állapotváltozók határozzák meg: nyomás, térfogat és hőmérséklet. Hamarosan, a gáztranszformáció ez nem más, mint bármely olyan helyzet, amikor egy bizonyos gázmennyiség változása zajlik a három állapotváltozó egyikében. Amikor egy változó változáson megy keresztül, ennek következtében egy másik változik.
A 17. században számos tudós végzett kísérleteket a gáztranszformációk sajátosságainak feltárására. Közülük megemlíthetjük: többek között Torriceli, Robert Boyle, Mariotte, Guericke. Tanulmányaiban az eljárás az egyik állapotváltozó megváltoztatásából és a többiek viselkedésének megfigyeléséből állt. Ennek során megfigyelték, hogy jelentősen meghatározzák a változó közötti kapcsolatot egy másik pedig arra volt szükség, hogy a harmadik ne változzon, vagyis maradjon állandó. Így a vizsgálatokat három különböző módon hajtották végre, mindegyiknek a sajátosságaival:
izoterm átalakulás, izobár transzformáció és izovolumetrikus transzformáció.Mielőtt részleteznénk a fent említett három transzformációt, emlékezzünk arra, hogy mi a Általános tökéletes gáztörvény: E törvény szerint az állapotváltozók által eredetileg meghatározott gáztömeg (p1, V1 és T1), amikor gázalakú átalakuláson megy keresztül, akkor az állapotváltozók vannak (p2, V2 és T2), amelyek a gáz végső állapotát jellemzik. Ezek a változók a következő összefüggést követik:

A fenti egyenletből láthatjuk, hogy a nyomás, a térfogat és a hőmérséklet a gáztranszformáció során változik.
Izoterm átalakulás illBoyle-Mariotte törvénye: az az átalakulás, amelyben a hőmérséklet T a gáz állandó marad, változtatva a nyomását P és annak mennyisége V. A következő lista érvényes:

Izobár transzformáció illMeleg-Lussac törvény: az az átalakulás, amelyben a nyomás P A gáz mennyisége állandó marad, változtatva annak térfogatát V és hőmérséklet T. A következő lista érvényes:
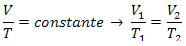
Izovolumetrikus transzformáció vagy Károly-törvény: más néven izometrikus transzformáció, az az átalakulás, amelyben a térfogat V a gáz állandó marad, változtatva a nyomását P és hőmérséklet T. A következő lista érvényes:

Írta: Nathan Augusto
Fizikából végzett
Forrás: Brazil iskola - https://brasilescola.uol.com.br/fisica/as-transformacoes-gasosas.htm

