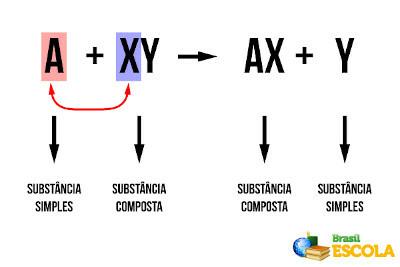
A oktett elmélet Newton Lewis javasolta, aki a vizsgálatok során megfigyelte, hogy atom kölcsönhatás történik hogy minden elem megszerezze a nemesgáz stabilitását, vagyis nyolc elektron a vegyértékréteg. Egyes molekulákban azonban előfordul az úgynevezett oktett tágulása vagy összehúzódása, vagyis a központi atom többé-kevésbé megjósolt kötéseket hoz létre.
Olvassa el: Kovalens kötés - osztályozások és jellemzők
Hogyan működik az oktettelmélet?
Természetesen minden rendszer hajlamos keresni a módját minél nagyobb stabilitást szerezzen, és ez sincs másképp az atomnál. Az atomok bármely anyag „alaprészecskéi”, és mindegyikük szerkezetében elektroszféra található. Ezt az elektroszférát megosztotta a Linus Pauling az energiaszintekben és az alszintekben. Pauling diagramot dolgozott ki annak bemutatására, hogy hogyan néz ki az elektronok eloszlása az atom magja körül.
Lásd az alábbi képet:
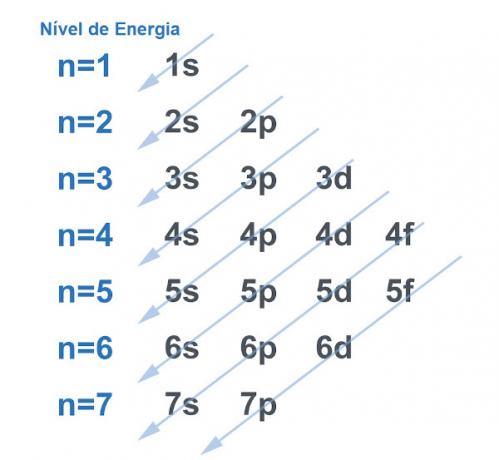
Minden szint és alszint tartalmaz egy mennyiséget elektronok. Hasonlatot véve elmondhatjuk, hogy minden szint polc, és minden alszint doboz. Mindegyik dobozban helyezzen el két elektronot. Az atom akkor stabil, ha minden elektronja párosul, vagyis amikor minden doboz két-két elektronral rendelkezik.
Példa:
Végezzük el az oxigén (O) elektronikus elosztását, amelynek természetes állapotában nyolc elektron van.
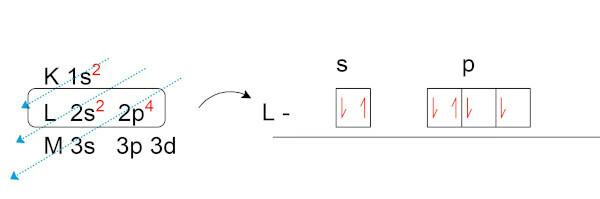
Vegyük észre, hogy a vegyértékrétegben (az L réteg, a p alszintben) van két párosítatlan elektron. Ezek az elektronok létesítik a kémiai kötéseket más elemekkel elektronikus párok kialakítására törekszik.
Az oktett elmélet az elektronok összegzésének matematikáján alapszik. Ha az utolsó elektronhéj összes alszintjén két-két elektron van, akkor a vegyérték-héjnak összesen nyolc elektronja lesz, következésképpen az atom stabil lesz.
Olvassa el: Kvantumszámok - az elektron energiamennyiségéhez kapcsolódó számok
Ne álljon meg most... A reklám után még több van;)
nemesgázok
A nemesgázok az egyetlen elem, amely monoatomikus formában található meg a természetbenazaz anélkül, hogy kötést létesítenénk egy másik atomdal. Ennek oka, hogy elektronikus stabilitás jellemzi őket. Szinte mindegyiknek nyolc elektronja van a vegyértékhéjban., betartva az oktett szabályt, kivéve a héliumgázt, amelynek csak két elektronja van.

Kivételek az oktettelmélet alól
Egyes vegyületek stabilizálódni képesek, ha nyolc vagy kevesebb elektron van a vegyértékes héjban. Ezekben az esetekben kivételek fordulnak elő az oktett elmélet alól.
oktett terjeszkedés
Főleg a foszfor (P) és a kén (S) esetében fordul elő, amelyek viszonylag nagy atomok és „d” alszinttel rendelkeznek. Ebben az esetben az atom több mint nyolc elektronot tart az utolsó héjában.
Példa:
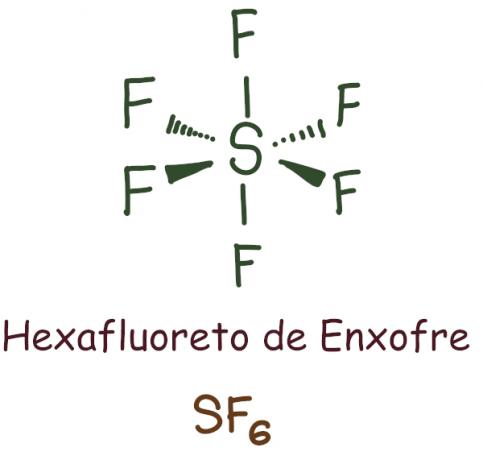
A kén-hexafluorid esetében a központi elem maradt 12 elektron, meghaladja az oktett-szabály szerinti stabilizáláshoz szükséges 8-at. Ebben az esetben az oktett tágulása következett be.
oktett összehúzódás
Berilliummal (Be), bórral (B) és néhánymal történik oxidok nitrogén. Lásd a példát:
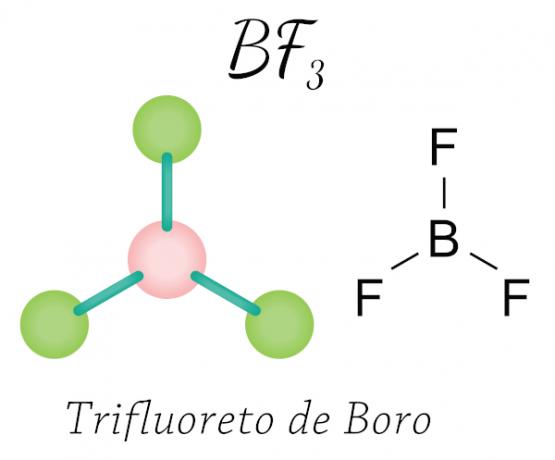
A bór-trifluorid esetében a fluoratomok megosztva jutnak a szükséges nyolc elektronhoz a vegyértékű héjban. elektronikus bórral, tiszteletben tartva az oktett szabályt, de a központi atom (bór) nem stabilizálódik hat elektronral, így fordul elő egy az oktett összehúzódása.
Hozzáférhet továbbá: A szigma link osztályozása: melyek a kritériumok?
megoldott gyakorlatok
1. kérdés - (Mackenzie-SP) Ahhoz, hogy a kén- és káliumatomok a nemesgázzal megegyező elektronikus konfigurációhoz jussanak, szükséges:
(Adatok: S = 16 atomszám; K = 19.)
A) a kén 2, a kálium pedig 7 elektront kap.
B) a kén 6 elektronot, a kálium pedig 7 elektront kap.
C) a kénből 2, a káliumból 1 elektron származik.
D) a kén 6 elektronot, a kálium pedig 1 elektront kap.
E) a kén 2 elektront kap, a kálium pedig 1 elektront ad le.
Felbontás
E. alternatíva A kén a 16. oszlop vagy a 6A család eleme. Ennek a családnak az elemei hajlamosak két elektron befogadására, hogy elektronikus párokat alkossanak, és összesen nyolc elektron van a vegyértékhéjban. Az 1A család elemei, amelyek alkálifémek, a vegyértékhéjban csak egy elektron van. Ennek az elektronnak az adományozásával az előző réteg lesz a vegyértékréteg, már a nyolc elektron mellett, az oktett szabály diktálta.
2. kérdés - Az alábbi állításokat igaznak (T) vagy hamisnak (F) ítélje meg.
I () Az oktett-szabály kimondja, hogy a vegyértékhéjban nyolc elektronra van szükség ahhoz, hogy az atom stabil legyen.
II () A vegyértékréteg az atom második elektronikus rétege.
III () A halogéncsaládból származó klór (Cl) hajlamos két elektron megszerzésére a stabilitás megszerzéséhez.
IV () A nátrium (Na), az 1A család egyik eleme, hajlamos elveszíteni vegyértékű héjában az egyetlen elektront.
Jelölje meg a helyes alternatívát:
A) I, III és IV igaz.
B) I és IV igaz.
C) Csak a II igaz.
D) Csak a IV hamis.
E) Mind igaz.
Felbontás
B. alternatíva I és IV igaz. A II. Állítás téves, mivel a vegyértékréteg az atom utolsó elektronikus rétege, nem a második. A III. Állítás szerint a klór általában két elektront nyer, ami nem ellenőrzi, mivel a klór származik A 7A. Vagy 17. Családban általában csak egy elektront nyer, hogy így megszerezzék a gáz elektronikus konfigurációját nemes.
Írta: Laysa Bernardes Marques de Araújo
Kémia tanár