O ammónium-nitrát szilárd anyag, amelynek molekuláris képlete NH4A3 fehér megjelenés (tiszta). alkotott valami által ionok NH4+ (ammónium) és NO3- (nitrát), nem gyúlékony, de erősen oxidáló és reaktív. Bomlási reakciójaként termékként nagy mennyiségű gáz keletkezik, ami komoly problémát jelent a termék nem megfelelő tárolása miatt, mivel robbanások léphetnek fel. És még széles körben használják a mezőgazdaságban műtrágyaként.
Olvassa el: Természetes anyagok - a természetből származó molekulák
Mi az ammónium-nitrát?

Ammónium-nitrát ez egy só NH-ionok alkotják4+ (ammónium) és NO3- (nitrát). Ez egy szilárd vegyület, amikor tiszta, fehér színű. Széles körben használják mezőgazdasági műtrágyaként, de robbanóanyagok gyártásában is használható, mint nagyon oxidáló anyag, majd oxidálódik. Az ammónium-nitrát elszabaduló reakciója nagy mennyiségű gázok, okozó robbanásveszélyes hatás.
Az ammónium-nitrát jellemzői
Molekulatömeg: 80,04336 g / mol.
Az ionokból álló só: ammónium (NH4+) és nitrát (NO3-).
Megjelenés: fehér szilárd anyag.
Erős oxidálószer.
Könnyen reagál más anyagokkal.
Nem gyúlékony.
Normál hőmérsékleti és nyomási körülmények esetén:
- sűrűség: 1,73 g / cm3;
- forráspont: 210 ° C;
- olvadáspont: 169,6 ° C;
- vízben való oldhatóság mértéke: 216 g / 100 ml;
- pH: 5,5 (0,2 M).
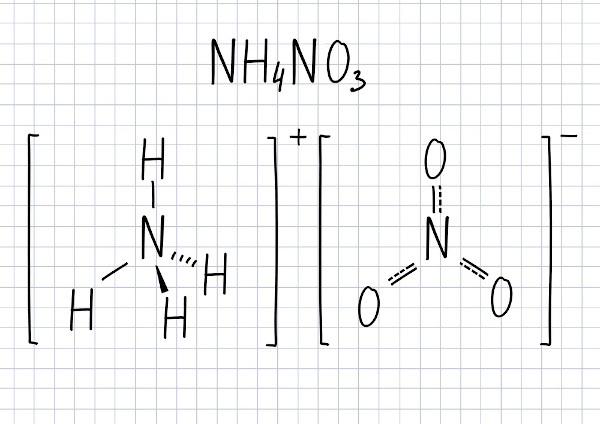
Ammónium-nitrát képlet
Ennek a vegyületnek a molekulaképlete NH4A3.
Az ammónium-nitrát bomlása
amiért a nagy reakcióképességű és nagy oxidáló képességű anyag, az ammónium-nitrát magas hőmérsékletnek kitéve kiváltja a bomlási reakció, és a fő termékek gázok, nitrogén, oxigén és vízgőz. A bontást két lépésben adják meg:
→ 1. lépés:
2NH4A3 (s) → 2N2O (g) + 4H2O (g)
→ 2. szakasz:
2N2O → 2N2(g) + O2g)
→ Globális egyenlet:
2NH4A3 (s) → 2N2(g) + O2(g) + 4H2O (g)
Vegye figyelembe, hogy az első egyenletbenaz egyik termék a bomlás során kapott az dinitrogén-oxid (N2O), más néven nevetőgáz. Az autómotorok üzemanyag-elégető képességének növelésére és érzéstelenítőként használják, elsősorban a fogorvosok. Ez is az egyik fő gáz, amely felelős üvegházhatás.
Lásd még: Milyen típusú kémiai reakciók vannak?
Ammónium-nitrát termelés
Ammónium-nitrátot a következő módon nyerhetünk: reakció ammónium-szulfát (NH4) között2CSAK4 és kalcium-nitrát Ca (NO3)2. Lásd lentebb:
(NH4)2CSAK4 + Ca (NO3)2 → 2 NH4A3+ Ügy4
Előállítható gáznemű ammóniából is, amelyet salétromsavoldatban buborékoltatunk meg, reakciótermékként vizes ammónium-nitrátot tartalmazva. Néz:
NH3. g) + HNO3 (aq) → NH4A3(itt)
Az ammónium-nitrát felhasználása

- Műtrágyagyártás
- Robbanóanyagok bányákban, kőbányákban és építőiparban
- Gyomirtó és rovarölő szerek
- Dinitrogén-oxid előállítása ipari felhasználásra
- Oxidok abszorbensei
- Oxidáns a rakétahajtóművekhez
- Izoterm zsákok gyártása
- Érzéstelenítő füst előállítása a méhészeti csalánkiütés kezelésére
Hozzáférhet továbbá: Hogyan lehet oltani a tüzet?
Ammónium-nitrát veszélyek
Az ammónium-nitráttal kapcsolatos egyik fő kockázat az nem megfelelő tárolás. Mivel nagyon oxidáló anyag és számos más vegyülettel reagál, kiváltja a reakció nagy mennyiségű gáz felszabadulásával. A nem megfelelő tárolás gyúlékony termékekkel való szennyeződésnek, hőhatásnak vagy gáz visszatartásnak van kitéve, mi okozhat robbanásokat.
Ez történt például az Egyesült Államokban Texasban, egy Franciaországból érkező teherhajóval, amely 2086 tonna ammónium-nitrátot szállított. megtörtént a baleset 1947-ben és Texas City Katasztrófa néven vált ismertté. A tragédia 581 ember halálát okozta és ez a hajóban nem lévő tűz miatt következett be, amely elérte az ammónium rakományt, és kiváltotta a robbanást.
Egy másik példa a robbanássorozat ami 2020. augusztus 4-én történt a Bejrút városa, Libanon, több mint 100 ember meghalt és 5000 megsebesült. A robbanás nagysága az ott tárolt 2750 tonna ammónium-nitrát rakomány láncreakciójának meggyulladása volt.
Azt is érdemes megjegyezni, hogy az ammónium-nitrát okozhat bőr- és szemirritáció és ha belélegzik, légzési gondok. A véráramban az anyag mérgező erővel rendelkezik, mivel reagál a testnedvekkel, és ennek a reakciónak a termékei, például a nitrát, egészségkárosodást okozhatnak, mint pl. kék baba betegség, más néven infantilis methemoglobinemia (alacsony vér hemoglobinszint). Ez a betegség a vidéki területek családjaiban ismétlődik a műtrágyákban jelen lévő ammónium-nitráttal való szennyeződés miatt a mezőgazdasági régió víztestjeiben.
írta Laysa Bernardes
Kémia tanár
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/nitrato-de-amonio.htm
