Az atomok végtelenül kis részecskék, amelyek az univerzum összes anyagát alkotják. Idővel a tudósok új felfedezései alapján megváltozott az elképzelés arról, hogy milyen lesz az atomszerkezet. Erről többet megtudhat a szövegbenAz atommodell alakulása.
A modell a valóság (nem maga a valóság) reprezentációja, tehát az atomi modellek a reprezentációi az atom fő összetevői és szerkezete, és megmagyarázza az anyag bizonyos fizikai és kémiai viselkedését. Ezt azért teszik, mert az ember még ultramikroszkópokkal sem képes izolált atomot látni.
Ha képet szeretne kapni arról, hogy milyen kicsi az atom, ismerje meg ezt A A hétköznapi mikroszkóp alatt látható legkisebb részecske több mint tízmilliárd atomot tartalmaz! Az atom olyan kicsi, hogy, ha egymilliót teszünk egymás mellé, nem érnénk el a hajszál vastagságú.
Elmetérkép: Atom
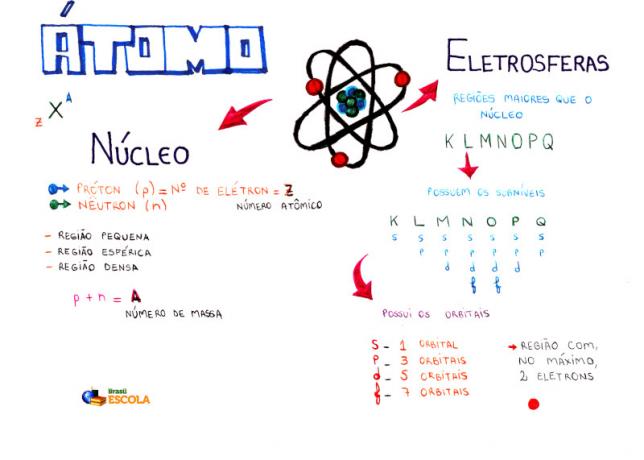
* A gondolattérkép PDF formátumban történő letöltéséhez Kattints ide!
Az atommodellek közül a Rutherford-Bohr modell az, amelyet jelenleg a középiskolában használnak az atom szerkezetének és tulajdonságainak megértésére. E modell szerint az atom szerkezete két fő részből áll: a
mag és a elektroszféra.
Az atom szerkezetének két fő része - az elektroszféra és a mag
* Mag: Az atom központi részeként tömör, tömör, masszív és nagyon sűrű, emellett nagyobb tömegű részecskék alkotják, amelyek protonok és neutronok.

Az atommagot alkotó protonok és neutronok illusztrációja
- Protonok: pozitív elektromos töltéssel rendelkező részecskék (relatív töltés = +1; töltés coulombban (C) = +1,602. 10-19), relatív tömege pedig 1.
Azt a tényt, hogy a protonok alkotják a magot, és összességében pozitív töltést adnak neki, felfedezte Eugen Goldstein, 1886-ban, Crookes ampullájának módosításával és néhány kísérlettel. Látta, hogy nagyon magas feszültség alatt kibocsátások jelentek meg (anódsugarak - az izzó belsejében lévő gázmaradványok, amelyeknek elektronjait az elektromos kisülés letépte). Az elektromos vagy mágneses mező elhelyezésével az izzón kívül ezeket a sugarakat a negatív pólus felé terelték. Ez azt jelentette, hogy voltak pozitív szubatomi részecskék, amelyeket protonoknak neveztek.
Később, Ernest Rutherford (1871-1937) elvégezte a szövegben leírt kísérletet Rutherford Atomja, ami arra késztette, hogy felfedezze a proton helyét: a magban.
- Neutronok: részecskék, amelyek tömege megegyezik a protonokéval (1), de mint a neve is mutatja, semlegesek, vagyis nincs elektromos töltésük.
A neutronokat 1932-ben fedezte fel James Chadwick (1891-1974), aki rájött, hogy a radioaktív berillium magja semleges részecskéket bocsát ki, amelyek tömege nagyjából megegyezik a protonok tömegével (valójában ez valamivel nagyobb).
Ne álljon meg most... A reklám után még több van;)
A mag átmérője az atom proton- és neutronmennyiségétől függ, de átlagosan 10 körüli-14 hónap és 10-15 m.
Az atommag gyakorlatilag az atom teljes tömegét koncentrálja, nagyon kis részként: mind a proton, mind a neutron körülbelül 100 000-szer kisebb, mint maga a teljes atom! Összehasonlításképpen képzeljük el, hogy megnöveljük a hidrogén elem atomjának magját (amelynek csak van egy proton) teniszlabda méretére, a legközelebbi elektron körülbelül három kilométerre található távolság! Még akkor is, ha egy atomot egy 14 emeletes épület magasságára nagyítanának meg, annak magja akkora lenne, mint egy egyszerű sószem a hetedik emeleten. Tényleg valami csodálatos, nem gondolod ?!
* Elektroszféra: Is régió, ahol az elektronok a mag körül forognak. Annak ellenére, hogy a magnál jóval nagyobb térfogatú régió, gyakorlatilag üres, mivel minden elektron 1836-szor kisebb, mint 1 proton (vagy 1 neutron). Ezért az atom tömege gyakorlatilag minden a magban van. Az elektronok negatív elektromos töltéssel rendelkező részecskék (-1).
Az elektronokat 1897-ben fedezte fel Joseph John Thomson (1856-1940), a Thomson atommodell. Thomson kísérlete részletesen látható a szövegben Thomson kísérlete elektromos kisülésekkel, de röviden: felhasználta a fent említett Crookes ampullát, és rájött, hogy a katódsugarak mindig vonzza a pozitív pólus, ami bebizonyította, hogy az atom negatív részecskékkel rendelkezik, amelyeket ún elektronok.
Az elektronok másodpercmilliomod másodpercenként milliárdszor forognak a sejt körül, megformálva az atomot és úgy viselkedve, mintha szilárd lenne.
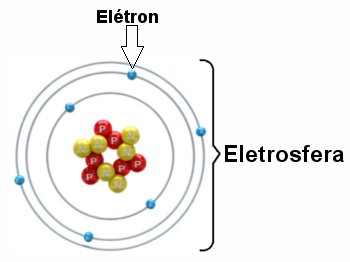
Illusztráció egy elektroszféráról, amelyben három elektronikus réteg és az elektron körül forog a sejtmag.
Röviden, táblázatot készíthetünk az atom szerkezetének részét képező három fő szubatomi részecske megkülönböztetésére:

A három fő szubatomi részecske - protonok, neutronok és elektronok - tömege és elektromos töltése
Az összes kémiai elem atomjai ebből a három szubatomi részecskéből állnak. Az a vegyi elem különbözik a másiktól, hogy mekkora mennyiségben jelennek meg ezek a részecskék, főleg a protonok mennyisége a magban, amelyet atomszámnak hívnak. Tanulmányozza tovább a szövegen keresztül. Kémiai elem.
* Elmetérkép készítette: Diogo Lopes
Írta: Jennifer Fogaça
Kémia szakon végzett
Kémia
Anyagok, víz, hidrogén-cianid gáz, szén-dioxid, ammónia, hidrogén, hélium, anyagok osztályozása egyszerű, összetett anyagok, keverékek, keverékfázisok, homogén keverék, keverék heterogén.



