Valamint a ciklánok, alkének, alkinek, többek között a alkadiének szintén szenvedik a hívásokat addíciós reakciók. A szövegben kb diének reakciói, azt fogja tapasztalni, hogy az addíciós reakciók a dolgozott dién típusától függenek. A diének nagyjából a következő csoportokba sorolhatók:
sűrített vagy felhalmozódott (nincs egyetlen kötés a két páros között);
Például: H2C = CH-CH3
konjugálva vagy váltakozva (csak egyetlen kötés van a két kettős között);
Például: H2C = CH — CH = CH2
izolált (legalább két egyszeres kötés a két páros között).
Például: H2C = CH-CH2—CH2—CH = CH2
A Diels-Alder reakció 1928-ban két német vegyész, Otto Paul Hermann Diels és Kurt Alder fejlesztette ki. Ez egy nagyon fontos reakció a szerves kémia területén, mivel lehetővé teszi:
azonosítsa a dién szénhidrogéneket;
telített gyűrűs szénhidrogéneket kapunk (előnyösen ciklohexánok).
Ez a szerves reakció csak alkadiének vagy konjugált vagy váltakozó diének és hívják 1.4. kiegészítés. A vegyület, amelyben egyszerűbben megfigyelhetjük az 1,4-addíciót, a but-1,3-dién, az alábbiakban látható:
H2C = CH — CH = CH2
JEGYZET: Ebben a vegyületben előfordulunk rezonancia jelenség, amelyben a két pi kötés elektronjai a láncon keresztül mozognak. Egy pár pi elektronok elfoglalni kezdi a lánc központi régióját (2. és 3. szénatom között), míg a másik pi-kötés elektronjai eltolódnak az egyik végszénhez. Így van kötőhelyünk az 1. és 4. szénatomon, kettős pedig a 2. és 3. szénatomon.

Rezonancia a but-2,3-dién szerkezetben
Ne álljon meg most... A reklám után még több van;)
Nál nél Diels-Alder reakció, az egyik reagens egy konjugált dién, míg a másik egy szerves vegyület, amely jelen lehet Hívás kettős a szénatomok között. Az alábbiakban egy példa a Diels-Alder reakció but-2,3-dién és propén között:
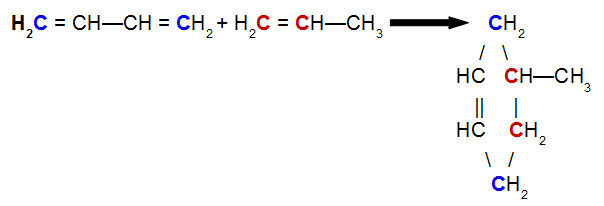
A but-2,3-dién és a propén Diels-Alder reakciójának egyenlete
A fenti egyenlet elemzésével láthatjuk, hogy a but-2,3-dién kötés 1. és 4. szénatomja (mindkettő kék színű) illetve propén 1-es és 2-es (mindkettő vörös) szénatomjára, ami elágazó szénláncú ciklént eredményez, 4-metil-ciklohexén. Ennek oka a but-2,3-dién molekula rezonanciája, amely elmozdítja a pi kötést a 2. és 3. szénatom között, valamint a pi kötés megszakadása a propén 1. és 2. szénatomja között.
OBS.²: Fontos hangsúlyozni, hogy a konjugált alkadiénnel reagáló vegyülettől függetlenül a pi-kötésben csak a szénatomok között lesz szakadás a láncban. Ha a szerkezetnek a szénatomon kívüli atomjai között pi-kötései vannak, akkor azok nem szakadnak meg. Az alábbiakban bemutatunk egy olyan szerkezetet, amely képes reagálni az a-val alkadién a Diels-Alder reakció, ami a kettős kötés (kék színű) szénatomjai közötti pi-kötés megszakadását eredményezi.
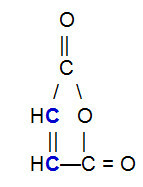
A maleinsavanhidrid szerkezeti képlete
Általam. Diogo Lopes Dias
Hivatkozni szeretne erre a szövegre egy iskolai vagy tudományos munkában? Néz:
NAPOK, Diogo Lopes. "Diels-Alder reakciók"; Brazil iskola. Elérhető: https://brasilescola.uol.com.br/quimica/reacoes-diels-alder.htm. Hozzáférés: 2021. június 28.
Kémia

Alkének, gáz, etén, etilén, műanyagok, szintetikus kaucsuk, színezékek, szintetikus szövetek, robbanóanyagok, ásványolaj-krakkolás, polietilén, olefáns gáz, olefinek, szénhidrogének, lánc aciklusos szén-dioxid.



