A szövegben "Cím vagy tömegszázalék”Láttuk, hogyan lehet kiszámítani az oldott anyag és az oldat tömege közötti arányt szilárd, folyékony és gáznemű oldatok esetében. Ebben a szövegben azonban látni fogjuk, hogy a titer mennyisége is kiszámítható folyékony vagy gáz halmazállapotú oldatok esetén.

A cím a kötetben a következő kifejezéssel számolható:
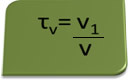
Tekintsük példának az antiszeptikus és fertőtlenítőszerként használt etil-alkohol vizes oldatát, amely volt úgy állítjuk elő, hogy 70 ml tiszta alkoholt adunk annyi vízhez, hogy 100 ml térfogatot töltsünk fel megoldás. Tehát van:
τ = 70 ml = 0,7
100ml
A címet százalékban is kifejezhetjük, csak megszorozva az eredményt 100% -kal. Tehát ebben az esetben 70% -os etil-alkohol-oldattal rendelkezünk, ami azt jelenti, hogy az oldat minden 100 térfogategységéből 70 térfogategység alkohol.
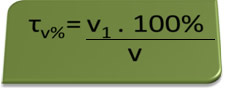
Az alábbi esetben 70% -os etil-alkohol-oldatot alkalmazunk 250 ml térfogatú oldatban; ami azt jelenti, hogy 175 ml alkohol a számítások szerint:
100 ml 70 ml alkohol
250 ml x
x = 70. 250
100
X = 175 ml alkohol

Azt azonban nem mondhatjuk, hogy ebben az esetben 75 ml (250-175) vízünk van. Ellentétben a tömegtiterrel, amelyben az oldószer tömegét hozzáadhatjuk az oldott anyag tömegéhez, hogy megtaláljuk az oldat tömegét, ezt nem lehet megtenni a térfogat-titerhez viszonyítva.

Ne álljon meg most... A reklám után még több van;)
Ez azt jelenti, hogy az oldat térfogata nem egyenlő az oldószer térfogatának és az oldott anyag térfogatának összegével (bár a különbség gyakran elhanyagolhatónak tekinthető). Ezekben a folyadékokban meglévő intermolekuláris erők ugyanis befolyásolják a végső térfogatot.
A fent említett oldat esetében például az etil-alkohol, amikor az alkoholt vízzel keverjük, az oldat teljes térfogatának összehúzódása következik be; vagyis a végső térfogat kisebb lesz, mintha csak az alkohol és a víz térfogatát adnánk hozzá. Az alkoholmolekulák ugyanis kötéseket vagy hidrogénkötéseket hoznak létre a vízmolekulákkal, csökkentve a köztük lévő tereket.
Ezért ebben és más esetekben az oldat térfogatát kísérletileg kell mérni, ha ez nem szerepel a gyakorlatban.
A térfogatszázalékot széles körben használják alkoholos italok és kereskedelmi alkoholok esetében, amint azt fentebb említettük. Lásd a számítás két fontos alkalmazását:
- Alkoholszonda: az alkoholszonda az etil-alkohol koncentrációját méri a vérben, Brazíliában pedig tilos bárkinek bármilyen járművet vezetnie, amelynek véralkohol-tartalma legalább 0,1 térfogatszázalék. Az ilyen alkoholtartalmú személy minden liter vérre 1 ml alkoholt tartalmaz, amit a következő számítások mutatnak:
τv%=V1. 100%
v
0,1 % = V1. 100%
1L
V1 = 0,1% → V1 = 0,001 L = 1 ml
100%

- Etanoltartalom a benzinben: Brazíliában a benzint etanol hozzáadásával szabályozzák. De a benzin etanoltartalma legfeljebb 24 térfogatszázalék vízmentes alkohol lehet (mivel a benzinnek vízmentesnek kell lennie). Minél több etanolt adunk a benzinhez, annál inkább világosabb lesz az üzemanyag színe és növekszik a sűrűsége.
Írta: Jennifer Fogaça
Kémia szakon végzett
Hivatkozni szeretne erre a szövegre egy iskolai vagy tudományos munkában? Néz:
FOGAÇA, Jennifer Rocha Vargas. "Kémiai megoldás kötetcíme"; Brazil iskola. Elérhető: https://brasilescola.uol.com.br/quimica/titulo-volume-uma-solucao-quimica.htm. Hozzáférés: 2021. június 28.
Kémia

Hogyan működik a Légzőkészülék, az alkohol koncentrációja, az alkoholos készülék, az etil-alkohollal kapcsolatos reakciók, a alkoholszonda, kálium-dikromát, üzemanyagcella, katalizátor, elektron felszabadulás, ecetsav, hidrogén, conce


