Amikor különböző elemeket vetünk alá egy láng működésének, észrevesszük, hogy mindegyik más színt bocsát ki. Például, ha stronciumot, nátriumot és réz sót égetünk, akkor a piros, intenzív sárga és zöld színeket látjuk, amint azt a következő ábra mutatja:

Ha e lángok fénye egy prizmára esik, a szakaszos spektrum, vagyis csak néhány színes fényes vonal figyelhető meg fény nélküli régiókkal tarkítva. Minden elemhez más lesz a spektrumunk.

Ezeket a spektrumokat nevezzük emissziós spektrum, mivel egy bizonyos elem adta ki őket, és annak azonosítására szolgálnak.
Ilyen spektrumokat lehet kapni egy fénysugár segítségével, amelyet magasan egy elektromos kisülési csőben hoznak létre hőmérsékletek és alacsony nyomások, amelyek bizonyos elemek gázait tartalmazzák, például hidrogént, vagy nemesgázokat ordít:

A prizmán keresztül előállított elektromágneses sugárzás (fény) áteresztésével ezen elemek mindegyikének emissziós spektrumát kapjuk.
Korábban azt gondolták, hogy az elért napspektrum teljesen folyamatos, de William Hyde Wollaston angol tudós megállapította, hogy nagyon keskeny fénysugárral dolgozva, körülbelül 0,01 mm réssel, láthatta, hogy a napspektrum hét fekete vonalat tartalmaz erről. Később a fiatalok
Joseph Fraunhofer (1787-1826) prizmák és diffrakciós rácsok segítségével megállapította, hogy a napspektrum valójában több ezer egymásra helyezett fekete vonalat tartalmaz.Valamivel később a fizikai Gustav Robert Kirchhoff észrevette, hogy a nátrium-spektrum által elért sárga foltok pontosan ugyanabban a helyen vannak, mint két fekete vonal a Nap spektrumában. ő és a vegyész Robert Wilhelm Bunsen több kísérletet végzett és észrevette, hogy ha a Bunsen-égőből származó fehér fény, például a napfény, elhalad a nátrium által kibocsátott sárga fény mellett, és a spektrum előállításához keresztezik a prizmát; az eredmény egy folyamatos napspektrum lenne, szivárvány színben, de a fekete vonalak (Fraunhofer által D vonalaknak nevezik) ugyanabban a helyzetben, mint a nátrium spektrum sárga vonalai.
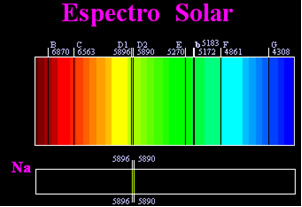
A Nap minden színű fényt bocsát ki, a vöröstől az ibolyáig, azonban a Föld légkörén áthaladva a jelenlévő gázok pontosan elnyelik a Nap fényét az általuk kibocsátott színekben.
Ezeket a spektrumokat nevezzük abszorpciós spektrumok.
Ezen megfigyelések alapján Kirchoff hármat létrehozott törvényeket spektroszkópiához, amelyek:
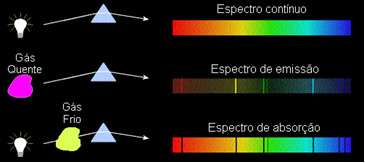
1) Egy test áttetsző forró, a három fizikai állapot bármelyikében spektrumot bocsát ki folyamatos.
2) Egy gáz átlátszó - mint a fenti nemesgázoké - a emissziós spektrummegjelenésével vonalak fényes. E vonalak számát és helyzetét a gázban lévő kémiai elemek határozzák meg.
3) Ha a folyamatos spektrum halad át egy gázon a legalacsonyabb hőmérsékleten a hideg gáz okozza a jelenlétét sötét vonalak, az egy abszorpciós spektrum. Ez történt a nátriumgázon áthaladó napfény spektrumával. Ebben az esetben az abszorpciós spektrumban lévő vonalak száma és helyzete a gázban lévő kémiai elemektől is függ.
Írta: Jennifer Fogaça
Kémia szakon végzett
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/espectros-emissao-absorcao-leis-kirchhoff.htm
