O kiszámítása atomtömeg egy elem az a matematikai erőforrás, amelyet a meglévő kémiai elemek periódusos rendszerében lévő tömegérték meghatározásához használnak. Általában a atomtömeg számítás, ismernünk kell a kémiai elem:
Elem izotópok;
Az elem egyes izotópjainak tömegszáma;
Az elem egyes izotópjainak százaléka a természetben.
A hidrogénatom tömegének kiszámítását például a következő adatok alapján hajtották végre:
Bemutatja a protium izotópokat (H1), deutérium (H2) és a trícium (H3);
Ezen izotópok tömege 1, 2, illetve 3;
A Protium aránya a természetben 98,9%;
A deutérium aránya a természetben 0,09%;
A trícium százalékos aránya a természetben 0,01%.
Matematikai standard az atomtömeg kiszámításához
Végezni a atomtömeg számítás bármely kémiai elem esetében a következő matematikai mintát kell használnunk:
1O: szorozzuk meg az egyes izotópok tömegszámát százalékukkal;
2O: adja hozzá az összes eredményt, amelyet az első lépés szorzataiban talált;
3O: ossza el a talált összeget 100-mal.
M.A. = tömegszám.százalék + tömegszám.százalék
100
Elmetérkép: Atomi mise
* A gondolattérkép PDF formátumban történő letöltéséhez Kattints ide!
Példák az atomtömeg kiszámítására
⇒ 1. példa: A kén atomtömegének kiszámítása.
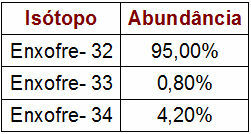
A kénizotópok százalékos és tömegadatai
A megadott táblázat az egyes kén-izotópok tömegszámát és százalékát mutatja a természetben. Az atomtömeg kiszámításához egyszerűen hajtsa végre a következő lépéseket:
1O Lépés: szorozzuk meg az egyes izotópok tömegszámát a bőségük értékével.
Kén - 32 (S32)
s32 = 32.95
s32 = 3040
Kén - 33 (S33)
s33 = 33.0,8
s33 = 26,4
Kén - 34 (S34)
s34 = 34.4,2
s34 = 142,8
2O Lépés: add hozzá a tömegszám és az izotóp rengetegének szorzatában talált értékeket.
Összeg = S32 + S33 + S34
Összeg = 3040 + 26,4 + 142,8
Összeg = 3209,2
3O Lépés: számítsa ki az atomtömeget úgy, hogy a kapott eredmények összegét elosztja 100-mal:
M.A. = Összeg
100
M.A. = 3209,2
100
M. = 32,092 u
⇒ 2. példa: Egy adott kémiai elemnek (D) három izotópja van, amelyek tömegszáma:
30D 32D 34D
Tudva, hogy ennek az elemnek az atomtömege 32,20 u, és az izotóp 20% -a van 32D jellegű, mi az értéke a többi izotóp százalékának?
Az utasítás megadja az egyik izotóp tömegszámát, atomtömegét és százalékos arányát. A többi izotóp százalékának meghatározásához a következő lépéseket kell végrehajtanunk:
1O Lépés: meghatározza az egyes izotópok százalékos arányát.
Izotóp - 30 (DS30)
DS30 = 30.x
DS30 = 30x
Izotóp - 32 (DS32)
DS32 = 32.20
DS32 = 640
Izotóp - 34 (D34)
DS34 = 34.y
DS34 = 34y
2O Lépés: az atomtömeg kiszámításához használja a matematikai kifejezésben található összes adatot.
M.A. = tömegszám.százalék + tömegszám.százalék
100
32,2 = 30x + 640 + 34év
100
32,2.100 = 30x + 640 + 34év
100
3220-640 = 30x + 34év
30x + 34y = 2580
x = 2580 - 34y
30
3O Lépés: használja a fenti kifejezést a következő érvelésből:
Az 1. izotóp százaléka + A 2. izotóp százaléka + A 3. izotóp százaléka = 100%
x + 20 + y = 100
x + y = 100-20
x + y = 80
x = 80 - y
2580 - 34y = 80-év
30
2580 - 34y = 30. (80 éves)
2580-34 y = 2400-30y
2580 - 2400 = 34y-30y
4y = 180
y = 80
4
y = 45%
4O Lépés: számítsa ki az x százalékos értékét a harmadik lépésben létrehozott kifejezésben.
x + y = 80
x + 45 = 80
x = 80 - 45
x = 35%
Általam. Diogo Lopes Dias
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/calculo-massa-atomica.htm
