THE klapejronska jednadžba je matematički izraz koji povezuje veličine kao što su pritisak (P), volumen (V), temperatura (T) i broj čestica (n) koje čine a savršen ili idealan plin. Ova je jednadžba dobila ime po francuskom fizičaru Pavaoemilirati seklapejron i može se shvatiti kao uopćavanje empirijskih zakona plinovisavršenuGay-Lussac, Charles i Boyle. Bila je temeljna za proučavanje idealnih plinova i omogućila je razvoj Termički strojevi, što ih čini sve učinkovitijima tijekom posljednjih nekoliko desetljeća.
Pogledajte i: Otkrića fizike koja su se dogodila nesrećom
Clapeyronova jednadžba: zakon idealnog plina
Clapeyronova jednadžba je izveden iz tri empirijska zakona, odnosno zakoni koji su utvrđeni eksperimentima. Takvi zakoni objašnjavaju ponašanje plinova u transformacije plinaizovolumetrijski (Gay-Lussac zakon), izobarna (Charlesov zakon) i izoterme (Boyleov zakon). Prema ovim zakonima:
u transformacijama izovolumetrijski, omjer tlaka i termodinamičke temperature idealnog plina ostaje konstantan;
u transformacijama izobarno, omjer zapremine i termodinamičke temperature idealnog plina je konstantan;
- u transformacijama izotermeumnožak tlaka i volumena idealnog plina ostaje konstantan.
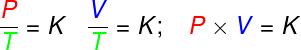
Str - pritisak (Pa - pascal)
V - količina plina (m³)
T - termodinamička temperatura plina (K - kelvin)
Iz tri gore navedena zakona, Clapeyronova jednadžba određuje koja je vrijednost toga konstantno (K) dobiven u svakoj od gore spomenutih transformacija. Prema Clapeyronovoj jednadžbi, ta je konstanta jednaka broju molova pomnoženih s a konstanta R, poznata kao univerzalna konstanta idealnih plinova i jednaka Boltzmannova konstanta pomnoženo sa Avogadrov broj.
Formula
Pogledajte formulu koja je poznata kao jednadžbauClapeyron:
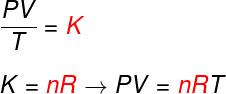
Ne - broj molova (mol)
R - univerzalna konstanta idealnih plinova (R = 0,082 atm.l / mol. K ili 8,314 J.mol / K)
Analizirajući Clapeyronovu jednadžbu, moguće je vidjeti da je pritisak koji vrše idealni plinovi je izravno proporcionalna temperaturi a također i do broj madeža. Nadalje, tlak je obrnuto proporcionalan volumenu zauzeta plinom.
O model idealnog plina omogućeno Clapeyronovom jednadžbom široko se koristi za razvoj strojeva koje pokreće tekućine, kao što su strojevi na parni pogon i motori s unutarnjim izgaranjem.
Iz Clapeyronove jednadžbe moglo bi se dobiti nekoliko važnih rezultata. Na primjer, jedan od njih predviđa da 1 mol bilo kojeg idealnog plina zauzima zapreminu 22,4 l kada se podvrgne pritisku od 1 atm (1,01.105 Pa) i na temperaturi od 273.000 (0 ° C).
Pogledajte i: Najvažniji pojmovi u termologiji
Riješene vježbe na Clapeyronovoj jednadžbi
Pitanje 1 - (UECE) Plin kojem temperatura, volumen i tlak mogu biti povezani PV = nRT ima sljedeće značajke:
a) vrlo velika prosječna udaljenost između molekula kako bi se zanemarile intermolekularne interakcije, osim kada se sudaraju; molekule se podvrgavaju elastičnim sudarima.
b) vrlo mala srednja udaljenost između molekula; molekule se podvrgavaju neelastičnim sudarima.
c) vrlo velika srednja udaljenost između molekula kako bi se zanemarile intermolekularne interakcije, osim kada se sudaraju; molekule se podvrgavaju neelastičnim sudarima.
d) vrlo velika srednja udaljenost između molekula i s jakim intermolekularnim interakcijama; molekule se podvrgavaju elastičnim sudarima.
Razlučivost:
U modelu idealnog plina velik broj bezdimenzionalnih čestica kreće se velikom brzinom u slučajnim smjerovima. Jedine interakcije koje trpe ove čestice su savršeno elastični sudari, pa je ispravna alternativa slovo A.
Pitanje 2 - (UFRGS) Razmotrite sljedeće izjave o idealnim plinovima.
Ja Konstanta R prisutna u jednadžbi stanja za plinove pV = nRT ima jednaku vrijednost za sve idealne plinove.
II. Jednake zapremine različitih idealnih plinova, pri istoj temperaturi i tlaku, sadrže isti broj molekula.
III. Prosječna kinetička energija molekula idealnog plina izravno je proporcionalna apsolutnoj temperaturi plina.
Koji su točni?
a) Samo ja
b) Samo II
c) Samo III
d) Samo I i II
e) I, II i III
Predložak:
Pogledajmo alternative:
Ja točno, stoga se naziva univerzalnom konstantom idealnih plinova.
II. ispravno. Prema Clapeyronovoj jednadžbi, ako dva idealna plina imaju jednak tlak, temperaturu i volumen, tada je broj čestica u tim plinovima jednak.
III. ispravno. Prema teoremu o energetskoj ekvivalentnosti, kinetička energija čestica u idealnom plinu proporcionalna je njegovoj temperaturi.
Stoga je ispravna alternativa slovo e.
Pitanje 3 - (UFJF) Ljudi poput Clapeyrona, Boylea, Mariottea, Gay-Lussaca, van der Wallsa, između ostalih, razvili su važne studije koje uključuju svojstva plinova. Ponašanje stvarnih plinova približava se idealnim plinovima u uvjetima niskog tlaka, kao i plinovima sadržanima u velikom volumenu i plinovima zadržanim na visokim temperaturama. Uzmimo u obzir da je u laboratorijskom pokusu spremnik zapremine V potpuno zatvoren i sadrži 1 mol idealnog plina pod pritiskom 4,0 atm je podvrgnut ekspanziji pri konstantnoj temperaturi koja je jednaka 127 º C i da se ponašanje ovog plina ponaša kao idealan plin, kao što je prikazano u grafički.
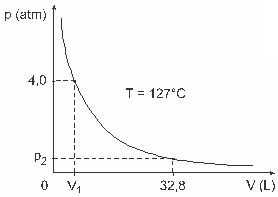
U ovom slučaju, kada plin zauzima zapreminu jednaku 32,8 L, tlak koji vrši na njega bit će:
(S obzirom: univerzalna konstanta savršenih plinova je R = 0,082 atm. L / mol. K.)
a) 0,32 atm
b) 0,40 atm
c) 1,0 atm
d) 2,0 atm
e) 2,6 atm
Razlučivost:
Slovo C.
Da bismo riješili vježbu, podatke moramo primijeniti na Clapeyronovu jednadžbu, ali prije toga moramo temperaturu, koja je u stupnjevima Celzija, transformirati u kelvin. Provjeri:

Napisao Rafael Hellerbock
Učitelj fizike
Izvor: Brazil škola - https://brasilescola.uol.com.br/fisica/a-equacao-clapeyron.htm

