definicija materija daje jednostavna i sveobuhvatna fraza: sve je ono što zauzima mjesto (isto što i volumen) u prostoru i ima težinu (umnožak mase i gravitacije). Neki primjeri materije: drvo, bakterije, virus, čovjek, zrak, voda, stol, vozilo itd.
Mogli bismo navesti tisuće primjera kao materija prilično je sveobuhvatan. Ali postoji li nešto što nije važno? Naravno, da, međutim, u ovom se slučaju naziva energijom, kao u sljedećim primjerima:
Svjetlo: naziva se svjetlosnom energijom;
Pritisak: naziva se energija pritiska;
Zvuk: naziva se zvučna energija;
Vatra: povezanost toplinske i svjetlosne energije;
Struja: nazvana električna energija;
Toplina: nazvana toplinska energija;
RTG: oblik elektromagnetske energije;
THE energije može se definirati kao snaga sposoban proizvesti akciju i pokret. Stoga je vrlo jednostavno razlikovati materiju od energije, jer jedna zauzima prostor i ima masu, a druga ne.
Važna zanimljivost oko materija jest da se to može nazvati na dva različita načina: tijelo i objekt.
Tijelo: to je dio materija. Primjeri: vunena pređa, slomljeno staklo, vjetar, deblo stabla;
Objekt: to je dio materija koja ima specifičnu upotrebu. Primjeri: košulja, komprimirani zrak, olovka, stolica.
Mapa uma: Materija
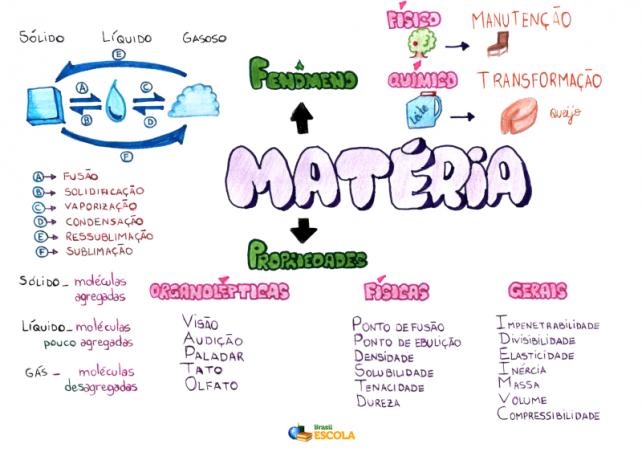
* Za preuzimanje mape uma u PDF-u, Kliknite ovdje!
Sastav materije
Općenito govoreći, svi materija tvori osnovna strukturna jedinica, nazvana atom, koja ima sljedeći sastav:
Jezgra: sastavljen od protona i neutrona;
protoni: pozitivno nabijene čestice;
neutronima: nenapunjene čestice;
Razine energije: regije u kojima se nalaze podrazine;
Podrazine energije: regije u kojima su orbitale;
Orbitale: regije u kojima će elektroni najvjerojatnije pronaći;
elektroni: negativno nabijene čestice.
Kada se dva ili više atoma kombiniraju, oni tvore molekule koje mogu nastati tvari kao i pojedinačni atomi.
fizička stanja materije
Vas fizička stanja najčešće u kojima možemo pronaći stvar su:
Čvrsto: stanje u kojem čestice (atomi ili molekule), koje tvore materiju, predstavljaju najvišu razinu organizacije;
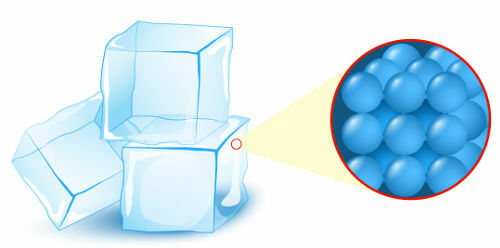
Prikaz organizacije čestica u čvrstom stanju
Tekućina: stanje u kojem čestice (atomi ili molekule), koje tvore materiju, predstavljaju nižu razinu organizacije;
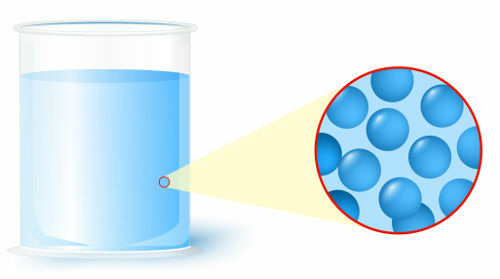
Prikaz organizacije čestica u tekućem stanju
Plinoviti: stanje u kojem čestice (atomi ili molekule), koje tvore materiju, nemaju organizaciju.
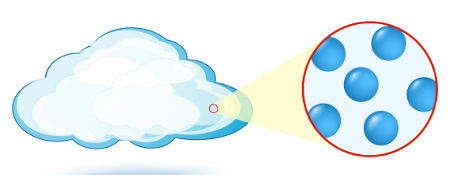
Prikaz organizacije čestica u plinovitom stanju
Opća svojstva tvari
bilo koje i sve materija, bez obzira na kemijski elementi koji je čine, moraju imati svojstva navedena u nastavku:
Elastičnost: svojstvo koje tvar ima u čvrstom stanju kada je podvrgnuta ekstremnoj elastičnoj sili, a da joj strukture nisu slomljene. Kad ta sila prestane, materija se vraća u svoj izvorni oblik;
Kompresibilnost: kada je dio materije u plinovitom stanju podvrgnut kompresiji, on zauzima manji volumen;

Materijal koji se komprimira u cilindar
Inercija: kada se materija kreće, ona nastoji ostati u pokretu. Ako miruje, tendencija je da ostane mirovati;
Djeljivost: tvar se može rastaviti na manje dijelove;
Neprobojnost: dva subjekta ne mogu istovremeno zauzimati isti prostor.
Ja, Diogo Lopes Dias
Izvor: Brazil škola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-materia.htm

