THE topljivost ili koeficijent topljivosti, to je fizikalno svojstvo materije koje se uvijek praktički određuje u laboratoriju. Povezan je s kapacitetom koji materijal, tzv otopljeni, predstavlja da ga drugi, otapalo.
Što se tiče topljivosti, otopljene tvari mogu se klasificirati na sljedeći način:
Topive: one koji se otapaju u otapalu. Natrijev klorid (otopljena tvar), na primjer, topljiv je u vodi (otapalu);
Slabo topiv: one koji imaju poteškoće s otapanjem u otapalu. To je slučaj s kalcijevim hidroksidom [Ca (OH)2] (otopljena tvar) u vodi;
Netopivi: oni se ne otapaju u otapalu. Na primjer, pijesak (otopljena tvar) je netopiv u vodi.
THE topljivost je vrlo povezan s pripremom rješenja (homogene smjese), jer je za dobivanje otopine bitno da se otopljena tvar otopi u otapalu.
Čimbenici koji utječu na topljivost
Čak i kada je otopljena tvar topljiva u otapalu, postoje neki čimbenici koji mogu utjecati na sposobnost otapanja otopljene tvari. Jesu li oni:
a) Odnos između količine otopljene tvari i otapala
Otapalo uvijek ima granicu otopljene tvari koju može otopiti. Ako povećamo količinu otapala zadržavajući količinu otopljene tvari, otapalo nastoji otopiti svu korištenu otopljenu tvar.
B) Temperatura
Temperatura je jedini fizikalni faktor koji može promijeniti topljivost otapala s obzirom na danu otopljenu tvar. Ova modifikacija ovisi o prirodi otopljene tvari, kao što ćemo vidjeti u nastavku:
endotermna otopljena tvar: je onaj koji uspijevamo otopiti veću masu, sve dok je otapalo na temperaturi višoj od sobne temperature. Što je otapalo vruće, topiva će se otopiti.
Primjer: Veću količinu mljevene kave moguće je otopiti kad je voda vruća.
Egzotermna otopljena tvar: je onaj koji uspijevamo otopiti veću masu, sve dok je otapalo na temperaturi nižoj od sobne temperature. Što je otapalo hladnije, topiva će se otopiti.
Primjer: Kad je soda hladna, moguće je otopiti veću količinu ugljičnog dioksida.
Načini određivanja topljivosti
Kako je topivost svojstvo utvrđeno eksperimentalnim načinom, topivost materijala je općenito već procijenjena u najrazličitijim otapalima. Tako možemo pristupiti topljivosti otopljene tvari u određenom otapalu na sljedeći način:
a) Analiza tablice
Učenik često može naići na topivost iz interpretacije tablice. Pogledajte sljedeći primjer:
Primjer: (UEPG - prilagođeno) Tablica u nastavku prikazuje topljivost Li soli2CO3 u 100 grama vode.
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)

Tablica prikazuje vrijednosti mase u gramima Li2CO3 koji se može otopiti u 100 grama vode, od 0 OC do 50 OÇ. Vidimo da što je voda vruća, to je manje Li2CO3 otapa. Stoga, Li2CO3 to je egzotermna otopljena tvar (više će se otapati ako je voda hladna).
b) Analiza grafa
Topljivost se može procijeniti tumačenjem grafa. Da biste to učinili, jednostavno odredite temperaturu, okrenite je na krivulju, a zatim krivulju okrenite prema osi y, što je masa otopljene otopljene tvari u gramima.
Primjer: (UFTM - prilagođeno) Grafikon prikazuje krivulju topljivosti AX soli2.
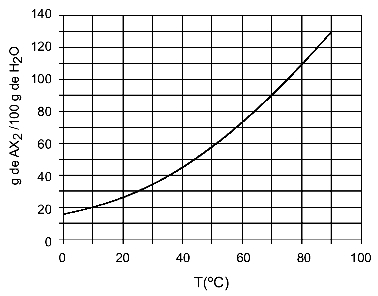
Grafikon kaže da je na y osi količina vode (otapala) 100 grama. Za otopljeni AX2, odredit ćemo količinu vode pri sljedećim temperaturama:
30OÇ: Kad uključimo temperaturu 30OC do krivulje, a zatim krivulja do osi y, imamo da pri ovoj temperaturi 100 grama vode može otopiti približno 35 grama otopljene AX2.
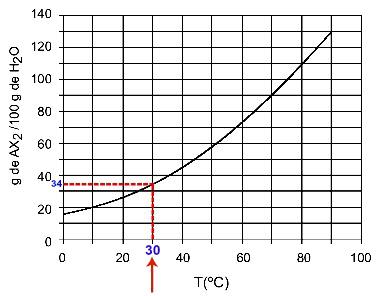
Određivanje topljivosti AX2 u 30OÇ
40OÇ: Kad uključimo temperaturu 40OC do krivulje, a zatim krivulja do osi y, imamo da pri ovoj temperaturi 100 grama vode može otopiti približno 45 grama otopljene AX2.
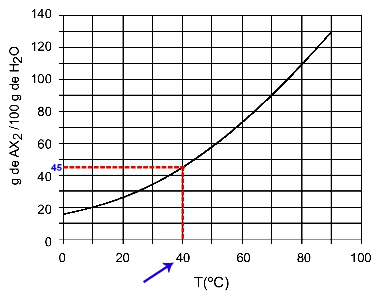
Određivanje topljivosti AX2 u 40OÇ
Kako je otopljena količina otopljene tvari veća sa svakim povećanjem temperature, imamo da je AX2 to je endotermna otopljena tvar.
c) tekstualna interpretacija
Pogledajte sljedeći primjer:
Primjer: (PUC-MG) Određene tvari mogu tvoriti homogene smjese s drugim tvarima. Tvar koja je u najvećoj količini naziva se otapalom, a ona koja je u najmanjoj količini otopljena tvar. Natrijev klorid (NaCl) tvori homogenu otopinu s vodom u kojoj je moguće otopiti na 20 ° C 36 g NaCl u 100 g vode.
U tekstu se navodi da ako imamo 100 grama vode (otapala), na temperaturi od 20 OC, moguće je otopiti do 36 grama NaCl.
Ja, Diogo Lopes Dias
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
DANI, Diogo Lopes. "Što je topivost?"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-solubilidade.htm. Pristupljeno 28. lipnja 2021.
