U izotermičkoj transformaciji, varijacija volumena i tlaka određenog plina, ali stalna temperatura; otuda i podrijetlo izotermnog imena (grčki: izo = jednak; termo = toplina).
Znanstvenici Boyle i Mariotte, izolirano, provodili su slične pokuse i dobiveni rezultat je bio: kako tlak raste, volumen plina opada.
Pomislite samo na primjer na klip šprice. Ako na ovaj klip izvršimo vanjski pritisak, odnosno ako povećamo tlak, smanjit će se količina zraka zauzeta u štrcaljki i obrnuto.
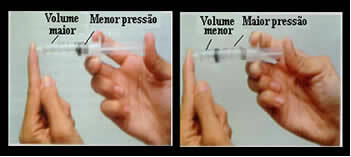
Volumen i tlak su obrnuto proporcionalni: na lijevoj ploči je tlak mali, a volumen koji zauzima zrak velik. S desne strane, kada se na klip štrcaljke izvrši veći pritisak, volumen se smanjuje.
Ovo nije izoliran slučaj, to je nešto što se ponavlja s uobičajenom pravilnošću za plinove. Stoga je ta činjenica navedena u obliku zakona, koji se može opisati na sljedeći način:
| Boyleov zakon ili Boyle-Mariotteov zakon: Pod konstantnom temperaturom, volumen koji zauzima fiksna masa plina obrnuto je proporcionalan njegovom tlaku. |
To znači da ako udvostručimo tlak plina, njegov volumen će se prepoloviti i tako dalje. Kad su dvije takve količine obrnuto proporcionalne, njihov je proizvod konstanta; stoga se matematički ovaj odnos može prikazati na sljedeći način:
| P.V = k |
Gdje je k = konstanta.
Dakle, ako u prvoj situaciji imamo vrijednost tlaka određenog plina kao P1, a njegov odgovarajući volumen kao V1, tada moramo:
| Str1. V1 = k |
Ako povećamo ovaj tlak na P2, njegov volumen također će se promijeniti u V2 i opet ćemo morati:
| Str2 . V2 = k |
Dakle, dolazimo do zaključka:
| Str1. V1 = P2. V2 |
Ta postojanost može se vidjeti na primjeru navedenom u donjoj tablici tlakova i volumena plina fiksne mase:
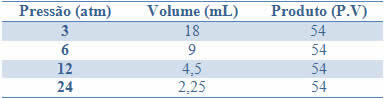
Grafikom ovih vrijednosti vidjet ćemo nastanak krivulje.
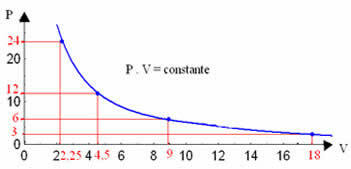
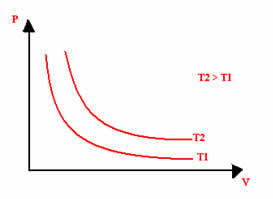
Grafički prikaz izotermne transformacije uvijek će biti hiperbola, bez obzira na vrijednosti tlaka i volumena i temperature na kojima je eksperiment izveden. Ova hiperbola se naziva izoterma; pa, kao što se može vidjeti na donjem grafikonu, različite temperature dovode do različitih izotermi.
Izvor: Brazil škola - https://brasilescola.uol.com.br/quimica/transformacao-isotermica-ou-lei-boyle.htm

