Kapacitet koji veze moraju privući električne naboje definiran je kao polaritet, koji poprima drugačiji karakter ovisno o vezi na kojoj je prisutan.
Najčešće veze koje uključuju organske spojeve događaju se između atoma ugljika ili između atoma ugljika i vodika: C ─ C i C ─ H (ugljikovodici). Ovu vrstu veze klasificiramo kao kovalentnu, prisutna je u svim vezama organskih spojeva koje tvore samo ugljik i vodik.
Kada u molekuli organskog spoja postoji još jedan kemijski element, osim ugljika i vodika, njegove molekule imat će određenu polarnost. Ovaj element nazivamo heteroatomom, a to mogu biti: dušik (N), kisik (O), između ostalog.
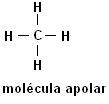
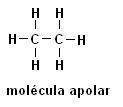
Metan (CH4) Etan (C2H6)
Imajte na umu da u obje strukture nema heteroatoma, u ovom su slučaju molekule klasificirane kao nepolarne.


Prisutnost kisika kao heteroatoma čini da molekule pokazuju polaritet. Prva molekula je spoj etanol (CH3CH2Oh), prisutnost hidroksil-OH daje ovom spoju polarni karakter, čak iako u svojoj strukturi sadrži nepolarni dio.
Napisala Líria Alves
Diplomirao kemiju
Brazilski školski tim
Vidi više! ravni izomer
Organska kemija - Kemija - Brazil škola
Izvor: Brazil škola - https://brasilescola.uol.com.br/quimica/moleculas-organicas-polares-apolares.htm

