THE Zakon brzine reakcije odnosi brzinu kemijske transformacije s koncentracijama reagensa u količini tvari (mol / L), što se može navesti na sljedeći način:

Na primjer, uzmite u obzir sljedeću generičku reakciju:
aA + bB → cC + dD
Recimo da povećamo koncentraciju reaktanata A i B, što će se dogoditi sa brzinom reakcije? Pa, kako će se količina čestica reaktanata povećavati u istom prostoru, bit će i učinkovitijih sudara između njih, što će rezultirati povećanjem brzine razvoja reakcije. Što znači da će vam povećati brzinu.
Stoga je brzina reakcije izravno proporcionalna koncentraciji reaktanata. Međutim, to ovisi i o temperaturi. Stoga imamo sljedeću matematičku jednadžbu koja predstavlja zakon brzine reakcije:

Na što:
v = brzina reakcije;
k = konstanta koja ovisi samo o vrijednosti temperature;
α i β = eksponenti određeni eksperimentalno.
Tek kad je reakcija elementarna, odnosno dogodi se u jednom koraku, eksponenti su točno jednaki koeficijentima uravnotežene kemijske jednadžbe: v = k. [THE]The. [B]B
. Međutim, u drugim se slučajevima mora eksperimentalno odrediti odgovarajuća jačina do koje mora biti povišena koncentracija svakog reagensa.Zakon brzine reakcija nosi mnoga imena, evo nekoliko: Zakon masovne akcije, Jednadžba brzine, Kinetički zakon reakcije i Guldberg-Waageov zakon.
Razmotrimo primjer kako primijeniti ovaj zakon:
Razmotrimo sljedeću elementarnu reakciju:
2 HCl (g) → H2 (g) + Kl2 (g)
a) Napišite jednadžbu brzine ove reakcije;
b) Kroz eksperimente, brzina reakcije razgradnje vodikovog klorida i koncentracija ovog reagensa, pri konstantnoj temperaturi od 25 ° C, zabilježeni su u donjoj tablici:
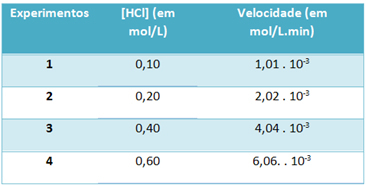
Na temelju toga odredite karakterističnu konstantu brzine ove reakcije pri spomenutoj temperaturi.
Rješenje:
The) v = k. [HCl]2
b) v = k. [HCl]2
k = __v___
[HCl]2
k = 1,01. 10-3 mol. L-1. min-1
0,01 mol. L-1
k = 1,01. 10-1 min-1
Da biste riješili slovo "b", možete upotrijebiti podatke bilo kojeg od pokusa da će dobivena vrijednost biti jednaka.
Ali što ako reakcija nije elementarna? Kako će biti moguće riješiti ovakva pitanja u neelementarnim reakcijama? Da biste saznali kako, pročitajte Zakon brzine za neelementarne reakcije.
Napisala Jennifer Fogaça
Diplomirao kemiju
Izvor: Brazil škola - https://brasilescola.uol.com.br/quimica/lei-velocidade-das-reacoes-quimicas.htm
