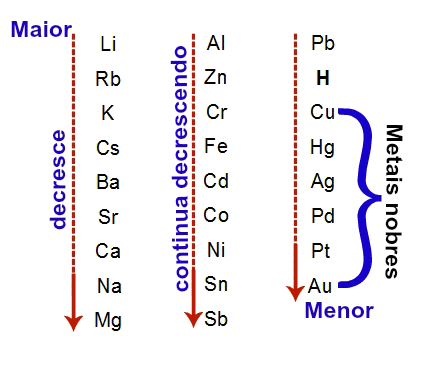
reakcije sa bazični oksidi su kemijske pojave u kojima se tvar ove klase oksida stavlja u isti spremnik kao a anorganska kiselina, a kiseli oksid ili jedan amfoterni oksid.
Vidi i:Reakcije s amfoternim oksidima
anorganska sol i voda su uobičajeni proizvodi u a reakcija s bazičnim oksidima. Da bismo saznali hoće li se proizvesti anorganska sol ili voda, moramo pogledati tvar koja prati osnovni oksid u reagensu. Pogledajte primjere u nastavku i shvatite kako se ovaj proces odvija.
Reakcije s bazičnim oksidima i anorganskim kiselinama
U reakcijama između bazičnih oksida i anorganskih kiselina nastaju anorganska sol i voda, jer osnovni oksidni kation (Y+) stupa u interakciju s anionom (X-) kiseline i hidronijev kation (H+) kiseline stupa u interakciju s anionom oksida:
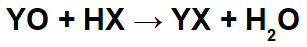
Primjer: Radijev oksid i bromovodična kiselina
U ovoj reakciji imamo radij oksid (RaO) i bromovodičnu kiselinu (Hbr) kao reaktante. Dakle, dolazi do sljedećih interakcija:
Radio kation (Ra+2) s bromidnim anionom (Br-1) tvoreći sol radij bromida (RaBr2).
Hidronijev kation (H+1) s oksidnim anionom (O-2) tvoreći vodu (H2O).
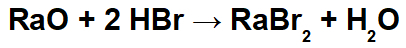
Vidi i:Reakcije s dvostrukim oksidima
Reakcije s bazičnim oksidima i kiselim oksidima
U tim reakcijama nastaje anorganska sol interakcijom između bazičnog oksidnog kationa (Y+) i rezultirajući kiseli anion (WOThe-) kemijske reakcije između kiselog oksida i vode.
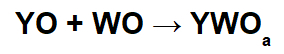
Primjer: Natrijev oksid i sumpor dioksid
U ovoj reakciji imamo natrijev oksid (Na2O) i sumpor dioksid (SO2). Važno je napomenuti da u početku, kada kiseli oksid interagira s vodom, dolazi do stvaranja sumporne kiseline (H2SAMO3):
Nemoj sada stati... Ima još toga nakon reklame ;)

Od stvaranja ove kiseline dolazi do interakcije između natrijevog kationa (Na+1) osnovnog oksida i sulfitnog aniona (SO3-2) kiseline, tvoreći sol natrijevog sulfita (Na2SAMO3):
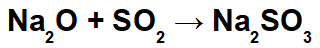
Reakcije s bazičnim oksidima i amfoternim oksidima
Amfoterni oksidi su tvari koje pokazuju dvostruko kemijsko ponašanje: u prisutnosti kisele tvari, ponaša se kao bazični oksid; u prisutnosti tvari bazične prirode, ponaša se kao kiseli oksid.
Dakle, kada je a bazični oksid reagira s amfoternim oksidom, to će se ponašati kao kiseli oksid, stvarajući anorgansku kiselinu u prisutnosti vode. Reakcijom između aniona anorganske kiseline i kationa bazičnog oksida nastat će produkt soli.
Primjer: Kalijev oksid i krom III oksid
U ovoj reakciji imamo kalijev oksid kao reaktante (K2O) i krom oksid (Cr2O3). Važno je napomenuti da, u početku, kada amfoterni oksid interagira s vodom, dolazi do stvaranja kromosomske kiseline (2HCrO2):

Od stvaranja ove kiseline dolazi do interakcije između kalijevog kationa (K+1) osnovnog oksida i kromitnog aniona (SO3-2) kiseline, tvoreći sol kalijevog kromita (2KCrO2):

Od mene Diogo Lopes Dias
Želite li referencirati ovaj tekst u školskom ili akademskom radu? Izgled:
DANI, Diogo Lopes. "Reakcije s bazičnim oksidima"; Brazilska škola. Dostupno u: https://brasilescola.uol.com.br/quimica/reacoes-com-oxidos-basicos.htm. Pristupljeno 27. srpnja 2021.
Nomenklatura soli, klasifikacija soli, naziv aniona, naziv kationa, željezni sulfat, željezni sulfat, nitrat srebra, kalijevog klorida, natrijevog klorida, kalcijevog klorida, srebrnog nitrata, bakrenog sulfata, karbonata kalcij.