Organski spojevi mogu biti predstavljeni na različite načine, kao što je ravna strukturna formula, pojednostavljena ili kondenzirana strukturna formula ili formula crtica. Međutim, najjednostavniji prikaz je putem molekularne formule.

Dakle, pogledajmo kako odrediti molekularnu formulu organskih spojeva na temelju drugih gore navedenih formula.
1. Kroz ravnu strukturnu formulu:ova formula pokazuje raspored ili raspored atoma unutar molekule. Na primjer, ispod je ravna strukturna formula jednog od ugljikovodika prisutnih u benzinu.

Imajte na umu da su u ovoj formuli prikazani svi atomi i sve postojeće veze između njih. Sada, da biste odredili molekularnu formulu ovog spoja, samo izbrojite broj atoma svakog elementa i stavite indeks na donju desnu stranu dotičnog elementa.
Važan aspekt koji treba istaknuti je da molekularnu formulu organskih spojeva uvijek započinjemo od elementa ugljika, jer je glavni sastojak ovih tvari. Pogledajte primjer:
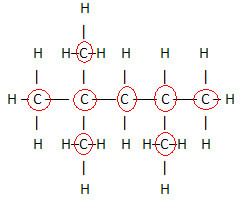
Budući da postoji 8 ugljika, molekularnu formulu počinjemo pisati ovako: Ç8
Da bismo dovršili ovu formulu, brojimo količinu vodika:
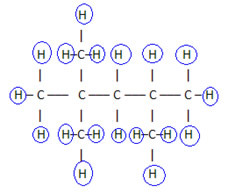
dakle, tvoj molekularna formula é Ç8H18.
2. Kroz pojednostavljenu ili sažetu strukturnu formulu: u ovoj vrsti formule količina vodika je skraćena. Na primjer, pogledajte istu formulu za molekulu koja se nalazi u benzinu, sada u kondenziranom obliku:
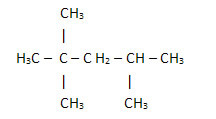
Na ovaj način još je lakše izbrojati količinu vodika, samo dodajte indekse (3 +3+ 3 +2 +1 +3 +3 = 18).
Ali sada pogledajmo kondenziranu strukturnu formulu linolne kiseline, koja postoji u povrću kao što su pamuk, soja, suncokret itd. a koji se koristi u bojama i lakovima:
H3C─CH2CH2CH2CH2CH═CH─CH2CH═CH─CH2CH2CH2CH2CH2CH2CH2─COOH
Računajući količinu ugljika, vodika i kisika, imamo sljedeće molekularna formula linolne kiseline: Ç18H32O2.
3. Kroz formulu poteza: ova formula dodatno pojednostavljuje kako predstaviti organske spojeve, jer izostavlja skupine C, CH, CH2 i CH3.
Primjer je linolna molekula, pogledajte kako izgleda:

Najprije izbrojimo količinu ugljika, sjetimo se da je u ovoj formuli svaka veza između ugljika predstavljena crticom. Dakle, vrhovi, kao i dvije točke pregiba, odgovaraju atomima ugljika.
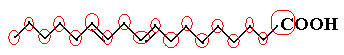
Dakle, imamo: Ç18
Sada, da izbrojimo količinu vodika, moramo se sjetiti da se veze između ugljika i vodika podrazumijevaju, budući da je poznato da ugljik čini četiri veze; dakle, količina veza koja nedostaje je količina vodika vezanog za taj element.
Pogledajte objašnjenja u nastavku:
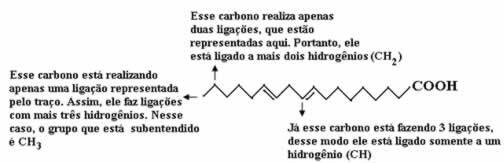
Dakle, količina vodika će biti: 32.

Količinu kisika prilično je jednostavno izbrojati, jer postoje samo dvije. Od molekularna formula é: Ç18H32O2.
Autora Jennifer Fogaça
Diplomirao kemiju
Izvor: Brazil škola - https://brasilescola.uol.com.br/quimica/formulas-moleculares-compostos-organicos.htm
