Elektronska distribucija odnosi se na to kako su elektroni raspoređeni u slojevima ili energetskim razinama koje okružuju jezgru atoma.
Prema Rutherford-Böhr atomskom modelu, atoma poznatih kemijskih elemenata ima najviše sedam elektronski slojevi, koji povećavaju energiju iznutra prema van jezgre (1 – 2 – 3 – 4 – 5 – 6 – 7). Ovih sedam slojeva možemo označiti i odgovarajućim slovima K – L – M – N – O – P – Q, pri čemu je K prvi, bliži jezgri i ima najnižu energiju. S druge strane, Q sloj je sedmi, najudaljeniji od jezgre i onaj s najvećom energijom.
Budući da svaki atom ima atomski broj (količina protona u jezgri) i različit broj elektrona, elektronski slojevi svakog atoma imaju različite energije koje drže elektrone s tom energijom odlučan.
Mapa uma: elektronička distribucija

* Da biste preuzeli mapu uma u PDF-u, Kliknite ovdje!
Zabilježite u nastavku neke atome i elektrone raspoređene u njihovim elektroničkim slojevima:

Atom vodika, helija, berilija i kisika
Imajte na umu da je raspodjela četiri atoma berilija: 2 – 2, a kisika 2 – 6. Samo kroz ove primjere moguće je vidjeti da elektronička distribucija slijedi redoslijed. Na primjer, ljuska K (1) može imati najviše dva elektrona.
U nastavku imamo tablicu koja određuje maksimalnu količinu elektrona koji se može distribuirati u svakom elektroničkom sloju:
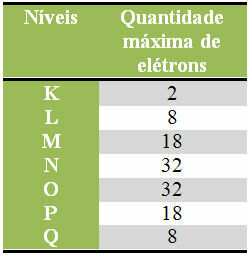
Maksimalni broj elektrona u elektroničkim razinama
Također treba imati na umu da posljednja ljuska koju treba napuniti, takozvana valentna ljuska, mora imati najviše osam elektrona. Dakle, ako ste rasporedili elektrone i vidjeli da posljednja ljuska ima količinu veću od 8, ali manju da bi 18, dakle, trebalo ostaviti samo 8 elektrona u toj ljusci i dodati ostatak u sljedeću ljusku plus vanjski.
Na primjer, razmotrite elektronsku distribuciju atoma kalcija. Gledajući periodni sustav, vidimo da ima atomski broj jednak 20, dok u osnovnom stanju postoji isti broj elektrona. Dakle, moramo rasporediti 20 elektrona u njihove elektronske ljuske. Pogledajte u nastavku:
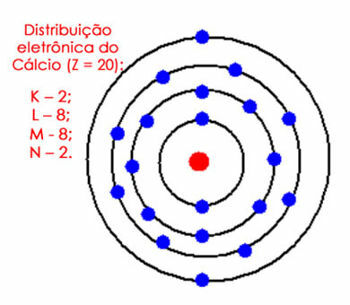
Elektronska raspodjela kalcija u atomu
Imajte na umu da M ljuska može zadržati do 18 elektrona, ali ako u nju stavimo preostale elektrone, imala bi 10 elektrona, što se ne može dogoditi u valentnoj ljusci. Dakle, stavljamo ostale elektrone (2) u sljedeću ljusku, a to je N.
Ali ako je količina elektrona u posljednjoj ljusci između 18 i 32, ostavljate 18 elektrona, a ostatak prenosite u vanjske ljuske. Pogledajte još jedan primjer:
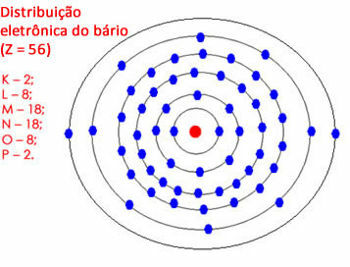
Elektronska raspodjela barija u atomu
Imajte na umu da "N" ljuska može sadržavati najviše 32 elektrona, ali ovdje bi imala 28. Tako ostavljamo 18 elektrona, a ostatak prenosimo sljedećoj ljusci. Ali "O" ljuska bi imala 10 elektrona, tako da smo ostavili 8 i podijelili ostala 2 preostala elektrona na "P" ljusku.
Međutim, postoji lakši način da se izvrši ova elektronička distribucija elektrona atoma. To je kroz Paulingov dijagram (otkad ga je stvorio znanstvenik Linus Carl Pauling (1901-1994)), također poznat kao dijagram elektroničke distribucije ili ipak, Dijagram razina energije. Ovaj dijagram izgleda ovako:
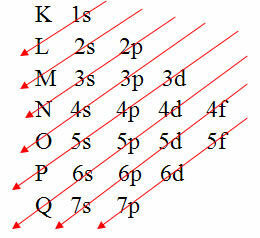
Grafički prikaz elektroničke distribucije dan je Paulingovim dijagramom
Da biste razumjeli kako su elektroničke distribucije elektrona i iona napravljene u ovom dijagramu, pročitajte tekstove u nastavku:
* raspodjela elektrona;
* elektronička distribucija iona.
* Autor slike Linusa Paulinga: Nobelprize.org
** Mapa uma od mene Diogo Lopes
Autora Jennifer Fogaça
Diplomirao kemiju
Izvor: Brazil škola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-distribuicao-eletronica.htm


