Kemijska izomerija pojava je koja se uočava kada dvije ili više organskih tvari imaju istu molekularnu formulu, ali različitu molekularnu strukturu i svojstva.
Kemijske tvari s tim karakteristikama nazivaju se izomeri.
Pojam je izveden iz grčkih riječi iso = jednak i puki = dijelova, odnosno jednakih dijelova.
Postoje različite vrste izomerije:
- ravni izomer: Spojevi se identificiraju ravnim strukturnim formulama. Dijeli se na lančanu izomeriju, funkcijsku izomeriju, izomeriju položaja, kompenzacijsku izomeriju i tautomerizam.
- svemirski izomer: Molekularna struktura spojeva ima različite prostorne strukture. Dijeli se na geometrijsku i optičku izomeriju.
ravni izomer
Na ravna izomerija ili ustavna izomerija, molekularna struktura organskih tvari je ravna.
Spojevi koji pokazuju ovu karakteristiku nazivaju se ravni izomeri.
izomer lanca
Lančana izomerija događa se kada atomi ugljika imaju različite lance i jednaku kemijsku funkciju.
Primjeri:
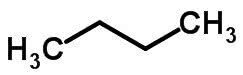
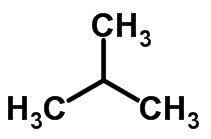
Izomerija funkcije
Izomerija funkcije nastaje kada dva ili više spojeva imaju različite kemijske funkcije i istu molekulsku formulu.
Primjeri: Ovaj je slučaj uobičajen između aldehida i ketona.
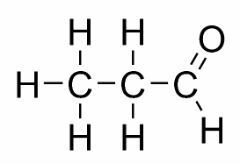
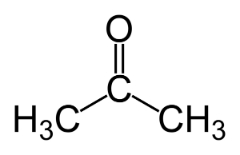
Izomer položaja
Izomerija položaja događa se kada se spojevi razlikuju različitim nezasićenim, razgranatim ili funkcijskim položajima u ugljikovom lancu. U ovom slučaju izomeri imaju istu kemijsku funkciju.
Primjeri:

offsetni izomer
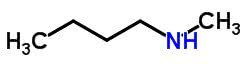
Kompenzacijska izomerija ili metamerizam javlja se u spojevima s istom kemijskom funkcijom koji se razlikuju po položaju heteroatoma.
Primjeri:

Tautomerija
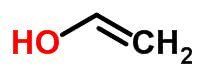
Tautomerija ili dinamička izomerija mogu se smatrati posebnim slučajem funkcijske izomerije. U tom se slučaju jedan izomer može promijeniti u drugi promjenom položaja elementa u lancu.
Primjeri:

svemirski izomer
THE svemirska izomerija, koja se naziva i stereoizomerija, događa se kada dva spoja imaju istu molekulsku formulu i različite strukturne formule.
U ovoj vrsti izomerije atomi se distribuiraju na isti način, ali zauzimaju različite položaje u prostoru.
geometrijski izomer
THE geometrijska izomerija ili se cis-trans javlja u nezasićenim otvorenim lancima i također u cikličkim spojevima. Da bi to učinili, ugljični ligandi moraju biti različiti.

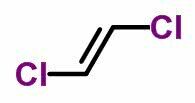
- Kada su isti ligandi na istoj strani, izomerna nomenklatura prima predznak cis.
- Kad su isti ligandi na suprotnim stranama, nomenklatura dobiva prefiks trans.
IUPAC (Međunarodna unija čiste i primijenjene kemije) preporučuje da se umjesto cis i trans, slova Z i E koriste kao prefiks.
To je zato što je Z prvo slovo njemačke riječi zusammen, što znači "zajedno". I to je prvo slovo njemačke riječi entegegen, što znači "suprotno".
optički izomer
THE optička izomerija pokazuju spojevi koji su optički aktivni. To se događa kada je tvar uzrokovana kutnim odstupanjem u ravnini polarizirane svjetlosti.
- Kad tvar savije optičku svjetlost udesno, ona se zove dešnjak.
- Kada tvar savije optičku svjetlost ulijevo, tvar se zove levorotarski.
Tvar također može postojati u dva optički aktivna oblika, dextogyra i levogyra. U ovom se slučaju zove enantiomer.
Da bi ugljikov spoj bio optički aktivan, on mora biti kiralan. To znači da se njihovi ligandi ne mogu preklapati, budući da su asimetrični.
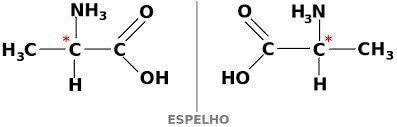
Zauzvrat, ako spoj ima oblik dekstrogire i levorotacije u jednakim dijelovima, oni se nazivaju racemične smjese. Optička aktivnost racemičnih smjesa je neaktivna.
Pročitajte i vi:
- Ugljik
- Organska kemija
- Molekularna formula
- strukturna formula
Vježbe
1. (Mackenzie 2012) Brojni stupac B, koji sadrži organske spojeve, povezujući ih sa stupcem A, prema vrsti izomerije koju svaka organska molekula predstavlja.
Stupac A
1. offsetni izomer
2. geometrijski izomer
3. izomer lanca
4. optički izomer
Stupac B
() ciklopropan
() etoksi-etan
() brom-kloro-fluoro-metan
() 1,2-dikloro-eten
Točan slijed brojeva u stupcu B, od vrha do dna, je
a) 2 - 1 - 4 - 3.
b) 3 - 1 - 4 - 2.
c) 1 - 2 - 3 - 4.
d) 3 - 4 - 1 - 2.
e) 4 - 1 - 3 - 2.
Alternativa b) 3 - 1 - 4 - 2.
2. (Uerj) Izomerija je pojava koju karakterizira činjenica da ista molekularna formula predstavlja različite strukture.
Uzimajući u obzir ravnu strukturnu izomeriju za molekularnu formulu C4H8, možemo identificirati izomere sljedećih vrsta:
a) lanac i položaj
b) lanac i funkcija
c) funkcija i kompenzacija
d) položaj i naknada
Alternativa a) niz i položaj
3. (OSEC) Propanon i izopropenol predstavljaju primjer izomerije:
a) od metamerije
b) funkcije
c) tautomerije
d) cis-tran
e) lanac
Alternativa c) tautomerije
Vidi i ti: Vježbe na ravnoj izomeriji

