Periodni sustav važan je alat za proučavanje koji prikuplja podatke o svim poznatim kemijskim elementima.
Provjerite svoje znanje pomoću ovog popisa 17 pitanja s različitim pristupima temi i riješite svoje sumnje rezolucijama komentiranim nakon povratnih informacija.
Da biste lakše razumjeli pitanja, upotrijebite periodni sustav elemenata dovršen i ažuriran.
Organizacija periodnog sustava
Pitanje 1
(UFU) Početkom 19. stoljeća, otkrićem i izolacijom nekoliko kemijskih elemenata, postalo je potrebno racionalno ih klasificirati kako bi se provodile sustavne studije. Mnogi su doprinosi dodani do trenutne periodične klasifikacije kemijskih elemenata. U vezi s trenutnom periodičnom klasifikacijom, odgovorite:
a) Kako su elementi redoslijedno navedeni u periodnom sustavu?
Periodni sustav organiziran je u nizove kemijskih elemenata u rastućem redoslijedu atomski broj. Taj broj odgovara broju protona u jezgri atoma.
Ovu metodu organizacije predložio je Henry Moseley kada je rekonfigurirao tablicu koju je predložio Dmitri Mendeleiev.
Element se u tablici može nalaziti prema obitelji i razdoblju u kojem je umetnut. Ova se distribucija odvija na sljedeći način:
| grupe ili obitelji | 18 vertikalnih sekvenci |
| Skupine elemenata koji imaju slične karakteristike. |
| Razdoblja | 7 vodoravnih sekvenci |
| Broj elektroničkih slojeva koje element ima. |
b) Koje se skupine u periodnom sustavu mogu naći: halogen, alkalijski metal, zemnoalkalni metal, halkogen i plemeniti plin?
Razvrstavanje elemenata u skupine vrši se prema svojstvima. Elementi koji su u istoj skupini imaju slična svojstva i za dane klasifikacije moramo:
| Klasifikacija | Skupina | Obitelj | Elementi |
| halogen | 17 | 7A | F, Cl, Br, I, At i Ts |
| alkalni metal | 1 | 1A | Li, Na, K, Rb, Cs i Fr |
| zemnoalkalijski metal | 2 | 2A | Budi, Mg, Ca, Sr, Ba i Ra |
| halkogen | 16 | 6A | O, S, Se, Te, Po i Lv |
| plemeniti plin | 18 | 8A | On, Ne, Ar, Kr, Xe, Rn i Og |
pitanje 2
(PUC-SP) Riješite problem na temelju analize izjava u nastavku.
I - Trenutni suvremeni periodni sustav raspoređen je u rastućem redoslijedu atomske mase.
II - Svi elementi koji imaju 1 elektron i 2 elektrona u valentnoj ljusci su, alkalni metali i zemnoalkalijski metali, pod uvjetom da je glavni kvantni broj ovog sloja (n 1).
III - U istom razdoblju elementi imaju isti broj razina (slojeva).
IV - U istoj skupini (obitelj) elementi imaju jednak broj razina (slojeva).
Zaključeno je da su, s obzirom na trenutni periodni sustav kemijskih elemenata, točni:
a) I i IV (samo).
b) I i II (samo).
c) II i III (samo).
d) II i IV (samo).
e) III i IV (samo).
Ispravna alternativa: c) II i III (samo).
Analizirajući svaku alternativu moramo:
JA - POGREŠNO. Elementi su poredani uzlaznim redoslijedom atomskog broja.
II - TOČNO. Elektroni u valentnoj ljusci definiraju skupinu u kojoj se nalazi element.
| alkalni metali | 1 elektron u valentnoj ljusci |
| 3čitati | 2-1 |
| 11Na | 2-8-1 |
| 19K | 2-8-8-1 |
| 37Rb | 2-8-18-8-1 |
| 55Cs | 2-8-18-18-8-1 |
| 87Fr | 2-8-18-32-18-8-1 |
| zemnoalkalijski metali | 2 elektrona u valentnoj ljusci |
| 4biti | 2-2 |
| 12mg | 2-8-2 |
| 20Ovdje | 2-8-8-2 |
| 38Gosp | 2-8-18-8-2 |
| 56Ba | 2-8-18-18-8-2 |
| 88Žaba | 2-8-18-32-18-8-2 |
Glavni kvantni broj odgovara ljusci u kojoj se nalazi elektron, a razlikuje se od 1 jer elektroničkom distribucijom primjećujemo da je mjesto elektrona iz druge ljuske odn n = 2.
III - TOČNO. Lokacija elementa u određenom razdoblju posljedica je broja slojeva prilikom elektroničke distribucije.
| Razdoblja | 7 vodoravnih sekvenci |
| 1. razdoblje | 1 sloj: K |
| 2. razdoblje | 2 sloja: K, L |
| 3. razdoblje | 3 sloja: K, L, M |
| 4. razdoblje | 4 sloja: K, L, M, N |
| 5. razdoblje | 5 slojeva: K, L, M, N, O |
| 6. razdoblje | 6 slojeva: K, L, M, N, O, P |
| 7. razdoblje | 7 slojeva: K, L, M, N, O, P, Q |
Primjer: kemijski element smješten u drugom razdoblju.
IV - POGREŠNO. Elementi koji pripadaju istoj skupini imaju slična svojstva, a to je zbog činjenice da imaju isti broj elektrona u valentnoj ljusci.
Primjer:
| Berilijum | Magnezij |
|
2 elektrona u valentni sloj. |
2 elektrona u valentni sloj. |
Stoga su berilij i magnezij dio skupine 2 Periodnog sustava.
pitanje 3
(Unitins) U vezi s modernom periodičnom klasifikacijom elemenata, identificirajte istinitu tvrdnju:
a) u obitelji, elementi uglavnom imaju jednak broj elektrona u posljednjoj ljusci.
b) na periodnom sustavu kemijski su elementi smješteni u padajućem redoslijedu atomskih masa.
c) u obitelji elementi imaju vrlo različita kemijska svojstva.
d) u jednom razdoblju elementi imaju slična kemijska svojstva.
e) svi reprezentativni elementi pripadaju skupini B periodnog sustava.
Ispravna alternativa: a) u obitelji elementi uglavnom imaju jednak broj elektrona u posljednjoj ljusci.
a) TOČNO. Kemijski elementi iste obitelji imaju jednak broj elektrona u posljednjoj ljusci, što ih čini sličnim karakteristikama.
b) POGREŠNO. Atomske mase se povećavaju kako se povećava atomski broj elementa.
c) POGREŠNO. Kemijska svojstva elemenata su slična, pa su grupirani u istu obitelj.
d) POGREŠNO. Elementi imaju svoje elektrone raspoređene u istom broju ljuski.
e) POGREŠNO. Reprezentativni elementi pripadaju skupini A, koja odgovara obiteljima: 1A, 2A, 3A, 4A, 5A, 6A, 7A i 8A. Elementi koji pripadaju skupini B prijelazni su elementi.
pitanje 4
(Vunesp) S obzirom na svojstva kemijskih elemenata i periodnog sustava, netočno je tvrditi:
a) metal je tvar koja provodi električnu struju, je duktilna i podatna.
b) nemetal je tvar koja ne provodi električnu struju, nije duktilna niti podatna.
c) polumetal ima fizički izgled metala, ali kemijsko ponašanje slično ponašanju nemetala.
d) većina kemijskih elemenata sastoji se od nemetala.
e) plemeniti plinovi su jednoatomni.
Pogrešna alternativa: d) većina kemijskih elemenata su nemetali.
Obratite pažnju na klasifikaciju kemijskih elemenata na periodnom sustavu na metale, nemetale i polumetale.

Kao što vidimo, većina elemenata su metali.
a) TOČNO. Metali provode električnu energiju zbog oblaka elektrona koje formiraju slobodni elektroni, a koji su karakteristični za njihovu strukturu. Oni su duktilni jer se mogu pretvoriti u žice ili listove, ovisno o regiji u kojoj se vrši pritisak. Oni su također podatni jer se s ovom vrstom materijala mogu proizvesti vrlo tanki limovi.
b) TOČNO. Nemetali imaju suprotne karakteristike metala. Umjesto vodiča, oni su dobri toplinski izolatori i, budući da su lomljivi, nisu oblikovani u žice ili listove jer nemaju dobru plastičnost i podatnost.
c) TOČNO. Semimetali imaju osobine srednje vrijednosti od metala i nemetala. Budući da su poluvodiči električne energije, oni imaju metalni sjaj, ali su lomljivi poput nemetala.
d) POGREŠNO. Većina elemenata klasificirana je kao metali. Klase metala prisutne u periodnom sustavu su: alkalne, zemnoalkalne, prijelazne unutarnje i vanjske.
e) TOČNO. Plemeniti plinovi su monoatomni, pa ih predstavljaju samo njihovi inicijali.
Primjer:
| plemeniti plin | halkogen |
| Helij (He) | Kisik (O2) |
| monoatomski: nastao atomom | dvoatomni: nastali od dva atoma |
Zbog stabilnosti plemenitih plinova, elementi ove obitelji imaju nisku reaktivnost i poznati su i kao inertni.
5. pitanje
O organizaciji trenutnog Periodnog sustava, odgovorite:
a) Što su stupci?
b) Koje su crte?
c) Koja se metoda koristi za organiziranje kemijskih elemenata?
Odgovori:
a) stupci su skupine Periodnog sustava, prije nazivane obiteljima, koje okupljaju kemijske elemente sličnih svojstava.
b) Linije su razdoblja Periodnog sustava i označavaju broj elektroničkih slojeva atoma u osnovnom stanju.
c) Kemijski elementi u trenutnom Periodnom sustavu poredani su uzlaznim redoslijedom atomskog broja, što ukazuje na broj protona u jezgri atoma.
Obitelji periodnog sustava
Pitanje 1
(CESGRANRIO) Stvarajući asocijaciju između stupaca u nastavku, koji odgovaraju obiteljima elemenata prema periodnom sustavu, numerički slijed bit će:
| 1. plemeniti plinovi | • Skupina 1A |
| 2. alkalni metali | • Skupina 2A |
| 3. zemnoalkalijski metali | • Skupina 6A |
| 4. Halkogeni | • Skupina 7A |
| 5. Halogeni | • Grupa 0 |
a) 1, 2, 3, 4, 5.
b) 2, 3, 4, 5, 1.
c) 3, 2, 5, 4, 1.
d) 3, 2, 4, 5, 1.
e) 5, 2, 4, 3, 1.
Ispravna alternativa: b) 2, 3, 4, 5, 1.
| skupine | elektronička konfiguracija |
| • Skupina 1A: 2. alkalni metali | nas1 (s n |
| • Skupina 2A: 3. zemnoalkalijski metali | nas2 (s n |
| • Skupina 6A: 4. Halkogeni | nas2np4 |
| • Skupina 7A: 5. Halogeni | nas2np5 |
| • Grupa 0: 1. plemeniti plinovi | 1s2 (On) ili mi2np6 (ako je n> 1) |
pitanje 2
(UECE) Kemijski element sa Z = 54 ima u svom valentnom sloju konfiguraciju 5s2 5p6. Elementi sa Z = 52 i sa Z = 56 pripadaju obiteljima:
a) halkogeni i zemnoalkalna zemlja
b) halogeni i lužine
c) halogeni i zemnoalkalna zemlja
d) halkogeni i lužine
Ispravna alternativa: a) halkogeni i zemnoalkalne zemlje.
S obzirom na atomske brojeve, izvršili smo elektroničku distribuciju i pronašli sljedeće rezultate:
| 54X i | 52Vas | 56Ba |
|
8 elektrona u valentni sloj |
6 elektrona u valentni sloj |
2 elektrona u valentni sloj |
| Plemeniti plinovi: 8A obitelj | Halkogeni: 6A obitelj | Alkalna zemlja: obitelj 2A |
pitanje 3
(F. Ibero-Americana-SP) Skupina periodnog sustava koju karakterizira prevladavanje umjetnih elemenata je sljedeća:
a) lantanidi
b) plemeniti plinovi
c) prijelazni metali
d) zemnoalkalijski metali
e) aktinidi
Ispravna alternativa: e) aktinidi.
Umjetni elementi su oni koji u prirodi ne postoje i koji su sintetizirani u laboratoriju nuklearnim reakcijama.
Oni se nazivaju i transuranskim elementima, jer ti radioaktivni elementi imaju atomski broj veći od 92, što odgovara uranu.
Općenito, ti su elementi kratkotrajni i traju do djelića sekunde.
Prema tim informacijama moramo:
Elementi koji se nalaze u prirodi su: lantanidi, plemeniti plinovi, prijelazni metali i zemnoalkalijski metali. Izuzev tehnecija i prometa, koji su umjetni.
Prevladavaju umjetni elementi aktinidi, klasificirani kao unutarnji prijelazni metali i umetnuti u periodni sustav ispod lantanida. Od te serije prirodni su samo aktinij, torij, protaktinij i uran.
pitanje 4
(U. Katolička crkva Salvador-BA) Vrsta X2- s 8 elektrona u najudaljenijoj ljusci (valentna ljuska) može biti iz elementa X, koji u Periodnom sustavu pripada skupini:
a) 7A
b) 6A
c) 2A
d) 1A
e) 8A
Ispravna alternativa: b) 6A.
Prema pravilu okteta, da bi element stekao stabilnost, on pretpostavlja elektroničku konfiguraciju plemenitog plina koji ima 8 elektrona u valentnoj ljusci.
Naboj 2- na vrsti X2- označava da je element dobio 2 elektrona.
Elektronska konfiguracija vrste koja ima 8 elektrona u najudaljenijoj ljusci je ns2np6.
Nakon gubitka dva elektrona, element se vraća u svoje osnovno stanje s ns elektronskom konfiguracijom2np4.
6 elektrona u valentnoj ljusci karakteristično je za halkogene, elemente obitelji 6A.
Na primjer:
| Element: kisik | elektronička konfiguracija |
| 8O | 1s22s22p4 |
| vrsta O2- | 1s22s22p6 |
Nauči više o Obitelji periodnog sustava.
Kemijski elementi
Pitanje 1
(CESGRANRIO) S obzirom na elemente atomskih brojeva 3, 9, 11, 12, 20, 37, 38, 47, 55, 56 i 75, opcija koja sadrži samo alkalne metale je:
a) 3, 11, 37 i 55
b) 3, 9, 37 i 55
c) 9, 11, 38 i 55
d) 12, 20, 38 i 56
e) 12, 37, 47 i 75
Ispravna alternativa: a) 3, 11, 37 i 55
Alkalni metali odgovaraju kemijskim elementima koji završavaju elektroničku raspodjelu elektronom u podrazini.
Izrađujući elektroničku raspodjelu zadanih atomskih brojeva, imamo sljedeće alkalne metale:
| Z = 3 | Z = 11 | Z = 37 | Z = 55 |
| Litij | Natrij | Rubidij | Cezij |
Ostali atomski brojevi odgovaraju elementima sljedećih skupina:
Zemnoalkalijski metali: prekinuti elektroničku distribuciju na podrazini s2.
| Z = 12 | Z = 38 | Z = 56 |
| Magnezij | Stroncij | Barij |
Prijelazni metali: prekinuti elektroničku distribuciju na podrazini d.
| Z = 30 | Z = 47 | Z = 75 |
| Cinkov | Srebro | Renij |
Halogeni: prekinuti elektroničku distribuciju na podrazini str5.
| Z = 9 |
pitanje 2
(Unirio) „Umjetno srce smješteno u Eloi počelo se razvijati prije četiri godine u Sjedinjenim Državama, a već ga koristi oko 500 ljudi. Set, nazvan Srčani drug, sastoji se od tri glavna dijela. Najvažnija je okrugla vreća od četiri kilograma, promjera 12 centimetara i debljine 3 centimetra, izrađena od titana - srebrno-bijelog metala, lagana i čvrsta. ” Časopis Veja, srpanj 1999.
Među donjim metalima, onaj koji u posljednjem sloju ima broj elektrona jednak titanu je:
a) C
b) U
c) Ga
d) Mg
e) Xe
Točna alternativa: d) Mg.
| Titan | elektronička konfiguracija | Raspodjela slojeva |
| 22Vas | 1s2 2s2 2p6 3s2 3p6 4s2 3d2 | 2, 8, 10, 2 |
Iz elektroničke raspodjele titana vidimo da ovaj element ima 2 elektrona u posljednjoj ljusci.
| Element | elektronička konfiguracija | Raspodjela slojeva |
| 6Ç | 1s2 2s2 2p2 | 2, 4 |
| 11Na | 1s2 2s2 2p6 3s1 | 2, 8, 1 |
| 31Ga | 1s2 2s2 2p6 3s2 3p6 4s2 3d104p1 | 2, 8, 18, 3 |
| 12mg | 1s2 2s2 2p6 3s2 | 2, 8, 2 |
| 54X i | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 | 2, 8, 18, 18, 8 |
Element koji također ima 2 elektrona u posljednjoj ljusci je magnezij.
pitanje 3
(UFPA) Razmotrimo određeni kemijski element čiji je najenergičniji podrazina 5s2. Njegov atomski broj i grupa u kojoj se nalazi na Periodnom sustavu su:
a) 20; 1A
b) 20; 2A
c) 38; 2A
d) 38; 1A
e) 39; 2A
Ispravna alternativa: c) 38; 2A
Elektroničkom distribucijom otkrili smo da:
- Kemijski element nalazi se u obitelji 2A, jer ima najenergičniji podrazina s2
- Ima atomski broj 38, što odgovara ukupnom broju distribuiranih elektrona.
- Smješteno je u petom razdoblju, jer je elektronička distribucija izvršena do petog sloja.
Provjeravajući ove podatke u Periodnom sustavu, možemo potvrditi da je riječ o elementu stroncij.
pitanje 4
(UFC) X atom ima jedan proton više od y atoma. Na temelju tih podataka utvrdite točnu tvrdnju.
a) Ako je y zemnoalkalna zemlja, x je alkalijski metal.
b) Ako je y plemeniti plin, x je halogen.
c) Ako je y prijelazni metal, x je plemeniti plin.
d) Ako je y plemeniti plin, x je alkalni metal.
e) x se nalazi u istom razdoblju prije atoma y u periodnom sustavu.
Točna alternativa: d) Ako je y plemeniti plin, x je alkalni metal.
Periodni sustav raspoređen je uzlaznim redoslijedom atomskog broja.
Ako Y ima atomski broj z, a X ima jedan proton više od sebe, to znači da su ova dva elementa u istom razdoblju, a X slijedi Y.
Primjer:
| Element | naknadni element |
| zY | z + 1x |
| 11Na | 12mg |
Dva su elementa u 3. razdoblju, a magnezij ima jedan proton više od natrija.
Prema ovom obrazloženju moramo:
a) POGREŠNO. Alkalni metal dolazi prije zemnoalkalijskog metala na periodnom sustavu. Točna bi izjava bila: Ako je y alkalni metal, x je zemnoalkalna zemlja.
b) POGREŠNO. Halogen dolazi ispred plemenitog plina na periodnom sustavu. Točna bi izjava bila: Ako je y halogen, x je plemeniti plin.
c) POGREŠNO. Prijelazni metali i plemeniti plinovi odvojeni su drugim kemijskim elementima i stoga nisu sekvencijalni.
d) TOČNO. Plemeniti plinovi su zadnja skupina na periodnom sustavu, a alkalni metali prva, pa su sekvencijalni.
Primjer:
| plemeniti plin | alkalni metal |
| zY | z + 1x |
| 2on | 3čitati |
Litij, alkalni metal, ima jedan proton više od helija, što je plemeniti plin.
e) POGREŠNO. X je u istom razdoblju kao Y, ali nakon njega, ne ranije kao alternativna stanja.
5. pitanje
Iz atomskog broja kemijskog elementa moguće je znati:
a) broj neutrona u jezgri
b) broj elektrona u elektrosferi
c) masa jezgre
Odgovor: b) broj elektrona u elektrosferi
Atom u osnovnom stanju električki je neutralan. Dakle, znajući atomski broj, koji odgovara broju protona (pozitivno nabijene čestice), znamo broj elektrona (negativno nabijene čestice) u elektrosferi.
Na primjer, željezo ima atomski broj 26, tako da u osnovnom stanju ima 26 elektrona oko jezgre.
Nauči više o kemijski elementi to je atomski broj.
Periodična i aperiodična svojstva
Pitanje 1
(UFSM) Procijenite jesu li izjave povezane s periodičkim svojstvima elemenata istinite (T) ili netačne (F).
() Ovisi o atomskim masama elemenata.
() Ponavljaju se u više ili manje pravilnim intervalima u odnosu na porast atomskih brojeva.
() Su slični u istoj skupini elemenata.
() Su slični u istom razdoblju elemenata.
() U istoj skupini numeričke vrijednosti periodičkih svojstava uvijek se povećavaju kada dođe do povećanja atomskog broja elemenata.
Ispravan slijed je:
a) V - Ž - V - Ž - Ž
b) V - Ž - Ž - V - V
c) Ž - V - V - Ž - Ž
d) Ž - V - Ž - V - V
e) V - Ž - Ž - V - Ž
Ispravna alternativa: c) F - V - V - F - F
(NETOČNO) Ovisi o atomskim masama elemenata.
Prema Moseleyevu zakonu periodičnosti, mnoga fizička i kemijska svojstva kemijskih elemenata razlikuju se o atomskom broju.
(PRAVI) Ponavljaju se u više ili manje pravilnim razmacima u odnosu na porast atomskih brojeva.
Svojstva poput atomskog radijusa, atomskog volumena, gustoće, tališta i vrenja primjeri su svojstava koja se redovito ponavljaju u periodnom sustavu.
(PRAVI) Jesu li slični u istoj skupini elemenata.
Grupe periodnog sustava raspoređene su s elementima koji imaju slična svojstva.
(NETOČNO) Slični su u istom razdoblju elemenata.
Svojstva su slična u obiteljima, a ne u razdobljima. U razdobljima se elementi raspoređuju prema broju elektroničkih slojeva.
(NETOČNO) U istoj skupini numeričke vrijednosti periodičkih svojstava uvijek se povećavaju kada dođe do povećanja atomskog broja elemenata.
Svojstva se mogu povećavati ili smanjivati ovisno o atomskom broju. Primjer za to je elektronegativnost, koja se smanjuje kako se atomski broj povećava u određenoj skupini.
Pročitajte i vi: Periodična svojstva
pitanje 2
(FAESP) Aperiodična svojstva elemenata su:
a) gustoća, atomski volumen i atomska masa.
b) talište, elektronegativnost i specifična toplina.
c) atomski volumen, atomska masa i talište.
d) atomska masa, specifična toplina i točka topljenja.
e) atomska masa i specifična toplina.
Ispravna alternativa: e) atomska masa i specifična toplina.
Aperiodična svojstva ponavljaju se u redovitim razmacima.
Atomska masa je mjera mase atoma u jedinicama atomske mase, koja odgovara mase ugljika-12.
Specifična toplina određuje količinu topline koja je potrebna za povećanje temperature od 1 g elementa za 1 ° C.
Ova dva svojstva nisu povezana s položajem elementa na periodnom sustavu.
Ostala svojstva klasificirana su kao periodična jer se povećavaju ili smanjuju s atomskim brojem. Jesu li oni:
- Gustoća: predstavlja količnik između mase i volumena elementa.
- Atomski volumen: predstavlja volumen skupa atoma i utječe na udaljenost između njih.
- Točka topljenja: temperatura pri kojoj se događa prijelaz iz krute u tekućinu.
- Elektronegativnost: sposobnost atoma da privuče sebi elektronički par koji dijeli u kovalentnoj vezi.
Pročitajte i vi: elektronegativnost i Elektronski afinitet
pitanje 3
(PUC-PR) Koji su točni među sljedećim dijagramima koji se odnose na periodni sustav?
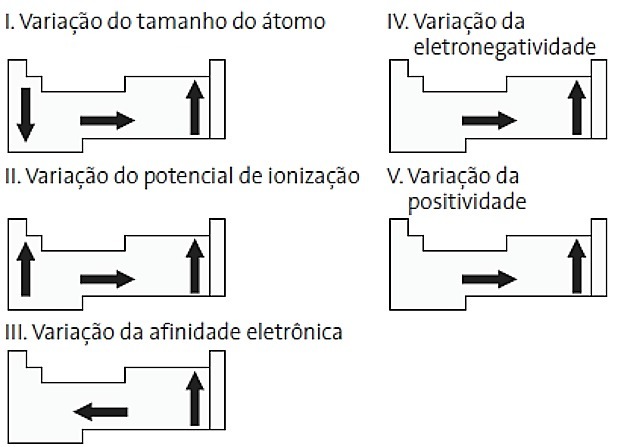
a) II i V
b) II i III
c) I i V
d) II i IV
e) III i IV
Ispravna alternativa: d) II i IV.
Ja POGREŠNO. Varijacija veličine atoma mjeri se prosječnom udaljenostom od jezgre do najudaljenijeg elektrona. Najveći atomi nalaze se na dnu tablice, pa se povećanje događa prema atomskom broju i točan prikaz je:
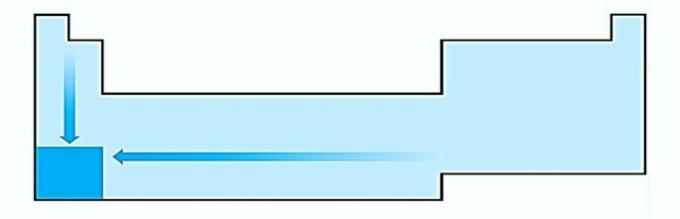
II. TOČNO Energija potrebna za kidanje elektrona s izoliranog atoma u plinovitom stanju naziva se ionizacijski potencijal. Povećava se kao što je prikazano na dijagramu izjava.
III. POGREŠNO. Elektronički afinitet izražava energiju koja se oslobađa kada neutralni atom u plinovitom stanju primi elektron, što je vrlo važno svojstvo nemetala. Najveći elektronički afiniteti uočeni su u halogena i kisika.
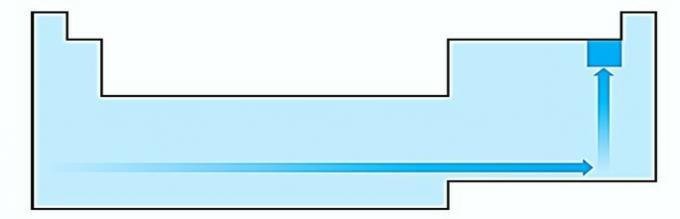
IV. TOČNO Elektronegativnost je povezana s ionizacijskim potencijalom i afinitetom elektrona. Kao takvi, halogeni su najelektronegativniji elementi periodnog sustava.
V. POGREŠNO. Elektropozitivnost se javlja u suprotnom smjeru od elektronegativnosti. Predstavlja sposobnost atoma da se odriče elektrona.
Stoga alkalni metali imaju najveću elektropozitivnost.
Nastavite provjeravati svoje znanje popisima:
- Vježbe na kemijskim vezama
- Vježbe o elektroničkoj distribuciji
- Vježbe na atomskim modelima
- Vježbe iz termokemije