Sublimacija je promjena iz čvrstog stanja u plinovito i obratno, bez prolaska kroz tekuće stanje.
Da bi tvar prošla postupak sublimacije, mora biti podvrgnuta određenim vrijednostima temperature i tlaka.
Naftalin i CO2 krutina (suhi led) primjeri su tvari koje podliježu sublimaciji u uvjetima okoline.

Dijagram faza
Fizičko stanje tvari možemo otkriti poznavanjem vrijednosti temperature i tlaka kojem je izložena.
Za to koristimo dijagrame izgrađene za svaku tvar na temelju eksperimentalnih vrijednosti.
Nazvano "Dijagram faza", podijeljen je u tri regije koja predstavljaju kruto, tekuće i plinovito stanje. Linije koje ograničavaju ta područja signaliziraju točke na kojima tvar mijenja fazu.
Trostruka točka na dijagramu označava temperaturu i tlak na kojima tvar može koegzistirati u tri faze. Ispod ove točke nalazi se krivulja sublimacije.
Točke na ovoj krivulji određuju vrijednosti tlaka i temperature pri kojima će doći do sublimacije.
Kad se krutina podvrgne pritisku manjem od trostruke točke, ako se zagrije, ona će preći izravno u plinovito stanje.
Promjena iz izravnog čvrstog stanja u plinovito može se dogoditi i smanjenjem tlaka kada je njegova temperatura niža od temperature trostruke točke.
Saznajte više na: Promjene fizikalnog stanja.
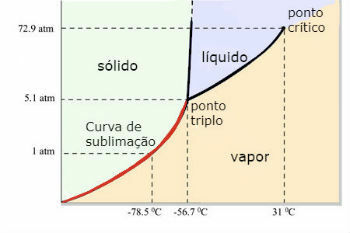
Dijagram faze ugljičnog dioksida (CO)2 )
Trostruka točka CO2 nastaje kad je tlak 5 atm. Ova činjenica opravdava da je uobičajeno vidjeti pojavu sublimacije u suhom ledu, jer je ambijentalni tlak 1 atmosfera.
Iz tog se razloga tekući ugljični dioksid ne dobiva u okolnim uvjetima. U tim uvjetima je ili u krutom ili u parnom stanju.
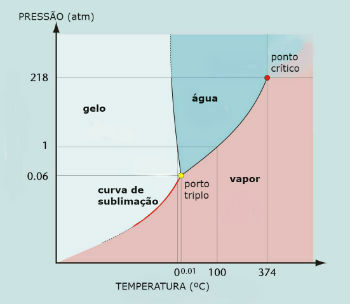
Dijagram vodene faze (H2O)
Do trostruke točke vode dolazi kada je tlak samo 0,06 atm. Dakle, u uvjetima okoline nije uobičajeno da se voda sublimira.
Da biste saznali više, također pročitajte:
- Fizička stanja vode
- Fizička stanja materije
- Ukapljivanje ili kondenzacija
- Svojstva materije
- Očvršćivanje
- Fuzija
- Isparavanje
- Ključanje
- Isparavanje



