Kao što je objašnjeno u tekstu „Kataliza i katalizator”, Katalizatori su kemijske vrste koje ubrzavaju brzinu reakcija. Njegova je upotreba vrlo korisna u kemijskoj industriji, gdje se nastoji uštedjeti što više vremena u proizvodnji.
Međutim, u određenim je situacijama zanimljivije da se reakcija odvija sporije; kao na primjer kada želite odrediti brzinu vrlo brzih reakcija. Da bi se postigao taj podvig, kontrolirajući i proučavajući ove reakcije, uobičajeno je dodavati tvar koja usporava reakcije, koje se nazivaju inhibitori, otrovi ili antikatalizatori.
Te se kemijske vrste kombiniraju s katalizatorom, poništavajući ili smanjujući njegovo djelovanje. To je moguće jer je mehanizam djelovanja katalizatora smanjenje energije aktivacije, olakšavanje reakcijskog procesa i povećavanje njegove brzine; već inhibitori djeluju obrnuto, što znači da povećavaju energiju aktiviranja potrebnu da reaktanti dođu do aktiviranog kompleksa.
Primjer koji se može spomenuti je arsen (As), koji ima tu funkciju u reakciji Haber-Bosch, reakciji koja se široko koristi u industriji za proizvodnju amonijaka, koristeći željezo (Fe
(s)) kao njegov katalizator. Dakle, učinkovitost željeza postaje vrlo mala u prisutnosti arsena koji ga inhibira, odnosno on je katalizatorski otrov ove reakcije, što je prikazano u nastavku: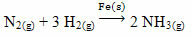
Arsen također može imati antikatalitičko djelovanje kada koristi metalnu platinu (Pt(s)) kao katalizator za reakciju izgaranja SO2 (g)za proizvodnju sumpornog trioksida (SO3 (g)). Prisutnost arsena, čak i u malim količinama, poništava katalitičko djelovanje platine, koja može paralizirati dio proizvodnje. Zato se obično u industrijama koje se bave ovom proizvodnjom koristi divanadij pentoksid (V2O5) kao katalizator umjesto platine.
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
Sljedeći se primjer javlja u sljedećoj reakciji razgradnje vodikovog peroksida:
2 sata2O2 (vod.) → 2 h2O(1) + 1 O2 (g)
U ovom slučaju, inhibitor koji se može koristiti je neka kiselina, jer kada je medij kiseo, reakcija se odvija sporije.
Ali inhibitor se također široko koristi u industriji, uglavnom da djeluje kao usporivač reakcije prirodne razgradnje hrane, pića, kozmetike i lijekova.
Na primjer, kozmetika može potrajati dugo dok ne dođe do potrošača; tako se u njima koriste različiti konzervansi, poput propilparabena koji se koristi u uljnoj fazi i djeluje protugljivično, te metilparabena koji se koristi u vodenoj fazi i koji djeluje antiseptički. Njihove odgovarajuće strukture prikazane su u nastavku:
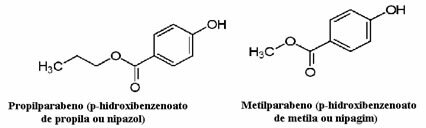
Zanimljivo je da na mnogim kozmetičkim etiketama postoji sljedeća fraza: „Ne sadrži parabene“. To znači da ova kozmetika nema ove konzervanse koje smo spomenuli i da, normalno, nisu testirana na životinjama.
Napisala Jennifer Fogaça
Diplomirao kemiju
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
FOGAÇA, Jennifer Rocha Vargas. "Inhibitori katalizatora"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/quimica/inibidores-catalisador.htm. Pristupljeno 27. lipnja 2021.


