Na molekule to su strukture koje imaju utvrđenu molarnu masu i relativno mali i točan broj atoma vezanih međusobno kovalentno, odnosno dijeljenjem elektrona.
Pogledajte tri primjera:
- Kisikov plin: Svaka od njegovih molekula nastaje dvostrukom vezom, odnosno dijeljenjem dva para elektrona između dva atoma kisika (O2);
- Voda: tvore je molekuli H2O. Što znači da svaka molekula ima dva atoma vodika koji dijele par elektrona, svaki s atomom kisika.
- Metan: ovaj spoj tvore molekule CH4, u kojem se četiri atoma vodika kovalentno vežu za jedan atom ugljika.
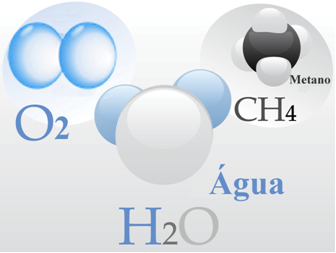
Molekularne tvari imaju neka karakteristična svojstva, kao što su:
- Različita topljivost u vodi i drugim otapalima;
- Oni se mogu predstaviti u tri fizička stanja;
- Općenito govoreći, oni su električni izolatori, čvrsti i tekući.
Sve molekule tvore nemetalni elementi, odnosno uključuju samo vodik, nemetale i polumetale. Ali ti elementi također mogu tvoriti tvari koje su prisutne samo u krutom stanju i koje imaju svojstva vrlo različita od svojstava molekula. ovo su makromolekule.
Makromolekule, također poznate kao kovalentne čvrste tvari ili krute tvari kovalentne mreže,to su strukture s vrlo visokom i nepreciznom molarnom masom, osim što ih tvori velika i neodređena količina atoma koji se kovalentno vežu i tvore trodimenzionalne rešetke. Makromolekule tvore kovalentni kristali ili atomski kristali.
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
Na primjer, atomi ugljika mogu dijeliti elektrone na mnogo načina i tvoriti mnogo različitih jednostavnih tvari. Ime je svojstvo da isti kemijski element mora tvoriti dvije ili više različitih jednostavnih tvari alotropija.
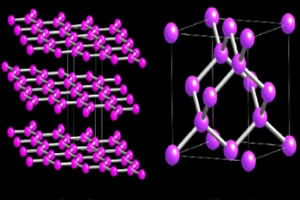
Dvije alotropne sorte ugljika koje tvore makromolekule su Dijamant i grafit. Na slikama dolje možete vidjeti da se u slučaju dijamanta svaki atom ugljika veže na četiri druga atoma ugljika i daje makromolekulu s tetraedarskom strukturom.

U međuvremenu, grafitnu strukturu tvore heksagonalni prstenovi sadržani u istoj ravnini. Atomi ugljika čine jednu dvostruku i dvije jednostruke veze.

Ali makromolekule se ne sastoje samo od jedne vrste elemenata; mogu se stvoriti i od atoma različitih kemijskih elemenata.
Primjer je silicijev dioksid (kvarc), čiji makromolekule imaju svaki atom silicija okružen s četiri atoma ugljika i svaki atom kisika povezan s dva atoma silicija.
Napisala Jennifer Fogaça
Diplomirao kemiju
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
FOGAÇA, Jennifer Rocha Vargas. "Molekule i makromolekule"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/quimica/moleculas-macromoleculas.htm. Pristupljeno 28. lipnja 2021.
Kemija
Što je alotropija, jednostavne tvari, plinoviti kisik, ozon, alotropni oblici, kemijski element kisik, ultraljubičaste zrake sunca, dijamant, grafit, atomskost, bijeli fosfor.
Karbonova prostorna formula, Lewisova elektronička formula, ravninska struktura, elektronički parovi, veza kovalentni, valentni sloj, evolucija atomskog modela, molekularna formula, strukturna formula, formule trodimenzionalni.
Kemijske formule, ravna strukturna formula, Couperova strukturna formula, trostruka veza, plin dušik, elektronička formula, Lewisova formula, molekularna formula, jednostruka veza, dvostruka veza, plin karbonska.


