Atomski broj, simboliziran slovom Z, odgovara količini protona koji postoje u jezgri atoma određenog kemijskog elementa. Na primjer, atomski broj vodika je 1, što znači da u svojoj atomskoj jezgri ima samo 1 proton.
Atomski se broj obično pojavljuje pored simbola za indeks kemijskog elementa (u donjem kutu) na lijevoj strani. Primjer: 1H.
U osnovnom je stanju atomski broj jednak broju elektrona, budući da je u tom stanju element neutralna, stoga količina pozitivnih naboja (protona) mora biti jednaka količini negativnih naboja (elektrona) atom.
Atomski broj je važan jer on je taj koji određuje glavne karakteristike i svojstva elementa, kao i njegovo ponašanje i mjesto u Periodnom sustavu. Elementi su navedeni u Periodnom sustavu uzlaznim redoslijedom atomskog broja, koji se obično pojavljuje iznad elementa, kao što je prikazano u nastavku. Imajte na umu da je prvi element vodik, H (Z = 1), zatim helij, He (Z = 2), zatim dolazi litij, Li (Z = 3) i tako dalje.
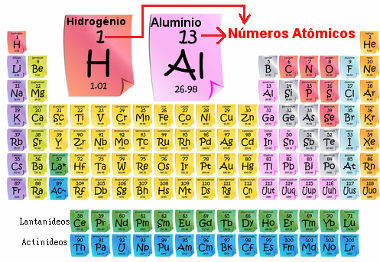
Atomski broj elemenata u Periodnom sustavu
Kemijski element možemo čak i pojmiti kao biće "Skup atoma koji imaju isti atomski broj". Dakle, kada govorimo, na primjer, o kemijskom elementu kisiku, govorimo o atomima s atomskim brojem 8. Ispod imamo atome kemijskih elemenata iz razdoblja 1 i 2 Periodnog sustava u rastućem redoslijedu atomskog broja:

Kemijski elementi iz razdoblja 1 i 2 Periodnog sustava u rastućem redoslijedu atomskog broja
Atomske brojeve u početku je definirao engleski fizičar Henry Gwyn Jeffreys Moseley (1887.-1915.) I prilikom izvođenja pokusa koji uključuju bombardiranje različitih elemenata kemičari s X-zrakama, primijetio je da je kvadratni korijen frekvencije X-zraka proizvedenih emisijom atomske jezgre izravno proporcionalan atomskom broju elementa u tablici. Povremeno. Ovim je zaključio da je atomski broj povezan sa svojstvima atoma jer predstavlja broj pozitivnih naboja u jezgri svakog atoma.
Kemijske veze ne utječu na atomski broj atoma, jer uključuju samo elektrone koji se nalaze u elektrosferi. Međutim, nuklearne reakcije uključuju atomsku jezgru pa je stoga uključen i atomski broj.
Na primjer, kada se čestice (uglavnom umjereni neutroni) bombardiraju na tešku, nestabilnu atomsku jezgru, ta jezgra je slomljena i daje dvije manje atomske jezgre, odnosno s manjim brojem protona i neutrona, oslobađajući kolosalnu količinu energije.
S druge strane, nuklearna fuzija je suprotan proces, to je kad se dvije male i lagane jezgre ujedine, nastajući veća i stabilnija jezgra, oslobađajući još veću količinu energije.
Dakle, kad god se pojave te nuklearne reakcije, potječu novi kemijski elementi, budući da se atomski brojevi početnih elemenata razlikuju od atomskih brojeva završnih elemenata. Na primjer, dolje pogledajte da iz fisije urana-235 s atomskim brojem 92 nastaju barij (Z = 56), kripton (Z = 36) i tri neutrona:

Reakcija nuklearne fisije urana-235
Napisala Jennifer Fogaça
Diplomirao kemiju
Izvor: Brazil škola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-numero-atomico.htm
