Što je temperatura viša, to je veća brzina reakcije.
To se lako može vidjeti u mnogim situacijama u našem svakodnevnom životu, kao u sljedećim primjerima:
- Kad želimo usporiti reakciju razgradnje hrane, spuštamo temperaturu, stavljajući je u hladnjak;

- Ako želimo ubrzati reakciju kuhanja hrane, samo je stavite u lonac za kuhanje. tlak koji, s porastom tlaka, također povećava temperaturu ključanja tekuće vode u kojoj se hrana je;

- Požari su općenito razarajući jer se temperatura okoline povećava, što uzrokuje povećanje brzine reakcije izgaranja;
- Da bi usporio metaboličke kemijske procese, smanjujući šanse za oštećenje mozga zbog nedostatak kisika, neke se operacije izvode snižavanjem tjelesne temperature pacijenta, zadržavajući se na oko 15 ° C;
- Ako šumeću tabletu stavimo u čašu vruće vode, a drugu u čašu hladne vode, prva će se otopiti puno brže.
Ali što objašnjava izravno proporcionalan utjecaj temperature na brzinu reakcije?
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
To je zato što je, kako je objašnjeno u tekstu „
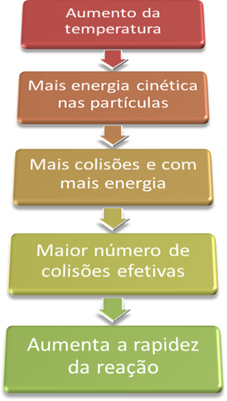
Uvjeti za pojavu kemijskih reakcija”, Da bi reakcija tekla, potrebno je zadovoljiti neke uvjete, kao što su čestice moraju se sudariti učinkovito i s minimalnom potrebnom energijom, koja se naziva energija aktivacije.Dakle, kada povećavamo temperaturu sustava, povećavamo i miješanje reakcijskih čestica i osiguravamo im više kinetičke energije. S tim će se dogoditi više sudara i s više energije, povećavajući količinu čestica koje će reagirati i, posljedično, povećavajući brzinu reakcije.
Napisala Jennifer Fogaça
Diplomirao kemiju
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
FOGAÇA, Jennifer Rocha Vargas. "Temperatura i brzina reakcija"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/quimica/temperatura-velocidade-das-reacoes.htm. Pristupljeno 27. lipnja 2021.


