THEdeelsaslušanje je laboratorijski, industrijski ili domaći postupak u kojem određena količina otapalo (čisti) se dodaje ili uklanja (isparavanjem) iz već postojeće otopine.
U bilo kojoj otopini uvijek postoji otapalo i barem jedna otopljena tvar, kao u smjesi od 500 ml vode i 10 g otopine natrijev klorid (NaCl) predstavljeni u nastavku:
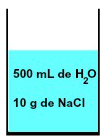
Prikaz smjese koju tvore voda i natrijev klorid
Ako se ovoj otopini doda volumen od 300 ml vode, naziva se ovaj postupak razrjeđivanje, dok se volumen otopine povećava - u ovom slučaju, na 800 ml -, bez promjene količine otopljene tvari.

Razrjeđivanje dodavanjem otapala u slanu otopinu
THE razrjeđivanje može se provesti i zagrijavanjem ove fiziološke otopine (sastavljene od 500 ml vode i 10 g NaCl) dok, na primjer, ne ostane 300 ml vode isparen. U tom bi se slučaju smanjio volumen otopine, međutim količina otopljene tvari ne bi se promijenila.

Razrjeđivanje isparavanjem otapala u fiziološkoj otopini
Principi razrjeđenja:
Konačni volumen otopine, kad se doda otapalo, uvijek je veći od početnog volumena;
Konačni volumen otopine, kada se otapalo ukloni, uvijek je manji od početnog volumena;
Masa otopljene tvari nikada se ne mijenja pri razrjeđivanju otopine;
Molski broj otopljene tvari nikad se ne mijenja pri razrjeđivanju otopine;
Kad se otapalu doda razrjeđenje, koncentracija konačne otopine uvijek je niža od koncentracije početne otopine;
Kad se ukloni razrjeđenje otapala, koncentracija konačne otopine uvijek je veća od koncentracije početne otopine.
Formule korištene u razrjeđivanju
Izračun konačnog volumena otopine:
Volumen konačne otopine u razrjeđenju u kojem se dodaje otapalo izračunava se prema sljedećem izrazu:
Vf = Vi + VThe
Vf = volumen konačne otopine
Vi = volumen početne otopine
VThe= volumen dodanog otapala
Ako se otapalo uklanja u razrjeđenju, konačni volumen izračunava se prema sljedećem izrazu:
Vf = Vi - Vi
Vi = volumen uparenog otapala.
⇒ Proračun zajednička koncentracija:
Koncentracija konačne otopine, nakon razrjeđivanja, može se izračunati na sljedeći način:
Çi.Vi = Cf.Vf
Çi= uobičajena koncentracija početne otopine
Vi = volumen početne otopine
Çf = molarnost ili koncentracija konačne otopine u mol / L
Vf= volumen konačne otopine
⇒ Proračun molarnost ili koncentracija u mol / L:
Molarnost konačne otopine, nakon razrjeđenja, može se izračunati sljedećim izrazom:
Mi.Vi = Mf.Vf
Mi= molarnost ili koncentracija početne otopine u mol / L
Vi = volumen početne otopine
Mf = molarnost ili koncentracija konačne otopine u mol / L
Vf= volumen konačne otopine
Calcu Izračun skupnog naslova:
Naslov konačne otopine, nakon razrjeđenja, može se izračunati prema sljedećem izrazu:
Ti.mi = Tf.mf
Ti= naslov početnog rješenja
mi = masa početne otopine
Tf = naslov konačnog rješenja
mf= masa konačne otopine
Kako se naslov može izračunati i kao postotak, a u vodenim otopinama masa nastoji imati jednaku vrijednost kao volumen, možemo upotrijebiti sljedeći matematički izraz:
Stri.Vi = Pf.Vf
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
Stri= postotak početne otopine
Vi = volumen početne otopine
Strf = postotak konačnog rješenja
Vf= volumen konačne otopine
Primjeri izračuna izrađenih u razrjeđenju:
1. primjer - (UFBA) Dodavanjem 300 ml vode u 100 ml 8% otopine natrijevog bikarbonata, koncentracija dobivene otopine je:
a) 24% b) 18% c) 9% d) 4% e) 2%
Podaci dobiveni vježbom:
Postotak početne otopine (stri) = 8%
Početni volumen otopine (Vi) = 100 ml
Konačni volumen otopine (Vf) = 400 ml (rezultat miješanja od 300 ml do 100 ml)
Postotak konačne otopine (strf) = ?
Za izračunavanje postotka koncentracije otopine možemo koristiti ove vrijednosti dane u sljedećem izrazu:
Stri.Vi = Pf.Vf
8.100 = Pf.400
800 = P.f.400
Strf = 800
400
Strf = 2%
2. primjer - (UFPA) 200 ml otopine magnezijevog hidroksida, Mg (OH)2, pripremljeni su otapanjem 2,9 g baze u vodi. Koji se volumen ove otopine mora razrijediti na 300 ml da bi se dobila otopina s molaritetom jednakim 0,125 M? Podaci: H = 1; Mg = 24; O = 16.
a) 450 ml b) 150 ml c) 400 ml d) 300 ml e) 900 ml
Podaci dobiveni vježbom:
Masa otopljene tvari u početnoj otopini (m1) = 2,9 g
Količina otopine koja će se koristiti za razrjeđivanje = 200 ml ili 0,2 L (nakon dijeljenja s 1000)
Početni volumen otopine (Vi) koji će se razrijediti =?
Konačni volumen otopine (Vf) = 300 ml
Molarnost ili koncentracija konačne otopine u mol / L (Mf) = 0,125M
Da bismo izračunali koncentraciju kao postotak otopine, moramo učiniti sljedeće:
Korak 1: Izračunajte molarnu masu otopljene tvari.
U tu svrhu moramo pomnožiti broj atoma svakog elementa s njegovom atomskom masom, a zatim dodati rezultate:
MMg (OH) 2 = 1.24 + 2.16 + 2.1
MMg (OH) 2 = 24 + 32 + 2
MMg (OH) 2 = 58 g / mol
Korak 2: Izračunajte koncentraciju u mol / L ili molarnost početne otopine:
Mi = m1
MV
Mi = 2,9
58.0,2
Mi = 2,9
11,6
Mi = 0,25 mol / L
Korak 3: Odredite volumen otopine koja će se razrijediti koristeći ponuđene vrijednosti i pronađene u sljedećem izrazu:
Mi.Vi = Mf.Vf
0.25.Vi = 0,125.300
0.25.Vi = 37,5
Vi = 37,5
0,25
Vi = 150 ml
3. primjer - (UEG-GO) Uzmimo u obzir da 100 ml vodene otopine bakrenog sulfata, s koncentracijom jednakom 40 g. L–1, Dodano je 400 ml destilirane vode. U tom će slučaju svaki ml nove otopine imati masu, u mg, jednaku:
a) 2 b) 4 c) 8 d) 10
Podaci dobiveni vježbom:
Količina vode dodane u razrjeđenje = 400 ml
Početni volumen otopine (Vi) = 100 ml
Konačni volumen otopine (Vf) = 500 ml (rezultat miješanja od 400 ml do 100 ml)
Uobičajena koncentracija početne otopine (Ci) = 40 g. L–1
Uobičajena koncentracija konačne otopine (Cf) u mg / ml =?
Da bismo izračunali koncentraciju otopine u mg / ml, moramo učiniti sljedeće:
Korak 1: Pretvorite početnu koncentraciju otopine iz g / L u mg / mL.
Da bismo to učinili, moramo pomnožiti i brojnik i nazivnik s 1000 i samo podijeliti zadanu koncentraciju s 1000:
Çi = 40g 1000
1L. 1000
Çi = 40 mg / ml
Stoga su jedinice g / L i mg / ml iste.
Korak 2: Izračunajte koncentraciju u mg / ml koristeći vrijednosti dane u sljedećem izrazu:
Çi.Vi = Cf.Vf
40.100 = Cf.500
4000 = Cf.500
Çf = 4000
500
Çf = 8 mg / ml
Ja, Diogo Lopes Dias
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
DANI, Diogo Lopes. "Što je razrjeđivanje?"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-diluicao.htm. Pristupljeno 28. lipnja 2021.