U sportskim aktivnostima, u bolnicama i u našem svakodnevnom životu primjena vrućih i hladnih instant obloga vrlo je česta. U oba slučaja određene tvari reagiraju s vodom. Na primjer, u slučaju hladnog obloga, sadrži dvije kapsule koje odvajaju vodu od NH4NA3, koji, kada se otopi u vodi, upija toplinu i proizvodi trenutnu hladnoću. U slučaju vrućih obloga, CaCl se otapa u vodi2 ili MgSO4, koji oslobađaju energiju koja stvara toplinu.
Ali zašto određena rješenja daju toplinu, budući da su egzotermna; a drugi apsorbiraju, budući da su endotermni?
Pa, da bismo razumjeli ovo pitanje moramo proučiti varijacija entalpije (ΔH) otopina, koji se sastoji od dva koraka:
(1.) Retikularna entalpija (ΔHpovlačenje): kada se otopljena tvar otopi u vodi, prvi korak je odvajanje njenih iona koji se nalaze u kristalnoj rešetki. Da bi se prekinule veze između iona, potrebno je opskrbiti sustav sustavom. Dakle, ovaj prvi postupak jest endotermički, jer upija energiju; biti tvoj pozitivna entalpija (ΔH> 0).
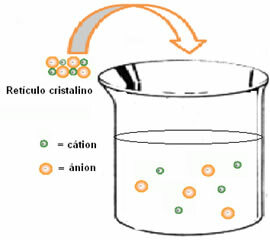
(2.) Entalpija hidratacije (ΔHskrivao)
: nakon što se ioni odvoje, obavijaju ih molekule otapala. U slučaju vode, to je otapalo i kažemo da se odvija hidratacija. Dipole vode privlače suprotno nabijeni ioni; dakle, da bi se došlo do ove interakcije, potrebno je oslobađanje energije. Dakle, u hidrataciji entalpija će biti negativna (ΔH <0), jer je postupak egzotermno.Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
Donja slika prikazuje kako dolazi do hidratacije, u kojoj postoji ionsko-dipolna interakcija, odnosno privlačenje između naboja odvojenih iona i vodenog dipola:
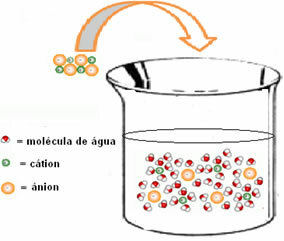
Promjena entalpije otopine (ΔHSunce) odredit će se zbrojem ove dvije entalpije. Ako je rezultat pozitivan, to znači da je retikularna entalpija veća, pa će entalpija otapanja ukazivati na to da je proces endotermičan.
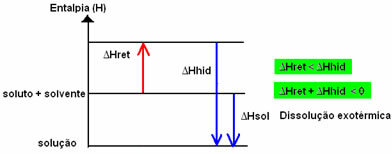
Dijagram entalpije endotermnog otapanja prikazan je u nastavku:
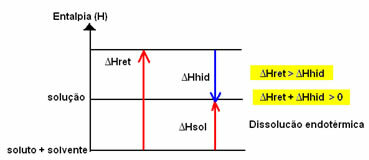
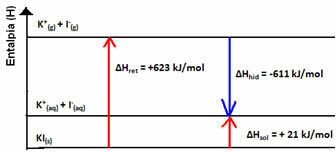
Na to ukazuje slučaj otapanja kalijevog jodida prikazan u nastavku:
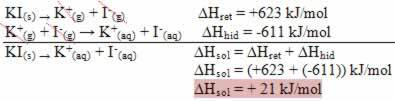
Vaš dijagram entalpije predstavljat će:
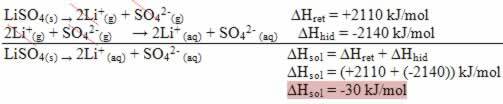
Ako je rezultat pozitivan, entalpija hidracije bit će veća od retikularne, a postupak je egzotermičan. Dijagrami entalpije egzotermnih otapanja predstavljeni su kako je prikazano u sljedećem primjeru:
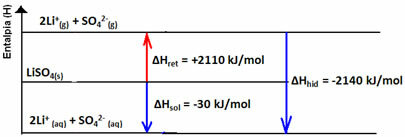
Zabilježite svoj dijagram entalpije u nastavku:
Napisala Jennifer Fogaça
Diplomirao kemiju
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
FOGAÇA, Jennifer Rocha Vargas. "Varijacija entalpije rješenja"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/quimica/variacao-entalpia-solucao.htm. Pristupljeno 28. lipnja 2021.


