Prije razgovora o nomenklaturi a kvaternarna amonijeva sol pravilno, važno je zapamtiti što je ovaj organski spoj. Kvartarna amonijeva sol potječe od zamjene vodika prisutnih u amonijevom kationu (NH4+) po radikali organsko, kao što je prikazano dolje:
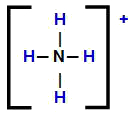
Strukturna formula amonijevog kationa
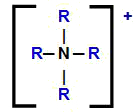
Strukturna formula amonijevog kationa s vodikovima zamijenjenim organskim radikalima
Uz zamjenu vodika, svaka kvaternarna amonijeva sol ima i bilo koji anion koji prati kation dobiven iz amonija. Dakle, opću strukturnu formulu ovog spoja možemo predstaviti na sljedeći način:
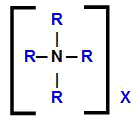
Opća strukturna formula kvaternarne amonijeve soli
Dakle, očito je da u formuli kvaternarne amonijeve soli imamo četiri organska radikala, ista ili različita, i bilo koji anion (X). Da bismo izvršili nomenklaturu ovih spojeva, moramo uzeti u obzir tu činjenicu.
Pogledajte kako nomenklatura kvaterne amonijeve soli prema IUPAC (Međunarodna unija čiste i primijenjene kemije):
Ime aniona + de + naziv radikala po abecednom redu + amonij
Sada slijedite neke primjeri primjene pravila nomenklatura kvaternarnih amonijevih soli:
Benzil-oktadecil-dimetilamonij-jodid
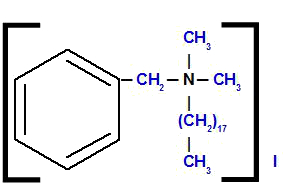
Analizirajući strukturu, primjećujemo da anion prisutan u spoju je Ja, koji se zove jodid. Lijevo od strukture imamo radikal benzil (spoj benzena s CH skupinom2). Odozgo i s desne strane imamo dva radikala metil (CH3), koji će se zvati 'dimetil'. Na dnu imamo radikal oktadecil, koji u svom lancu ima osamnaest atoma ugljika.
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
Dakle, naziv počinje s jodidom, nakon čega slijedi prijedlog plus naziv benzil, zatim oktadecil (zbog abecednog reda) i, na kraju, dimetil s amonijem.
Promatranje: Izrazi oct i di ne sudjeluju u abecednoj sekvencijalnoj organizaciji imena spoja.
tetraetilamonijev klorid
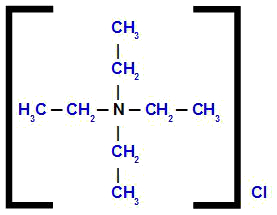
Analizirajući strukturu, primjećujemo da anion prisutan u spoju je Kl, koji se zove klorid. Četiri organska radikala prisutna u strukturi su etil (CH3-CH2-); stoga dobivaju naziv tetraetil.
Dakle, naziv započinje kloridom, nakon čega slijedi prijedlog plus naziv tetraetil, a iza njega slijedi izraz amonij.
Benzil-tridecil-dimetilamonij-bromid

Analizirajući strukturu, primjećujemo da anion prisutan u spoju je br, koji se zove bromid. Lijevo od strukture imamo radikal benzil (spoj benzena s CH skupinom2). Odozgo i s desne strane imamo dva radikala metil (CH3), koji će se zvati 'dimetil'. Na dnu imamo radikal tridecil, jer u njegovom lancu ima trinaest atoma ugljika.
Dakle, naziv započinje jodidom, nakon čega slijedi prijedlog plus naziv benzil, zatim tridecil (zbog abecednog reda) i, na kraju, dimetil s amonijem.
Difenil-dimetilamonij-sulfat
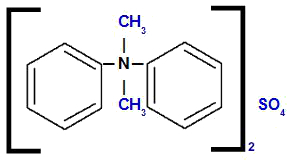
Analizirajući strukturu, primjećujemo da anion prisutan u spoju je SAMO4, koji se zove sulfat. S lijeve i desne strane konstrukcije imamo fenilni radikal (benzen), koji će se zvati 'difenil'. Na vrhu i na dnu imamo metilni radikali (CH3), koji će se zvati 'dimetil'.
Dakle, naziv započinje sulfatom, nakon čega slijedi prijedlog plus ime difenil, zatim dimetil (zbog abecednog poretka) i, konačno, amonij.
Ja, Diogo Lopes Dias