Eter to je oksigenirana organska funkcija, to jest ima kemijski element kisik, osim ugljika i vodika. Ova funkcija ima za glavnu strukturnu karakteristiku prisustvo dvoje organski radikali vezan za atom kisika.
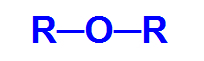
Opća strukturna formula etera
Dakle, ugljikov lanac etera je heterogen i može imati dva identična ili različita radikala alkil, vrste radikala koji nemaju aromatičnu strukturu, ili aril, radikali koji nemaju strukturu aromatičan.
Fizičke karakteristike etera
Što se tiče fizičkog stanja na sobnoj temperaturi: kada eter u svom sastavu ima četiri ili više atoma ugljika, tekućina je;
Što se tiče tališta i vrelišta: u usporedbi s drugim masnim organskim spojevima približni molari, imaju tačku topljenja sličnu onoj u alkana i nižu od ostalih spojeva organski;
Što se tiče gustoće: oni su spojevi koji imaju malu gustoću u usporedbi s vodom;
Što se tiče interakcijskih sila: eteri su sastavljeni s niskim polaritetom, međusobno djeluju kroz slabu trajnu dipolnu interakciju. S vodom i alkoholima eteri imaju sposobnost interakcije vodikovim vezama.
Što se tiče polaritet: su spojevi koji imaju kutnu geometriju, dakle, oni su polarni.
Što se tiče organoleptičkih karakteristika: to su tvari koje daju vrlo ugodan miris, ali njihovo udisanje može izazvati ovisnost.
Službena nomenklatura etera
Prefiks manjeg stabla + oksi + prefiks glavnog stabla + infiks + o
Za obavljanje službene nomenklature a eter, Ključno je odrediti koji je vaš glavni ligand, a koji manji. Da biste to učinili, slijedite dva primjera primjene ovog pravila imenovanja u nastavku:
1. primjer:
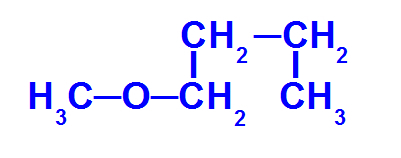
Strukturna formula etera s manje ugljika
Gornji eter ima sljedeće radikale:
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
Metil (CH3-);
Butil (CH3-CH2-CH2-CH2-).
Da bismo imenovali ovaj spoj, imamo:
manji radikalni prefiks: Met
+
oksi
+
glavni matični prefiks: ali
+
an (jer ima samo pojedinačne poveznice)
+
O
Dakle, ime ovoga eter to će biti metoksibutan.
2. primjer:
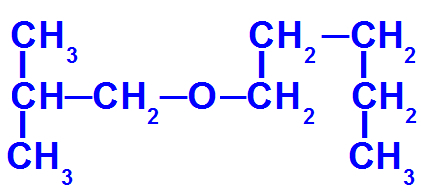
Strukturna formula etera s više ugljika
Ovaj eter ima sljedeće radikale:
Izobutil [(CH3)2-CH-CH2-);
pentil (CH3-CH2-CH2-CH2-CH2).
Da bismo to imenovali, imamo:
manji radikalni prefiks: izobut
+
oksi
+
glavni matični prefiks: pent
+
an (jer ima samo pojedinačne poveznice)
+
O
Dakle, naziv eter u pitanju će biti izobutoksipentan.
Uobičajena nomenklatura etera
Eter + naziv radikala (najjednostavniji, a zatim i najsloženiji) + ico
ili
Radikalna imena + eter
Slijedi dva primjera primjene za ovo pravilo imenovanja:
1. primjer:

Strukturna formula etera koji ima četiri ugljika
Da eter predstavlja sljedeće radikale:
Metil (CH3);
Izopropil (CH3-CH-CH3).
Dakle, za ovaj spoj imamo:
Eter
+
sporedni radikal: metil
+
glavni radikalni prefiks: izopropil
+
ich
Dakle, naziv eter u pitanju će biti metil izopropil eter, ili metil izopropil eter.
2. primjer:

Strukturna formula etera koji ima pet ugljika
Gornji eter ima sljedeće radikale:
Etil (CH3-CH2-);
Propil (CH3-CH2-CH2-).
Da bismo imenovali ovaj spoj, imamo:
Eter
+
sporedni radikal: etil
+
glavni radikalni prefiks: propil
+
ich
Dakle, naziv eter u pitanju će biti etil propil eter, koji također može biti etil propil eter.
Upotreba etera
Općenito se koriste eteri:
Kao inertna organska otapala, tj. Ne sudjelujući u bilo kojoj reakciji;
Koristi se za vađenje esencija, poput cvijeća, drveta itd .;
Koristi se za ekstrakciju raznih ulja i masti.
Ja, Diogo Lopes
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
DANI, Diogo Lopes. "Što je eter?"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-eter.htm. Pristupljeno 28. lipnja 2021.
Kemija

Esteri, aroma za hranu, aroma, reakcija esterifikacije, metil antranilat, pentil acetat, butil etanoat, etil butanoat, propanetriol, glicerin, stearin.


