परमाणु पदार्थ के आकार देने वाले को दिया गया नाम है (वह सब कुछ जो स्थान घेरता है और जिसमें द्रव्यमान होता है)। यह नाम ग्रीक दार्शनिक डेमोक्रिटस और ल्यूसिपस द्वारा प्रस्तावित किया गया था। रासायनिक तत्व, अणु, पदार्थ और कार्बनिक या अकार्बनिक पदार्थ परमाणुओं द्वारा बनते हैं।
इसके संविधान में, परमाणु में कण (प्रोटॉन, न्यूट्रॉन और इलेक्ट्रॉन) होते हैं, जो पदार्थ का सबसे छोटा हिस्सा नहीं होते हैं। फिर भी, आपका विज़ुअलाइज़ेशन संभव नहीं है. परमाणु के बारे में जो ज्ञात है वह वैज्ञानिक रूप से सिद्ध भौतिक, रासायनिक और गणितीय पहलुओं से संबंधित है।
परमाणु के बारे में ज्ञान के विकास ने कई तकनीकों का विकास और सुधार किया है।
एक परमाणु की मूल संरचना
कोर: परमाणु का सघन क्षेत्र और प्रोटॉन और न्यूट्रॉन धारण करता है;
उर्जा स्तर: नाभिक के आसपास के क्षेत्र और आवास उपस्तर, कक्षा और इलेक्ट्रॉन। सात ऊर्जा स्तर हैं, जिन्हें K, L, M, N, O, P और Q अक्षरों द्वारा दर्शाया गया है;
ऊर्जा उपस्तर: वे क्षेत्र हैं जिनमें कक्षक स्थित हैं। वे सभी स्तरों पर मौजूद हैं और अक्षरों (एस, पी, डी एफ) द्वारा दर्शाए जाते हैं। इसकी मात्रा प्रत्येक स्तर पर निर्भर करती है: के (एस सबलेवल हैं), एल (एस और पी सबलेवल हैं), एम (एस, पी और डी सबलेवल हैं), एन (उपस्तर एस, पी, डी और एफ है), ओ (उपस्तर एस, पी, डी और एफ है), पी (उपस्तर एस, पी और डी है) और क्यू (उपस्तर एस और है पी);
परमाणु कक्षक: जिन क्षेत्रों में इलेक्ट्रॉन मिलने की सबसे अधिक संभावना है। प्रत्येक सबलेवल में ऑर्बिटल्स की एक अलग संख्या होती है: s (एक ऑर्बिटल), p (तीन ऑर्बिटल्स), d (पांच ऑर्बिटल्स), और f (सात ऑर्बिटल्स);
प्रोटान: सकारात्मक कण (पी द्वारा दर्शाया गया);
इलेक्ट्रॉनों: नकारात्मक कण जिनमें तरंग व्यवहार भी होता है (ई द्वारा दर्शाया गया);
न्यूट्रॉन: अनावेशित कण जो नाभिक में प्रोटॉनों के बीच प्रतिकर्षण को कम करते हैं (n द्वारा निरूपित)।
माइंड मैप: परमाणु
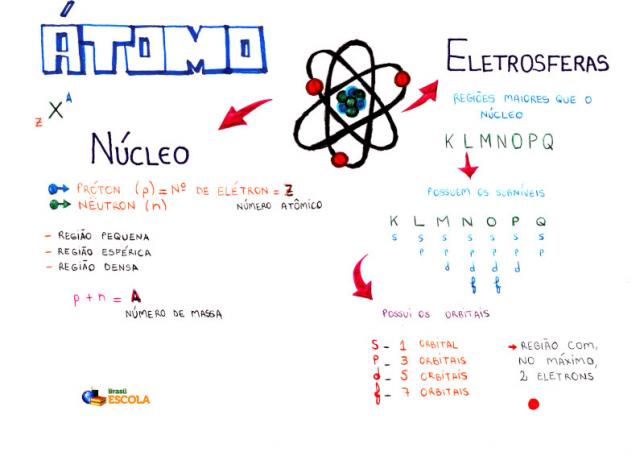
* माइंड मैप को पीडीएफ में डाउनलोड करने के लिए, यहाँ क्लिक करें!
एक परमाणु का प्रतिनिधित्व
किसी परमाणु को निरूपित करने का सबसे सरल तरीका उसके द्वारा निर्मित रासायनिक तत्व के संक्षिप्त नाम का उपयोग करना है। उदाहरण के लिए, संक्षिप्त नाम से, उन सभी परमाणुओं का प्रतिनिधित्व करता है जो रासायनिक तत्व सेलेनियम बनाते हैं।
परमाणु का प्रतिनिधित्व करने वाला संक्षिप्त नाम अभी भी दो महत्वपूर्ण जानकारी प्रदान कर सकता है: परमाणु संख्या (अक्षर Z द्वारा दर्शाया गया और हमेशा बाईं ओर परमाणु के संक्षिप्त नाम के नीचे) और द्रव्यमान संख्या (अक्षर A द्वारा दर्शाया गया है, जिसे परमाणु के परिवर्णी शब्द के शीर्ष पर बाईं या दाईं ओर स्थित किया जा सकता है) परमाणु)।
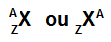
द्रव्यमान संख्या और परमाणु क्रमांक वाले परमाणु का परिवर्णी शब्द
परमाणु क्रमांक (जेड): परमाणु के नाभिक में मौजूद प्रोटॉन की संख्या और ऊर्जा स्तरों में मौजूद इलेक्ट्रॉनों (e) की संख्या को इंगित करता है।
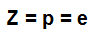
वह सूत्र जो परमाणु क्रमांक के प्रतिनिधित्व को इंगित करता है
-
मास संख्या (ए): परमाणु के नाभिक में मौजूद द्रव्यमान को इंगित करता है, जो प्रोटॉन (पी) और न्यूट्रॉन की संख्या (एन) की संख्या के योग के परिणामस्वरूप होता है।
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)

वह सूत्र जो द्रव्यमान संख्या के प्रतिनिधित्व को इंगित करता है
परमाणु समानताएं
एक ही रासायनिक तत्व या विभिन्न रासायनिक तत्वों के परमाणुओं की तुलना प्रोटॉन, इलेक्ट्रॉनों, न्यूट्रॉन और द्रव्यमान की संख्या के संदर्भ में की जा सकती है, जिन्हें निम्नानुसार वर्गीकृत किया जा सकता है:
ए) आइसोटोप
वे परमाणु हैं जिनमें:
समान परमाणु संख्या;
प्रोटॉन की समान संख्या;
विभिन्न द्रव्यमान संख्या;
न्यूट्रॉन की विभिन्न संख्या;
उदाहरण:
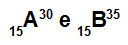
परमाणु A और B समस्थानिक हैं
परमाणु A और B समस्थानिक हैं क्योंकि:
परमाणु A में 15 प्रोटॉन, परमाणु क्रमांक 15, 15 इलेक्ट्रॉन, 15 न्यूट्रॉन और द्रव्यमान संख्या 30 है।
एटम बी में 15 प्रोटॉन, परमाणु क्रमांक 15, 15 इलेक्ट्रॉन, 20 न्यूट्रॉन और द्रव्यमान संख्या 35 है।
बी) आइसोबार
वे परमाणु हैं जिनमें:
विभिन्न परमाणु संख्याएं;
प्रोटॉन की विभिन्न संख्या;
इलेक्ट्रॉनों की विभिन्न संख्या;
समान द्रव्यमान संख्या;
विभिन्न संख्या में न्यूट्रॉन।
उदाहरण:
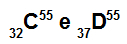
परमाणु सी और डी आइसोबार हैं
परमाणु C और D समदाब रेखीय हैं क्योंकि:
परमाणु C में 32 प्रोटॉन, परमाणु क्रमांक 32, 32 इलेक्ट्रॉन, 23 न्यूट्रॉन और द्रव्यमान संख्या 55 है।
परमाणु डी में 37 प्रोटॉन, परमाणु संख्या 37, 37 इलेक्ट्रॉन, 18 न्यूट्रॉन और द्रव्यमान संख्या 55 के बराबर है।
ग) आइसोटोन्स
वे परमाणु हैं जिनमें:
विभिन्न परमाणु संख्याएं;
प्रोटॉन की विभिन्न संख्या;
इलेक्ट्रॉनों की विभिन्न संख्या;
विभिन्न द्रव्यमान संख्या;
न्यूट्रॉन की समान संख्या।
उदाहरण:
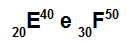
परमाणु E और F समस्थानिक हैं
परमाणु E और F समस्थानिक हैं क्योंकि:
एटम ई में 20 प्रोटॉन, परमाणु क्रमांक 20, 20 इलेक्ट्रॉन, 20 न्यूट्रॉन और द्रव्यमान संख्या 40 है।
परमाणु F में 30 प्रोटॉन, परमाणु क्रमांक 30, 30 इलेक्ट्रॉन, 20 न्यूट्रॉन और द्रव्यमान संख्या 50 है।
डी) आइसोइलेक्ट्रॉनिक्स
वे परमाणु हैं जिनमें:
इलेक्ट्रॉनों की समान संख्या।
ध्यान दें: आइसोइलेक्ट्रॉनिक परमाणुओं में समान द्रव्यमान संख्या (आइसोबार), समान संख्या में न्यूट्रॉन (आइसोटोन) या समान संख्या में प्रोटॉन (आइसोटोप) हो सकते हैं।
उदाहरण:
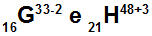
परमाणु G और H समइलेक्ट्रॉनिक हैं
परमाणु G और H समइलेक्ट्रॉनिक हैं क्योंकि:
एटम जी में 16 प्रोटॉन हैं, परमाणु संख्या 16 के बराबर, 18 इलेक्ट्रॉन (चिह्न -2 इंगित करता है कि इसमें प्रोटॉन की संख्या से दो अधिक इलेक्ट्रॉन हैं), 17 न्यूट्रॉन और द्रव्यमान संख्या 33 के बराबर है।
एटम एच में 21 प्रोटॉन हैं, परमाणु संख्या 21 के बराबर, 18 इलेक्ट्रॉन (+3 चिन्ह इंगित करता है कि इसमें प्रोटॉन की संख्या से तीन कम इलेक्ट्रॉन हैं), 27 न्यूट्रॉन, और द्रव्यमान संख्या 48 के बराबर है।
मेरे द्वारा। डिओगो लोपेज डायस
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? देखो:
DAYS, डिओगो लोपेज। "परमाणु क्या है?"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-atomo.htm. 27 जून, 2021 को एक्सेस किया गया।
रसायन विज्ञान
परमाणु और ब्रह्मांड का निर्माण, परमाणु सिद्धांत, कि सब कुछ बना है, पदार्थ परमाणुओं से बना है, चार तत्वों का सिद्धांत, प्राचीन कीमियागर, परमाणु सिद्धांत, मौलिक कण।
रसायन विज्ञान

नील्स बोहर, बोहर का परमाणु, परमाणु भौतिकी, स्थिर परमाणु, परमाणु मॉडल, ग्रह प्रणाली, इलेक्ट्रोस्फीयर की परतें, ऊर्जा स्तर, इलेक्ट्रॉन गोले, इलेक्ट्रॉन ऊर्जा, रदरफोर्ड परमाणु मॉडल, उत्तेजित अवस्था परमाणु।

