गैसआदर्श वही है जहां टक्कर कणों के बीच पूरी तरह से लोचदार होते हैं. उसके कणों के बीच किसी भी प्रकार की परस्पर क्रिया नहीं होती है, जैसे ताकतों आकर्षक या प्रतिकारक, इसके अलावा, ये कण स्थान नहीं लेते हैं।
के अनुसार गैसों का गतिज सिद्धांत, एक आदर्श गैस की उष्मप्रवैगिकी अवस्था को के चरों द्वारा पूरी तरह से वर्णित किया जाता है दबाव, मात्रा और तापमान.
नज़रयह भी: कैलोरीमेट्री: माइंड मैप, फॉर्मूला और सॉल्व्ड एक्सरसाइज
आदर्श गैस अवधारणा
आदर्श गैसें विशेष रूप से बनी होती हैं कणोंमेंआयामसमयनिष्ठ (नगण्य आकार के) जो. में हैं आंदोलनअराजक चालू है उच्चवेग। इस प्रकार की गैस में, तापमान और कणों के अनुवाद की गति समानुपाती होती है।
चूँकि एक आदर्श गैस के कणों के बीच कोई अन्योन्य क्रिया नहीं होती है, अत: आंतरिक ऊर्जा इस गैस का योग हमेशा के योग के बराबर होता है गतिज ऊर्जा इसे बनाने वाले सभी कणों का।
आदर्श गैसें जो भी हों, वे हमेशा एक जैसी ही रहेंगी संख्यामेंकणों एक ही मात्रा के लिए। उनका द्रव्यमान, बदले में, सीधे आपके. पर निर्भर करेगा अणु भार
(जी/मोल में मापा जाता है), इसके अलावा, आदर्श गैस का 1 मोल (लगभग 6.0.1023 कण) हमेशा एक. पर कब्जा करेंगे 22.4 एल के बराबर मात्रा।आप गैसोंअसली, जहां की घटना होती है टक्करअलचकदार कणों के बीच, आदर्श गैसों के व्यवहार के बहुत करीब आ जाते हैं कम दबाव और उच्च तापमान शासन। संयोग से, पृथ्वी पर दबाव और तापमान (25 डिग्री सेल्सियस और 1 एटीएम) की सामान्य परिस्थितियों में, अधिकांश गैसें आदर्श गैसों की तरह व्यवहार करती हैं, और इससे थर्मोडायनामिक व्यवहार के बारे में भविष्यवाणियों की गणना की सुविधा मिलती है जो अपने।
कुछ गैसें, जैसे भाप, जो में पतला है वायुमंडलीय गैस, को आदर्श गैस नहीं माना जा सकता लेकिन हाँ गैसोंअसली। इन गैसों में उनके कणों के बीच महत्वपूर्ण अंतःक्रिया होती है, जो कर सकते हैं गाढ़ा, उन्हें पैदा कर रहा है द्रवित करना, अगर वहाँ एक है तापमान में गिरावट.
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
आदर्श गैसों के लक्षण
इसे यहां देखें सार, आदर्श गैसों की कुछ विशेषताएं:
- उनमें कणों के बीच केवल पूरी तरह से लोचदार टकराव होते हैं;
- उनमें कणों के बीच कोई अंतःक्रिया नहीं होती है;
- उनमें कणों का आयाम नगण्य होता है;
- आदर्श गैस के 1 मोल में 22.4 लीटर का आयतन होता है, चाहे गैस कुछ भी हो;
- वास्तविक गैसें निम्न दाब और उच्च तापमान की स्थिति में आदर्श गैसों की तरह व्यवहार करती हैं;
- अधिकांश गैसें आदर्श गैसों के समान व्यवहार करती हैं।
आदर्श गैस कानून
विद्वानों द्वारा विकसित गैसों का अध्ययन चार्ल्सबॉयल,यूसुफलुईसमलैंगिक Lussac तथा रॉबर्टबॉयल के उद्भव के लिए नेतृत्व किया तीन अनुभवजन्य कानून, के शासन में आदर्श गैसों के व्यवहार की व्याख्या करने के लिए प्रयोग किया जाता है तापमान, दबाव तथा आयतनस्थिरांक, क्रमशः।
इन कानूनों ने मिलकर किसके उद्भव के लिए आवश्यक आधार बनाया आदर्श गैस कानून, जो संबंधित है गैस की प्रारंभिक थर्मोडायनामिक अवस्था state, मात्रा P. द्वारा परिभाषित1, टी1 और वी1, आपके साथ अंतिम थर्मोडायनामिक अवस्था (पी2, वी2 और टी2), कुछ सहने के बाद गैस परिवर्तन.
इसकी जाँच पड़ताल करो सूत्र सामान्य गैस कानून:
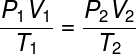
सामान्य गैस कानून कहता है कि उत्पाद देता है दबाव फर आयतनकागैस, थर्मोडायनामिक तापमान से विभाजित, केल्विन में, एक स्थिरांक के बराबर होता है। यह स्थिरांक, बदले में, द्वारा वर्णित है क्लैपेरॉन समीकरण, घड़ी:
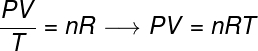
नहीं न - मोल्स की संख्या (mol)
आर - उत्तम गैसों का सार्वत्रिक स्थिरांक (0.082 atm.l/mol. के या 8.31 जे/मोल। क)
सूत्र में, पी गैस द्वारा लगाया गया दबाव है, वी इस गैस का आयतन है, और टी तापमान है, जिसे केल्विन में मापा जाता है। महानता नहीं न मोल्स की संख्या को संदर्भित करता है, जबकि आर आदर्श गैसों का सार्वभौमिक स्थिरांक है, जिसे अक्सर atm.l/mol की इकाइयों में मापा जाता है। के या जे/मोल में। K, बाद वाले द्वारा अपनाया जा रहा है एसआई.
नज़रयह भी:सौर हवा क्या है और यह पृथ्वी के वायुमंडल को कैसे प्रभावित करती है?
आदर्श गैस की आंतरिक ऊर्जा
ऊर्जाअंदर का के बीच उत्पाद का उपयोग करके आदर्श गैसों की गणना की जा सकती है लगातारमेंबोल्ट्जमान और थर्मोडायनामिक तापमान, ध्यान दें:
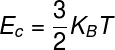
कख - बोल्ट्जमान स्थिरांक (कख = 1,38.10-23 जम्मू/कश्मीर)
पिछले रिश्ते से, जो हमें गणना करने की अनुमति देता है औसत गतिज ऊर्जा एक आदर्श गैस के कणों से, हम निम्नलिखित सूत्र बनाते हैं, जिसका उपयोग यह गणना करने के लिए किया जा सकता है कि अणुओं का माध्य वर्ग वेग किसी दिए गए तापमान T के लिए एक आदर्श गैस का, ध्यान दें:
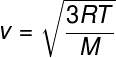
म - दाढ़ द्रव्यमान (जी/मोल)
यह सूत्र आपको यह देखने की अनुमति देता है कि a इसके अलावापरतापमान एक आदर्श गैस का कणों के माध्य वर्ग वेग में वृद्धि होती है।
अधिक जानते हैं:जानिए प्रकाश किससे बना होता है और इसकी विशेषताएं क्या हैं
आदर्श गैसों पर हल किए गए अभ्यास
प्रश्न 1) 227 डिग्री सेल्सियस के तापमान पर एक आदर्श गैस के दो मोल और 1 एटीएम के दबाव में पाए जाते हैं। इस गैस का आयतन लीटर में परिकलित कीजिए।
डेटा: आर = ०.०८२ atm.l/mol. क
क) 75 लीटर
बी) 82 एल
सी) 15 एल
डी) 27 एल
ई) 25 एल
खाका: अक्षर बी
संकल्प:
इस गैस के आयतन की गणना करने के लिए, हम क्लैपेरॉन समीकरण का उपयोग करेंगे, हालांकि, गणना करने से पहले, 227 डिग्री सेल्सियस के तापमान को केल्विन में बदलना आवश्यक है। इसके लिए हम इस तापमान में कारक 273 जोड़ते हैं, जिसके परिणामस्वरूप तापमान 500 K होता है।
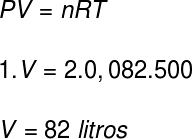
संकल्प के अनुसार, गैस का आयतन 82 लीटर है।
प्रश्न 2) एक आदर्श गैस का आयतन 20 l होता है, जब उस पर 3 atm का दबाव होता है, ताकि उसका तापमान स्थिर रहे, जबकि उसका आयतन तीन गुना हो। इस परिवर्तन से गुजरने के बाद इस गैस के अंतिम दबाव की गणना करें।
ए) 1 एटीएम
बी) 3 एटीएम
सी) 5 एटीएम
डी) 8 एटीएम
ई) 9 एटीएम
खाका: एक पत्र
संकल्प:
इस अभ्यास को हल करने के लिए, हम गैसों के सामान्य नियम का प्रयोग करेंगे, नोट:
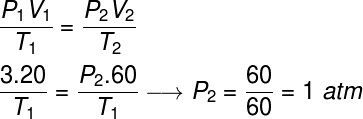
गणना करने के लिए, गैस को 60 लीटर की मात्रा निर्दिष्ट करना आवश्यक था, क्योंकि परिवर्तन के दौरान इसकी मात्रा तीन गुना हो गई थी।
राफेल हेलरब्रॉक द्वारा
भौतिक विज्ञान के अध्यापक