आयनीकरण एक रासायनिक प्रतिक्रिया है जो पानी में रखे आणविक पदार्थों से आयनों की उत्पत्ति करती है।
अतः हम कह सकते हैं कि आयनन इसकी प्रक्रियाआयन निर्माण.
अम्ल उन पदार्थों के उदाहरण हैं जो पानी में रखने पर आयनीकरण से गुजरते हैं।
आयनीकरण प्रक्रिया
निम्न उदाहरण के माध्यम से देखें कि आयनीकरण प्रक्रिया कैसे होती है:
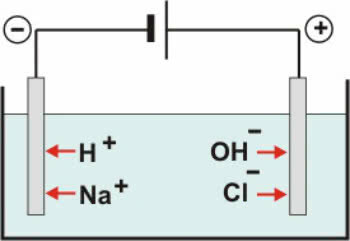
जब पानी में रखा जाता है, तो हाइड्रोक्लोरिक एसिड (HCl) आयनीकरण से गुजरता है। H और Cl के बीच रासायनिक बंधन टूट जाता है और H आयन बनते हैं+ और क्लू-जो पानी से घिरे हैं।
जैसा कि हमने देखा है, H+ एक इलेक्ट्रॉन और Cl. खो दिया- एक इलेक्ट्रॉन प्राप्त किया। हालांकि, एच+ इसे स्थिर करने की जरूरत है और इसलिए यह पानी से बांधता है।
इस प्रकार, एचसीएल आयनीकरण प्रतिक्रिया को निम्नानुसार भी दर्शाया जा सकता है:
अब हम हाइड्रोनियम धनायन (H .) के निर्माण का निरीक्षण करते हैं3हे+), H. के मिलन का परिणाम+ और H से2ओ
यह भी ध्यान रखना महत्वपूर्ण है कि इस उदाहरण में, Cl इलेक्ट्रॉन प्राप्त करता है क्योंकि यह सबसे अधिक है निद्युतअर्थात् इसमें इलेक्ट्रॉन ग्रहण करने की प्रवृत्ति होती है। इसलिए, यह आसानी से इलेक्ट्रॉनों को अपनी ओर आकर्षित करता है।
यह भी पढ़ें:
- इलेक्ट्रॉनों
- आयन, धनायन और आयन
- रासायनिक प्रतिक्रिया
अन्य आयनीकरण उदाहरण देखें:
1)
2)
आयनीकरण ऊर्जा या आयनीकरण क्षमता एक आवधिक संपत्ति है जो एक परमाणु से एक जमीनी अवस्था में एक इलेक्ट्रॉन को स्थानांतरित करने के लिए आवश्यक ऊर्जा की मात्रा को इंगित करती है।
हदबंदी और आयनीकरण
पृथक्करण यह एक भौतिक घटना है, रासायनिक प्रतिक्रिया नहीं। यह पानी में आयनिक यौगिकों से मौजूदा आयनों की रिहाई को संदर्भित करता है।
पृथक्करण और आयनीकरण के बीच मुख्य अंतर है:
- आयनीकरण: आयन बनते हैं;
- पृथक्करण: मौजूदा आयन अलग।
पृथक्करण प्रक्रिया केवल लवण और क्षार के साथ होती है। उदाहरण: NaCl, टेबल सॉल्ट।
रासायनिक प्रतिक्रियाओं के लिए पृथक्करण और आयनीकरण महत्वपूर्ण प्रक्रियाएं हैं, क्योंकि मुक्त आयन अणुओं की तुलना में अधिक प्रतिक्रियाशील होते हैं।
यह भी पढ़ें:
- एसिड
- लवण
- अड्डों
- आयनिक संतुलन
- पीएच और पीओएच की अवधारणा और निर्धारण
- निराकरण प्रतिक्रिया
टिप्पणी किए गए संकल्प के साथ, विषय पर प्रवेश परीक्षा के प्रश्नों की जांच करना सुनिश्चित करें: अकार्बनिक कार्यों पर अभ्यास.