का पृथक्करण अड्डों यह है एक शारीरिक प्रक्रिया यह अकार्बनिक पदार्थों के इस महत्वपूर्ण समूह के साथ होता है जब वे पानी में घुल जाते हैं, या जब वे संलयन प्रक्रिया से गुजरते हैं (ठोस अवस्था से तरल अवस्था में जाते हैं गरम करना)।
सामान्य तौर पर, की घटना आधार पृथक्करण यह उन धनायनों और आयनों की रिहाई है जो का निर्माण करते हैं आयनिक यौगिक, जो, इस मामले में, आधार है। तो, के दौरान आधार पृथक्करण, का रिलीज आयनों जो पहले से ही यौगिक में मौजूद है, यानी कोई नया आयन नहीं बनता है।
आधार किसी भी धातु (X) द्वारा बनता है, जो यौगिक का धनायन है, या अमोनियम धनायन (NH समूह) द्वारा4+), हाइड्रॉक्साइड आयन (OH समूह द्वारा दर्शाया गया) से बंधा हुआ है, जैसा कि नीचे दिए गए अभ्यावेदन में है:
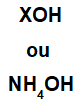
आधार सूत्र के सामान्य निरूपण
का रूप का प्रतिनिधित्व करते हैं आधार पृथक्करण यह एक समीकरण के माध्यम से किया जाता है जिसमें, अभिकारक में, हमारे पास आधार होता है और उत्पादों में, हमारे पास आयन (धनायन और आयन) होते हैं। क्या फर्क पड़ता है कि पृथक्करण कैसे होता है:
पानी में आधार का विघटन:
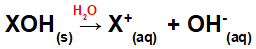
जलीय माध्यम में आधार के पृथक्करण का प्रतिनिधित्व करने वाला समीकरणation
आधार विलय द्वारा पृथक्करण:
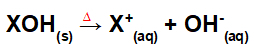
संलयन प्रक्रिया द्वारा आधार के पृथक्करण का प्रतिनिधित्व करने वाला समीकरण
उपरोक्त सामान्य समीकरणों का विश्लेषण करते हुए, हम सत्यापित करते हैं कि उन सभी में हमारे पास हमेशा आधार होगा, धनायन (जो धातु या NH समूह है)4+) और आयन (OH .)-). लेकिन क्या वे सब ऐसे ही हैं? क्या उनमें कोई अंतर नहीं है? पहले प्रश्न का उत्तर नहीं है और दूसरे प्रश्न का उत्तर हां है।
जब हम क्रियान्वित करते हैं आधार से पृथक्करण, आधार सूत्र का विश्लेषण करना सबसे पहले मौलिक है, क्योंकि, इससे हम. का भार निर्धारित कर सकते हैं धनायन और हाइड्रॉक्साइड आयनों की मोल मात्रा, क्योंकि धनायन की मोल मात्रा मानक है (हमेशा 1 मोल)।
यह याद रखने योग्य है कि आधार सूत्र में मौजूद OH समूहों की मात्रा, आधार के पृथक्करण में धनायन के आवेश और हाइड्रॉक्साइड आयन के mol में मात्रा निर्धारित करती है।
आइए एल्युमिनियम हाइड्रॉक्साइड के उदाहरण देखें [Al(OH)3] और गोल्ड हाइड्रॉक्साइड (AuOH)। एल्यूमीनियम आधार सूत्र में, तीन OH समूह होते हैं, और सोने के आधार सूत्र में, केवल एक OH समूह होता है। इस प्रकार, इन आधारों के पृथक्करण में, हमारे पास है:
अल (ओएच) हदबंदी3:
चूंकि इस आधार के सूत्र में तीन OH समूह हैं, धनायन पर आवेश +3 होगा और आयनों के मोल में मात्रा 3 mol के बराबर होगी, जैसा कि हम निम्नलिखित समीकरण में देख सकते हैं:
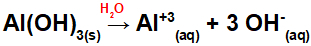
जलीय माध्यम में एल्युमिनियम बेस पृथक्करण समीकरण
AuOH से पृथक्करण:
चूंकि इस आधार के सूत्र में एक OH समूह है, धनायन पर आवेश +1 होगा और आयनों के मोल में मात्रा 1 mol के बराबर होगी, जैसा कि हम निम्नलिखित समीकरण में देख सकते हैं:
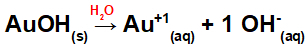
जलीय माध्यम में सोने के साथ आधार पृथक्करण का समीकरण
मेरे द्वारा। डिओगो लोपेज डायस
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-dissociacao-das-bases.htm
