ये पाठ जोड़ प्रतिक्रियाएं ने दिखाया कि इस प्रकार की कार्बनिक प्रतिक्रियाओं का नाम इस तरह रखा गया है क्योंकि कार्बन के बीच के बंधनों को तोड़कर कार्बनिक अणु में एक अभिकारक जोड़ा जाता है। इस पाठ में ऐल्कीनों का मामला दिखाया गया था, यहाँ हम पहले ही विचार करेंगे कि ऐल्कीनेस के साथ यह कैसे होता है, या अर्थात्, उन हाइड्रोकार्बन के साथ (केवल कार्बन और हाइड्रोजन परमाणुओं से बना होता है) जिनमें एक बंधन होता है तिगुना।
एल्काइन्स का सुभेद्य बिंदु बिल्कुल ट्रिपल बॉन्ड है, जहां पीआई (-) -टाइप बॉन्ड को तोड़ा जा सकता है (अतिरिक्त) आंशिक) या दो बार (कुल जोड़) और क्रमशः दोहरे (एल्किन्स) या एकल बांड वाले नए यौगिकों को जन्म देते हैं (अल्केन्स)।
आइए ऐल्काइनों में अतिरिक्त अभिक्रियाओं के मामलों को देखें:
1. हाइड्रोजन या हाइड्रोजनीकरण का जोड़:
इस मामले में, एच अणु2 एक उत्प्रेरक का उपयोग करके एल्काइन में जोड़ा जाता है, जो आमतौर पर पाउडर निकल (Ni), प्लैटिनम (Pt) या पैलेडियम (Pd) होता है। उत्प्रेरक का उपयोग करने की आवश्यकता के कारण, इस प्रतिक्रिया को भी कहा जाता है उत्प्रेरक हाइड्रोजनीकरण और यह चरणों में होता है: पहले चरण में आपको एक एल्केन मिलता है, और दूसरे चरण में, जो धीमा होता है, आपको एक अल्केन मिलता है।
यदि उपयोग किया जाने वाला उत्प्रेरक मजबूत है, जैसे निकल और प्लैटिनम, तो प्रतिक्रिया सीधे अल्केन उत्पन्न करती है। पैलेडियम बासो के साथ मिश्रित4 यह एक कमजोर उत्प्रेरक है और एल्कीन पैदा करता है। केवल एल्केन तक पहुंचने के लिए आंशिक उत्प्रेरक अवरोधक का उपयोग करना भी संभव है। यह प्रतिक्रिया उच्च दबाव और तापमान के तहत भी होती है।
इसके बाद, हमारे पास ईथेन में हाइड्रोजन का योग है, एथिलीन और फिर ईथेन का उत्पादन होता है:

2. हलोजन या हलोजन का जोड़:
एक एल्काइन पाई बंधन टूट जाता है और अणु में दो हलोजन परमाणु जुड़ जाते हैं (आवर्त सारणी के 17A परिवार के तत्व, सबसे अधिक इस्तेमाल किया जा रहा है: Cl2 और भाई2), एक विसाइनल डाइहैलाइड बनाता है, जिसका अर्थ है कि दो हैलोजन परमाणु पड़ोसी कार्बन परमाणुओं से बंधे होते हैं। प्रतिक्रिया जारी रह सकती है, अन्य पीआई बंधन को तोड़ना और अणु में दो और हलोजन परमाणु जोड़ना।
नीचे दिए गए उदाहरण में, हमारे पास रिश्वत के अतिरिक्त इस प्रकार है:
क्लोरीनसीएल क्लूक्लोरीन
││ ││
एच सी ≡ सी सीएच3 + क्लोरीन2 → एच सी ═ सी सीएच3 + क्लोरीन2 → एच सी ─ सी सीएच3
││
क्लोरीनक्लोरीन
ALCINO DI-HALETTE TETRAHALETTE
3. हाइड्रोजन हैलाइडों का योग (हैलोजनहाइड्राइड्स या हाइड्रोहैलोजनेशन):
यहां, एल्केनी में एक हाइड्रोजन हैलाइड जोड़ा जाता है, और आंशिक और कुल जोड़ भी हो सकता है। इस प्रकार की प्रतिक्रिया का एक महत्वपूर्ण पहलू यह है कि यह इस प्रकार है मार्कोवनिकोव का नियमयानी हाइड्रोजन अधिक हाइड्रोजनीकृत कार्बन (अधिक हाइड्रोजन परमाणुओं के साथ) को बांधता है और हैलोजन कम हाइड्रोजनीकृत कार्बन से बांधता है।
कुल हाइड्रोहैलोजेनेशन में, एक जेमिक डाइहैलाइड बनता है, यानी एक ऐसा यौगिक जिसमें दो हैलोजन परमाणु एक ही कार्बन से जुड़े होते हैं।
घड़ी:
एचब्र हूबीआर
││ ││
एच सी ≡ सी सीएच3 + एचबीआर → एच सी ═ सी सीएच3 + एचबीआर → एच सी ─ सी सीएच3
││
एचबीआर
ALCINO HALIDE GEMIC DI-HALOGIDE
इस प्रकार की प्रतिक्रिया का एक महत्वपूर्ण उदाहरण वह है जो तब होता है जब हाइड्रोजन क्लोराइड को एथीन में मिलाया जाता है, जिससे क्लोरोएथेन या विनाइल मोनोक्लोराइड, जो मोनोमर है जो पॉलीविनाइल क्लोराइड बहुलक बनाता है, जिसे इसके संक्षिप्त नाम से जाना जाता है परमवीर चक्र।
एचसीएलएचक्लोरीन
││ ││
एच सी ≡ सी एच + एचसीएल → एच सी ═ सी एच + एचसीएल → एच सी ─ सी एच
││
एचक्लोरीन
एथिनो क्लोरोएटेन 1,1-डाइक्लोरोएथेन
(पीवीसी मोनोमर)
पीवीसी उद्योग में व्यापक रूप से विभिन्न उत्पादों के निर्माण के लिए उपयोग किया जाता है, जैसे सैंडल, दवा की बोतलें, चिकित्सा उपकरण, बच्चों के लिए प्लास्टिक पैंट, बैग, तार कोटिंग्स, खिलौने, फर्नीचर असबाब, कार असबाब, रेनकोट, प्लास्टिक के जूते, विनाइल रिकॉर्ड, फर्श, पैकेजिंग फिल्म, पानी के पाइप में इस्तेमाल पाइप और सीवेज आदि
4. पानी का जोड़ (हाइड्रेशन):
इस प्रतिक्रिया में, पानी एल्केनी के साथ प्रतिक्रिया करता है, शुरू में एक एनोल बनाता है, जो एक आणविक पुनर्व्यवस्था से गुजरता है और एल्डिहाइड में बदल जाता है (ऐल्किनेस के मामले में एसिटिलीन से छोटा)। एनोल और एल्डिहाइड एल्डिहाइड प्रबलता के साथ गतिशील संतुलन में रहते हैं। यह मामला है डायनेमिक कॉन्स्टिट्यूकोनल आइसोमरी या टॉटोमेरी.
उदाहरण:

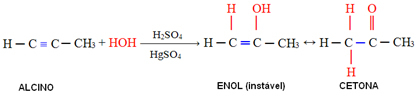
एसिटिलीन से बड़े एल्काइन्स के मामले में, मार्कोवनिकोव नियम का पालन किया जाता है और एनोल एक कीटोन को जन्म देता है:
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/quimica/reacoes-adicao-alcinos.htm
