यौगिकों के भौतिक और रासायनिक गुणों का विश्लेषण जो सहसंयोजक बंधन (इलेक्ट्रॉनों को साझा करके) करते हैं, हमें पता चलता है कि इन सामग्रियों के बीच बहुत अंतर हैं। लेकिन इससे पहले कि हम इन विशेषताओं को स्वयं देखें, आइए देखें कि आणविक और सहसंयोजक पदार्थों में क्या अंतर है।
पर आणविक पदार्थ वे वे हैं जो तब बनते हैं जब परमाणुओं को सहसंयोजक बंधों के माध्यम से जोड़ा जाता है, जिससे एक निर्धारित संख्या के अणु बनते हैं।
हालांकि, सहसंयोजक बंधन बहुत बड़ी और अनिश्चित संख्या में परमाणुओं के साथ एक नेटवर्क संरचना में यौगिकों की उत्पत्ति भी कर सकते हैं, जो हैं बड़े अणुओं. ऐसे पदार्थ कहलाते हैं सहसंयोजक यौगिक या सहसंयोजक नेटवर्क ठोस. इन यौगिकों के कुछ उदाहरण हैं: हीरा (C), ग्रेफाइट (C), सिलिकॉन डाइऑक्साइड (SiO .)2) और सिलिकॉन कार्बाइड (SiC)।
अब, आइए इसके मुख्य गुणों को देखें:
- कमरे के तापमान पर भौतिक अवस्था: परिवेशी परिस्थितियों में, आणविक और सहसंयोजक यौगिक पाए जाते हैं तीन भौतिक अवस्थाओं में (ठोस, द्रव और गैस)।
उदाहरण:
हे ठोस: चीनी (सुक्रोज), सिलिका (रेत), हीरा, ग्रेफाइट;
हे तरल: पानी, एसीटोन, इथेनॉल;
हे गैसीय: हाइड्रोजन सल्फाइड, क्लोरीन गैस, ब्रोमीन गैस, हाइड्रोजन गैस।

- गलनांक और क्वथनांक: सामान्य तौर पर, इन पदार्थों के गलनांक और क्वथनांक होते हैं आयनिक पदार्थों की तुलना में छोटा.
सहसंयोजक पदार्थों का क्वथनांक आणविक पदार्थों की तुलना में अधिक होता है, हमेशा 1000 ° C से ऊपर। इसका कारण यह है कि चूंकि उनके अणु क्रिस्टलीय जाली बनाने के लिए अधिक निकटता से जुड़े हुए हैं, इसलिए उन्हें अपनी स्थिति बदलने के लिए अधिक ऊर्जा प्रदान करना आवश्यक है।
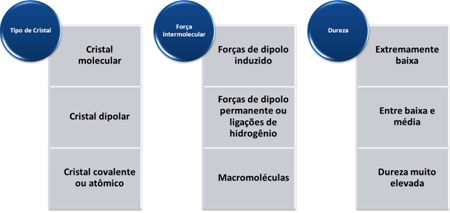
सहसंयोजक और आणविक यौगिकों के क्वथनांक और गलनांक में दो कारक हस्तक्षेप करते हैं: a अणु भार और यह अंतर-आणविक बल.
मोलर द्रव्यमान जितना अधिक होगा, अणु की जड़ता उतनी ही अधिक होगी और, परिणामस्वरूप, क्वथनांक और गलनांक जितना अधिक होगा। यदि दाढ़ द्रव्यमान का अनुमान लगाया जाता है, तो हम अंतर-आणविक बलों को देखते हैं। सबसे तीव्र अंतर-आणविक बल हाइड्रोजन बंधन का होता है, जिससे उच्च क्वथनांक और गलनांक होता है। मध्यवर्ती स्थायी द्विध्रुव है और सबसे कमजोर, जो कम क्वथनांक और गलनांक की ओर जाता है, प्रेरित द्विध्रुवीय है।
- विद्युत प्रवाह: अपने शुद्ध रूप में, तरल और ठोस दोनों विद्युत प्रवाह का संचालन नहीं करते हैं।
एक अपवाद ग्रेफाइट है, जो ठोस रूप में विद्युत प्रवाह का संचालन करता है, क्योंकि इसके दोहरे बंधन इलेक्ट्रॉन प्रतिध्वनित होते हैं और इसलिए एक निश्चित गतिशीलता होती है।
- घुलनशीलता: ध्रुव ध्रुवों में विलीन हो जाते हैं और अध्रुवीय अध्रुवीय में विलीन हो जाते हैं।
- तप: सहसंयोजक पदार्थों का प्रभाव या यांत्रिक आघात का प्रतिरोध कम होता है। सामान्य तौर पर, वे भंगुर ठोस होते हैं, जैसा कि कांच के मामले में दिखाया गया है, जो सोडियम और कैल्शियम सिलिकेट्स द्वारा बनता है।

- कठोरता: सामान्य तौर पर, उनके पास उच्च कठोरता होती है। ग्रेफाइट के अपवाद के साथ, क्योंकि इसके कार्बन परमाणु तीन अन्य कार्बन परमाणुओं से जुड़े होते हैं, कुछ गतिशीलता के साथ हेक्सागोनल प्लेट बनाते हैं, जिससे यह नरम हो जाता है। इस वजह से, इसका उपयोग स्नेहक के रूप में भी किया जाता है।
इन पदार्थों की कठोरता क्रिस्टल के प्रकार के अनुसार भिन्न होती है, जैसा कि नीचे दी गई तालिका में दिखाया गया है:
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/quimica/propriedades-dos-compostos-covalentes-moleculares.htm

