ऑक्सीकरण और यह कमी प्रतिक्रियाएँ होती हैं जो तब होती हैं जब a. होता है इलेक्ट्रॉन स्थानांतरण रासायनिक प्रजातियों के बीच वे विपरीत प्रतिक्रियाएं हैं: ऑक्सीकरण में इलेक्ट्रॉनों का नुकसान होता है और कमी में इलेक्ट्रॉनों का लाभ होता है।
ये प्रक्रियाएं एक साथ होती हैं, क्योंकि जब कोई पदार्थ दूसरे को इलेक्ट्रॉनों का दान करता है तो उसका ऑक्सीकरण होता है, जबकि इलेक्ट्रॉनों को प्राप्त करने वाले पदार्थ में कमी आती है।
जब कोई पदार्थ ऑक्सीकरण करता है, तो यह अन्य प्रजातियों को कम करने का कारण बनता है, इसलिए एक कम करने वाले एजेंट का नाम। इसी तरह, एक पदार्थ दूसरे के ऑक्सीकरण के कारण कम हो जाता है और इसलिए ऑक्सीकरण एजेंट होता है।
ऑक्सीकरण और कमी प्रतिक्रियाओं को शामिल प्रजातियों के ऑक्सीकरण संख्या (एनओएक्स) की भिन्नता द्वारा प्रदर्शित किया जाता है।
आम तौर पर, एक प्रतिक्रिया जो ऑक्सीकरण और कमी को प्रस्तुत करती है उसे निम्न द्वारा दर्शाया जा सकता है:
ए + बी+ → ए+ + बी
कहाँ पे,
ए: पदार्थ जो ऑक्सीकृत होता है, इलेक्ट्रॉनों को खो देता है, उसका मूल्य बढ़ाता है और कम करने वाला एजेंट होता है।
B: पदार्थ जो अपचयन से गुजरता है, इलेक्ट्रॉनों को ग्रहण करता है, ऑक्सीकरण को कम करता है और ऑक्सीकारक है।
ऑक्सीकरण और कमी के उदाहरण
रेडॉक्स रासायनिक समीकरण के उदाहरण के लिए निम्न छवि देखें।
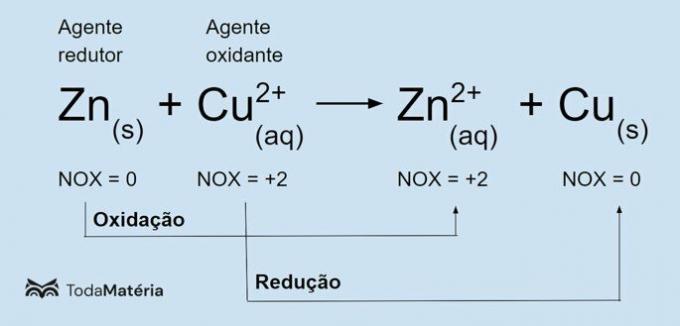
धात्विक जस्ता से गुजरता है ऑक्सीकरण और तांबे की कमी का कारण बनता है, इसलिए यह कम करने वाला एजेंट है। इसकी ऑक्सीकरण संख्या (nox) 0 से बढ़कर +2 हो जाती है क्योंकि यह 2 इलेक्ट्रॉनों को खो देता है।
कप्रिक आयन (Cu2+) अपचयन से गुजरता है और तांबे को ऑक्सीकरण का कारण बनता है, इसलिए यह ऑक्सीकरण एजेंट है। इसकी ऑक्सीकरण संख्या (nox) +2 से घटकर 0 हो जाती है क्योंकि यह 2 इलेक्ट्रॉनों को प्राप्त करता है और धात्विक तांबा बन जाता है, जो विद्युत रूप से तटस्थ होता है।
रोजमर्रा की जिंदगी में रेडॉक्स प्रतिक्रियाओं के अन्य उदाहरण हैं:
मीथेन दहन
चौधरी4(जी) + 2O2(जी) → सीओ2(जी) + 2H2हे(वी)
प्रकाश संश्लेषण
6सीओ2(जी) + 6H2हे(वी) → सी6एच12हे6 (यहां) + 6O2(जी)
लोहे का क्षरण
2Fe(एस) + 3/4O2(जी) + 3 घंटे2हे(वी) → 2Fe (OH)3(रों) (जंग Fe2हे3.3H2ओ)
के बारे में अधिक जानने ऑक्सीकरण संख्या (nox).
ऑक्सीकरण और कमी प्रतिक्रियाएं कैसे होती हैं?
तांबे और जस्ता से युक्त रेडॉक्स प्रतिक्रिया के समीकरण को अर्ध-प्रतिक्रियाओं द्वारा दर्शाया जा सकता है, जैसा कि नीचे दिखाया गया है।
- ऑक्सीकरण अर्ध-प्रतिक्रिया: Zn0(एस) → 2e- + Zn2+(यहां)
- अर्ध-प्रतिक्रिया में कमी: ass2+(यहां) + 2e- → गधा0(एस)
- वैश्विक समीकरण: Zn0(एस) + गधा2+(यहां) → जेडएन2+(यहां) + गधा0(एस)
रेडॉक्स प्रतिक्रिया में यह इलेक्ट्रॉन स्थानांतरण शामिल प्रजातियों की कमी क्षमता के अनुसार होता है। सबसे कम कमी क्षमता वाले घटक में इलेक्ट्रॉनों को दान करने की प्रवृत्ति होती है, जबकि उच्चतम क्षमता वाला घटक उन्हें प्राप्त करेगा।
उदाहरण के लिए, जस्ता की कमी क्षमता -0.76V है, जबकि तांबे की कमी क्षमता +0.34V है। इसलिए, जस्ता, क्योंकि इसमें कम कमी की क्षमता है, एक बेहतर कम करने वाला एजेंट है और कमी को बढ़ावा देता है तांबा, जिसमें उच्च कमी क्षमता होती है और इसलिए, इलेक्ट्रॉनों को प्राप्त करता है और जस्ता ऑक्सीकरण का कारण बनता है।
इसके बारे में भी पढ़ें रेडॉक्स प्रतिक्रियाएं.
ऑक्सीकरण और अपचयन पर व्यायाम
इस पाठ में आपने जो सीखा है, उसके बारे में अपने ज्ञान का परीक्षण करने के लिए निम्नलिखित प्रश्नों का उपयोग करें।
प्रश्न 1
ऑक्सीकरण और कमी प्रतिक्रियाओं के संबंध में, यह कहना सही है कि
a) रासायनिक प्रजातियों के नक्स में वृद्धि इंगित करती है कि इसमें कमी आई है।
b) जो पदार्थ इलेक्ट्रॉनों को खोता है वह ऑक्सीकरण से गुजरता है और एक ऑक्सीकरण एजेंट है।
c) रेडॉक्स प्रतिक्रियाओं में, इलेक्ट्रॉनों को स्थानांतरित किया जाता है।
d) जो पदार्थ इलेक्ट्रॉन ग्रहण करता है वह अपचयित होता है और अपचायक होता है।
ई) रासायनिक प्रजातियों के नॉक्स में कमी इंगित करती है कि इसका ऑक्सीकरण हो गया है।
सही विकल्प: c) ऑक्सीकरण-अपचयन प्रतिक्रियाओं में, इलेक्ट्रॉन स्थानांतरण होता है।
रेडॉक्स प्रतिक्रियाओं में, इलेक्ट्रॉनों को स्थानांतरित किया जाता है।
जो पदार्थ इलेक्ट्रॉन ग्रहण करता है वह अपचयन से गुजरता है और ऑक्सीकारक है। रासायनिक प्रजातियों के नॉक्स में कमी यह इंगित करती है कि यह कम हो गया है।
जो पदार्थ इलेक्ट्रॉनों को खोता है वह ऑक्सीकरण से गुजरता है और एक कम करने वाला एजेंट है। रासायनिक प्रजातियों के नॉक्स में वृद्धि इंगित करती है कि इसका ऑक्सीकरण हुआ है।
प्रश्न 2
दैनिक जीवन में रेडॉक्स प्रतिक्रियाओं के उदाहरण सिवाय
ए) जंग
बी) दहन
ग) प्रकाश संश्लेषण
डी) तटस्थता
गलत विकल्प: डी) तटस्थता।
एक उदासीनीकरण प्रतिक्रिया वह होती है जो एक एसिड और एक आधार के बीच होती है, जिसके परिणामस्वरूप नमक और पानी होता है। उदाहरण के लिए:
NaOH + HCl → NaCl + H2हे
रेडॉक्स प्रतिक्रिया के उदाहरण हैं:
मीथेन दहन
चौधरी4(जी) + 2O2(जी) → सीओ2(जी) + 2H2हे(वी)
प्रकाश संश्लेषण
6सीओ2(जी) + 6H2हे(वी) → सी6एच12हे6 (यहां) + 6O2(जी)
लोहे का क्षरण
2Fe(एस) + 3/4O2(जी) + 3 घंटे2हे(वी) → 2Fe (OH)3(रों)
प्रश्न 3
निम्नलिखित ऑक्सीकरण-कमी प्रतिक्रियाओं का निरीक्षण करें और इंगित करें कि ऑक्सीकरण और कम करने वाले एजेंट कौन से हैं।
मैं। Zn0(एस) + गधा2+(यहां) → जेडएन2+(यहां) + गधा0(एस)
द्वितीय. नितंब2+(यहां) + एच2(जी) → 2H+(यहां) + गधा(एस)
III. Zn(एस) + 2H+(यहां) → जेडएन2+(यहां) + एच2(जी)
जवाब:
एक रेडॉक्स प्रतिक्रिया में, ऑक्सीकरण से गुजरने वाला एक कम करने वाला एजेंट होता है और जो कम होने वाला होता है वह ऑक्सीकरण एजेंट होता है।
मैं। Zn0(एस) + गधा2+(यहां) → जेडएन2+(यहां) + गधा0(एस)
ऑक्सीकरण एजेंट: कॉपर (Cu)
कम करने वाला एजेंट: जिंक (Zn)
द्वितीय. नितंब2+(यहां) + एच2(जी) → 2H+(यहां) + गधा(एस)
ऑक्सीकरण एजेंट: कॉपर (Cu)
कम करने वाला एजेंट: हाइड्रोजन (एच)
III. Zn(एस) + 2H+(यहां) → जेडएन2+(यहां) + एच2(जी)
ऑक्सीकरण एजेंट: हाइड्रोजन (एच)
कम करने वाला एजेंट: जिंक (Zn)
सामग्री के साथ अधिक ज्ञान प्राप्त करें:
- ढेर क्या हैं?
- विद्युत रसायन
- इलेक्ट्रोलीज़
ग्रंथ सूची संदर्भ
फोन्सेका, एम. आर। एम रसायन, 2. 1. ईडी। साओ पाउलो: एटिका, 2013।
सैंटोस, डब्ल्यूएलपी; एमओएल, जी.एस. नागरिक रसायन शास्त्र, 3. 2. ईडी। साओ पाउलो: एडिटोरा एजेएस, 2013।
यूएसबीईआरसीओ, जे. कनेक्ट केमिस्ट्री, 2: केमिस्ट्री। - 2. ईडी। साओ पाउलो: सारावा, 2014।