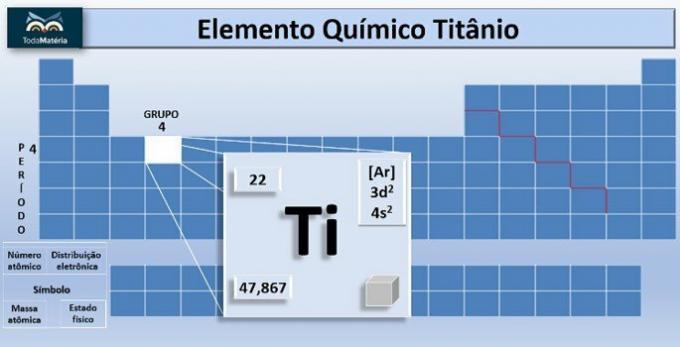
हे टाइटेनियम एक रासायनिक तत्व है जिसका प्रतीक Ti और परमाणु क्रमांक है, यानी प्रोटॉन की संख्या 22 के बराबर है। यह धातु आवर्त सारणी के समूह 4 और 4 में स्थित है।
तत्व का परमाणु द्रव्यमान 47.867 u है, और क्योंकि परमाणु के इलेक्ट्रॉनों में इसके 22 इलेक्ट्रॉन हैं, इसका इलेक्ट्रॉन वितरण 1s है2 2s2 2पी6 3एस2 3पी6 4एस2 3डी2.
टाइटेनियम में कई अनुप्रयोगों के लिए वांछनीय गुण हैं क्योंकि यह स्टील जितना मजबूत और बहुत हल्का है।
क्योंकि यह एक नमनीय, दुर्दम्य, संक्षारण प्रतिरोधी धातु है, यह यांत्रिक प्रतिरोध प्रस्तुत करता है, थर्मल स्थिरता और कम प्रतिक्रियाशीलता, इसे धातु मिश्र धातुओं में जोड़ा जाता है ताकि उनके पास उच्च प्रदर्शन। इसकी जैव अनुकूलता और गैर-विषाक्तता भी इसे अस्थि कृत्रिम अंग बनाने के लिए उपयोगी बनाती है।
टाइटेनियम की मुख्य विशेषताएं हैं:
- गलनांक: 1668 डिग्री सेल्सियस
- क्वथनांक: 3287 °C
- घनत्व: 4.5 ग्राम/सेमी3
- रंग: सिल्वर ग्रे
- 20 डिग्री सेल्सियस पर भौतिक अवस्था: ठोस
- समस्थानिक: Ti46, तुम47, तुम48, तुम49 और तुम50
इस रासायनिक तत्व की खोज अंग्रेज विलियम ग्रेगोर ने 1791 में की थी और इसका नाम ग्रीक से लिया गया है टाइटन्स, बाद में मार्टिन हेनरिक क्लैप्रोथ द्वारा जिम्मेदार ठहराया गया था।
टाइटेनियम ग्रह पर नौवां सबसे प्रचुर तत्व है और यह पृथ्वी की पपड़ी में रूटाइल (TiO) जैसे अयस्कों में पाया जाता है।2) और इल्मेनाइट (FeTiO .)3). इसलिए, इस धातु को प्राप्त करने का मुख्य तरीका खनन है।
टाइटेनियम का उपयोग किसके लिए किया जाता है?
क्योंकि यह कमरे के तापमान पर रासायनिक रूप से अक्रियाशील है, आसानी से ढाला जाता है, इसमें उच्च यांत्रिक और संक्षारण प्रतिरोध होता है, टाइटेनियम का उपयोग एक रणनीतिक धातु के रूप में किया जाता है।
विमानन और एयरोस्पेस उद्योग टरबाइन और धड़ घटकों जैसे भागों के उत्पादन के लिए टाइटेनियम के मुख्य उपयोगकर्ता हैं। अन्य अनुप्रयोग दंत कृत्रिम अंग, शल्य प्रत्यारोपण और गहनों का निर्माण कर रहे हैं।
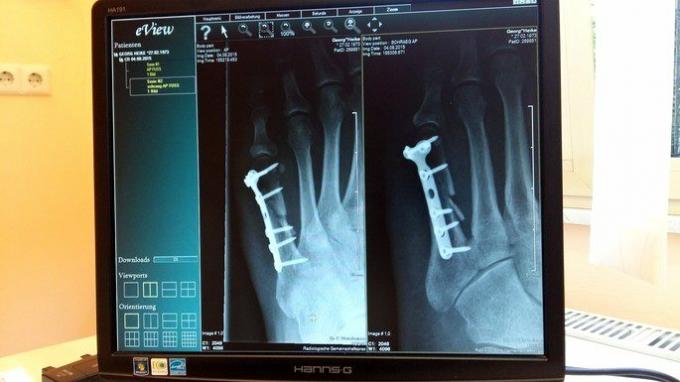
चिकित्सा में, टाइटेनियम मानव ऊतकों, हल्कापन और ताकत के साथ इसकी संगतता के कारण बहुत उपयोगी है। इसका उपयोग शरीर के अंगों के लिए प्रत्यारोपण के उत्पादन के लिए किया जाता है, जैसे कि फिक्सेशन स्क्रू, घुटने के जोड़ को बदलना, ह्यूमरस प्रोस्थेसिस, हिप प्रोस्थेसिस, अन्य।
टाइटेनियम डाइऑक्साइड (TiO)2) इस तत्व के मुख्य यौगिकों में से एक है, जिसका उपयोग विरंजन एजेंट के रूप में किया जा रहा है। आम तौर पर, उच्च गुणवत्ता वाली सफेद स्याही रंग और चमक के दृश्य स्वरूप को बेहतर बनाने के लिए इसका उपयोग करती है। अन्य उत्पाद, जैसे टूथपेस्ट और सनस्क्रीन, भी रंगद्रव्य का उपयोग करते हैं। डेयरी उत्पादों, मिठाइयों और पेय पदार्थों में मिलाए जाने वाले खाद्य रंग के रूप में भी उपयोग किया जाता है।
वास्तुकला में, हम उत्तरी स्पेन के बिलबाओ में गुगेनहाइम संग्रहालय में घुमावदार संरचनाओं को कवर करने के लिए टाइटेनियम के उपयोग को देख सकते हैं।

रोजमर्रा की जिंदगी में हम ऐसे कई उत्पाद पा सकते हैं जिनकी संरचना में टाइटेनियम है, जैसे साइकिल फ्रेम, चश्मा और टेनिस रैकेट।
रासायनिक उद्योग में, टाइटेनियम का उपयोग प्रतिक्रियाओं के लिए उत्प्रेरक के रूप में किया जाता है। इस तरह, यह प्रतिक्रिया की गति को नियंत्रित करना और पदार्थों की संरचना को प्रभावित किए बिना उत्पाद निर्माण के समय को कम करना संभव बनाता है।
ऑटोमोबाइल उद्योग ने कारों के निर्माण में उनके द्रव्यमान को कम करने और इस प्रकार, ईंधन की खपत को कम करने और उनके त्वरण को बढ़ाने के लिए टाइटेनियम के समावेश का अध्ययन किया है।
सामग्री के साथ अधिक ज्ञान प्राप्त करें:
- रासायनिक तत्व
- आवर्त सारणी
- धातु क्या हैं?
ग्रंथ सूची संदर्भ
एटकिंस, पी.डब्ल्यू.; जोन्स, एल. रसायन विज्ञान के सिद्धांत: आधुनिक जीवन और पर्यावरण पर सवाल उठाना। 3.ईडी. पोर्टो एलेग्रे: बुकमैन, 2006।
फेल्ट्रे, आर. रसायन विज्ञान के मूल सिद्धांत: वॉल्यूम। एक। चौथा संस्करण। साओ पाउलो: मॉडर्न, 2005।
ली, जे. डी। इतना संक्षिप्त अकार्बनिक रसायन नहीं। 5वें संस्करण का अनुवाद। अंग्रेज़ी। प्रकाशक एडगार्ड ब्लूचर लिमिटेड 1999.