रासायनिक समरूपता एक ऐसी घटना है जो तब देखी जाती है जब दो या दो से अधिक कार्बनिक पदार्थों का आणविक सूत्र समान होता है, लेकिन विभिन्न आणविक संरचना और गुण होते हैं।
इन विशेषताओं वाले रासायनिक पदार्थों को आइसोमर कहा जाता है।
यह शब्द ग्रीक शब्दों से लिया गया है आईएसओ = बराबर और मात्र = भाग, अर्थात् समान भाग।
विभिन्न प्रकार के आइसोमेरिज्म हैं:
- समतल समावयवी: यौगिकों की पहचान समतल संरचनात्मक सूत्रों द्वारा की जाती है। इसे चेन आइसोमेरिज्म, फंक्शन आइसोमेरिज्म, पोजिशन आइसोमेरिज्म, मुआवजा आइसोमेरिज्म और टॉटोमेरिज्म आइसोमेरिज्म में बांटा गया है।
- अंतरिक्ष समावयवी: यौगिकों की आणविक संरचना में विभिन्न स्थानिक संरचनाएं होती हैं। यह ज्यामितीय और ऑप्टिकल समरूपता में विभाजित है।
समतल समावयवी
पर समतल समावयवता या संवैधानिक समरूपता, कार्बनिक पदार्थों की आणविक संरचना समतल होती है।
इस विशेषता को प्रदर्शित करने वाले यौगिकों को समतल समावयवी कहा जाता है।
श्रृंखला समावयवी is
चेन आइसोमेरिज्म तब होता है जब कार्बन परमाणुओं में अलग-अलग चेन और एक ही रासायनिक कार्य होता है।
उदाहरण:
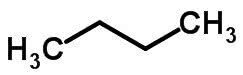
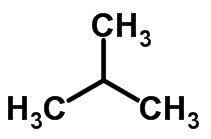
फंक्शन आइसोमेरिज्म
फ़ंक्शन आइसोमेरिज़्म तब होता है जब दो या दो से अधिक यौगिकों के अलग-अलग रासायनिक कार्य होते हैं और एक ही आणविक सूत्र होता है।
उदाहरण: यह मामला एल्डिहाइड और कीटोन्स के बीच सामान्य है।
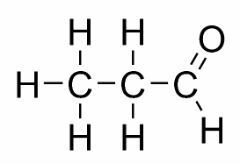
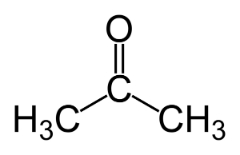
स्थिति आइसोमर
स्थिति समरूपता तब होती है जब यौगिकों को कार्बन श्रृंखला में विभिन्न असंतृप्ति, शाखाओं या कार्यात्मक समूह स्थितियों द्वारा विभेदित किया जाता है। इस मामले में, आइसोमर्स का एक ही रासायनिक कार्य होता है।
उदाहरण:

ऑफसेटिंग आइसोमर
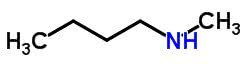
मुआवजा समरूपता या मेटामेरिज्म समान रासायनिक कार्य वाले यौगिकों में होता है जो हेटेरोएटम की स्थिति से भिन्न होता है।
उदाहरण:

टॉटोमेरी
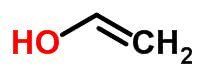
टॉटोमेरिज्म या डायनेमिक आइसोमेरिज्म को फंक्शन आइसोमेरिज्म का एक विशिष्ट मामला माना जा सकता है। इस मामले में, श्रृंखला में एक तत्व की स्थिति को बदलकर एक आइसोमर दूसरे में बदल सकता है।
उदाहरण:

अंतरिक्ष समावयवी
अंतरिक्ष समरूपता, जिसे स्टीरियोइसोमेरिज्म भी कहा जाता है, तब होता है जब दो यौगिकों का एक ही आणविक सूत्र और विभिन्न संरचनात्मक सूत्र होते हैं।
इस प्रकार के समावयवता में, परमाणु समान रूप से वितरित होते हैं, लेकिन अंतरिक्ष में विभिन्न पदों पर कब्जा कर लेते हैं।
ज्यामितीय समावयवी
ज्यामितीय समावयवता या सीआईएस-ट्रांस असंतृप्त खुली श्रृंखलाओं में और चक्रीय यौगिकों में भी होता है। ऐसा करने के लिए, कार्बन लिगेंड अलग होना चाहिए।

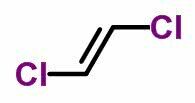
- जब समान लिगैंड एक ही तरफ होते हैं, तो आइसोमर नामकरण उपसर्ग प्राप्त करता है सीआईएस.
- जब समान लिगैंड विपरीत पक्षों पर होते हैं, तो नामकरण उपसर्ग प्राप्त करता है ट्रांस.
IUPAC (इंटरनेशनल यूनियन ऑफ प्योर एंड एप्लाइड कैमिस्ट्री) अनुशंसा करता है कि सीआईएस और ट्रांस के बजाय, जेड और ई अक्षरों को उपसर्ग के रूप में इस्तेमाल किया जाए।
ऐसा इसलिए है क्योंकि Z जर्मन शब्द का पहला अक्षर है ज़ुसममेन, जिसका अर्थ है "एक साथ"। और यह जर्मन शब्द का पहला अक्षर है एंटेजेन, जिसका अर्थ है "विपरीत"।
ऑप्टिकल आइसोमर
ऑप्टिकल आइसोमेरिज्म वैकल्पिक रूप से सक्रिय यौगिकों द्वारा प्रदर्शित किया जाता है। यह तब होता है जब कोई पदार्थ ध्रुवीकृत प्रकाश के तल में कोणीय विचलन के कारण होता है।
- जब कोई पदार्थ प्रकाशीय प्रकाश को दायीं ओर मोड़ता है तो उसे कहते हैं दांए हाथ से काम करने वाला.
- जब कोई पदार्थ प्रकाशीय प्रकाश को बाईं ओर मोड़ता है, तो पदार्थ कहलाता है लीवरोट्री.
एक पदार्थ दो रूपों में भी मौजूद हो सकता है जो वैकल्पिक रूप से सक्रिय हैं, डेक्सटोगाइरा और लेवोगाइरा। इस मामले में, इसे कहा जाता है एनैन्टीओमर.
वैकल्पिक रूप से सक्रिय होने के लिए कार्बन यौगिक के लिए, यह चिरल होना चाहिए। इसका मतलब यह है कि उनके लिगैंड असममित होने के कारण ओवरलैप नहीं कर सकते हैं।
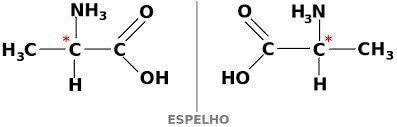
बदले में, यदि एक यौगिक में समान भागों में डेक्सट्रोगाइरा और लेवोरोटरी रूप होते हैं, तो उन्हें कहा जाता है नस्लीय मिश्रण. रेसमिक मिश्रण की ऑप्टिकल गतिविधि निष्क्रिय है।
यह भी पढ़ें:
- कार्बन
- कार्बनिक रसायन विज्ञान
- आण्विक सूत्र
- संरचनात्मक सूत्र
अभ्यास
1. (मैकेंज़ी 2012) संख्या कॉलम बी, जिसमें कार्बनिक यौगिक होते हैं, उन्हें कॉलम ए के साथ जोड़ते हैं, प्रत्येक कार्बनिक अणु प्रस्तुत करने वाले आइसोमेरिज्म के प्रकार के अनुसार।
कॉलम ए
1. ऑफसेटिंग आइसोमर
2. ज्यामितीय समावयवी
3. श्रृंखला समावयवी is
4. ऑप्टिकल आइसोमर
कॉलम बी
( ) साइक्लोप्रोपेन
( ) एथॉक्सी-इथेन
( ) ब्रोमो-क्लोरो-फ्लोरो-मीथेन
( ) 1,2-डाइक्लोरो-एथेन
कॉलम B में ऊपर से नीचे तक संख्याओं का सही क्रम है
ए) 2 - 1 - 4 - 3।
बी) 3 - 1 - 4 - 2।
ग) 1 - 2 - 3 - 4।
घ) ३ - ४ - १ - २.
ई) 4 - 1 - 3 - 2।
वैकल्पिक ख) ३ - १ - ४ - २.
2. (उर्ज) आइसोमरी वह घटना है जो इस तथ्य की विशेषता है कि एक ही आणविक सूत्र विभिन्न संरचनाओं का प्रतिनिधित्व करता है।
आणविक सूत्र C. के लिए समतल संरचनात्मक समरूपता को ध्यान में रखते हुए4एच8, हम निम्नलिखित प्रकार के समावयवों की पहचान कर सकते हैं:
ए) श्रृंखला और स्थिति
बी) श्रृंखला और कार्य
ग) कार्य और मुआवजा
डी) स्थिति और मुआवजा
वैकल्पिक ए) स्ट्रिंग और स्थिति
3. (OSEC) प्रोपेनोन और आइसोप्रोपेनॉल आइसोमेरिज़्म के एक मामले का उदाहरण देते हैं:
ए) मेटामेरिया का
बी) समारोह का
सी) टॉटोमरी का
डी) सीआईएस-ट्रान
ई) श्रृंखला
वैकल्पिक ग) तनातनी का
यह भी देखें: समतल समावयवता पर व्यायाम
