प्रयोग रसायन विज्ञान में अध्ययन की गई अवधारणाओं के बारे में अपने ज्ञान को सीखने और परीक्षण करने का एक व्यावहारिक तरीका है।
अपनी पढ़ाई को पूरा करने के लिए इन रासायनिक प्रयोगों का लाभ उठाएं, जो घर पर (वयस्कों की देखरेख में) किए जा सकते हैं या शिक्षक के साथ कक्षा में काम कर सकते हैं।
पहला अनुभव - रंगों को सुलझाना
शामिल अवधारणाएं: क्रोमैटोग्राफी और मिश्रणों का पृथक्करण
सामग्री
- विभिन्न रंगों के पेन (चिह्नित मार्कर)
- शराब
- कॉफी फिल्टर पेपर
- कप (प्रयोग की निगरानी की सुविधा के लिए गिलास)
कैसे बनाना है
- फिल्टर पेपर की कैंची और कट स्ट्रिप्स का प्रयोग करें। उपयोग किए गए प्रत्येक पेन के लिए एक आयत बनाएं।
- अब, आधार से लगभग 2 सेमी की दूरी पर, अपने चुने हुए रंग के पेन से एक वृत्त बनाएं और अंदर की तरफ पेंट करें।
- एक समर्थन पर खींचे गए संगमरमर से कागज के किनारे को सबसे दूर गोंद करें। इसके लिए आप एक टेप का उपयोग कर सकते हैं और इसे एक पेंसिल से जोड़ सकते हैं।
- कप में अल्कोहल डालें, बहुत ज्यादा नहीं, क्योंकि यह सिर्फ पेन के निशान के पास कागज के सिरे को छूना चाहिए।
- कागज को कप में रखें ताकि वह लंबवत हो। इसका समर्थन करने वाली पेंसिल किनारों पर टिकी होनी चाहिए।
- 10 से 15 मिनट तक प्रतीक्षा करें जब तक कि फिल्टर पेपर से अल्कोहल ऊपर न उठ जाए। उसके बाद, कागजों को हटा दें और उन्हें सूखने दें।
परिणाम
जब अल्कोहल पेन के निशान से होकर गुजरता है, तो यह रंग के घटकों के साथ इंटरैक्ट करता है और उन्हें पूरे कागज पर ले जाता है। इस प्रकार, विभिन्न वर्णक अल्कोहल के संपर्क में आने से अलग हो जाएंगे।
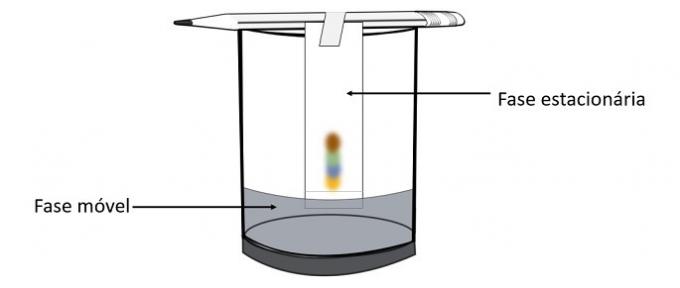
इस प्रयोग से यह पता लगाया जा सकता है कि पेन का रंग बनाने के लिए किन रंगों को मिलाया गया था।
व्याख्या
क्रोमैटोग्राफी मिश्रण को अलग करने की एक प्रकार की प्रक्रिया है। फिल्टर पेपर स्थिर चरण है और अल्कोहल मोबाइल चरण है जो स्थिर चरण से गुजरते समय मिश्रण के घटकों को खींच लेता है। इस प्रक्रिया में, अल्कोहल के साथ अधिक से अधिक संपर्क, विलायक के पारित होने के साथ वर्णक तेजी से आगे बढ़ेगा।
सामग्री के घटक, क्योंकि उनके पास अलग-अलग गुण हैं, मोबाइल चरण के साथ बातचीत करेंगे अलग-अलग तरीकों से, जिसे स्थिर चरण में अलग-अलग ड्रैग टाइम द्वारा देखा जा सकता है।
के बारे में अधिक जानने क्रोमैटोग्राफी.
दूसरा अनुभव - खाद्य संरक्षण
शामिल अवधारणाएं: कार्बनिक यौगिक और रासायनिक प्रतिक्रियाएं
सामग्री
- सेब, केला या नाशपाती
- नींबू या संतरे का रस
- विटामिन सी की गोली
कैसे बनाना है
- तीन फलों में से किसी एक को चुनें और इसे 3 बराबर भागों में काट लें।
- पहला टुकड़ा दूसरों के साथ तुलना के रूप में काम करेगा। इसलिए इसमें कुछ भी न मिलाएं, बस इसे हवा में खुला छोड़ दें।
- टुकड़ों में से एक में, नींबू या संतरे की सामग्री डालें। फैलाएं ताकि फल के अंदर का पूरा भाग रस से ढक जाए।
- अंतिम भाग में विटामिन सी फैलाएं, यह एक कुचल गोली हो सकती है, पूरे फलों के गूदे पर।
- देखें कि क्या होता है और परिणामों की तुलना करें।
परिणाम
हवा के संपर्क में आने वाले फल का गूदा जल्दी काला हो जाना चाहिए। नींबू या संतरे का रस और विटामिन सी, एस्कॉर्बिक एसिड नामक एक रसायन, फल के भूरे होने को धीमा कर देना चाहिए।

व्याख्या
जब हम किसी फल को काटते हैं, तो उसकी कोशिकाएं क्षतिग्रस्त हो जाती हैं, जिससे पॉलीफेनोल ऑक्सीडेज जैसे एंजाइम निकलते हैं, जो कि हवा के संपर्क में आने से भोजन में मौजूद फेनोलिक यौगिक ऑक्सीकृत हो जाते हैं और एंजाइमी ब्राउनिंग का कारण बनते हैं।
ऑक्सीजन की क्रिया को रोकने के लिए, एस्कॉर्बिक एसिड जैसे परिरक्षकों का उपयोग किया जाता है क्योंकि वे फेनोलिक यौगिकों के स्थान पर अधिमान्य रूप से ऑक्सीकृत होते हैं। प्रयोग में सुझाई गई साइट्रस, नींबू और संतरे जैसे प्राकृतिक स्रोतों में विटामिन सी टैबलेट के अलावा एस्कॉर्बिक एसिड भी मौजूद होता है।
के बारे में अधिक जानने ऑक्सीकरण.
तीसरा अनुभव - कौन तेजी से जमता है?
शामिल अवधारणाएं: संयुग्मन गुण और क्रायोस्कोपी
सामग्री
- दो ट्यूब (पार्टी के पक्ष में प्रयुक्त)
- कांच का प्याला
- टेबल नमक
- छना हुआ पानी
- बर्फ
- थर्मामीटर
कैसे बनाना है
- दोनों नलियों में समान मात्रा में छना हुआ पानी डालें। उदाहरण के लिए, प्रत्येक ट्यूब में 5 एमएल।
- किसी एक ट्यूब में टेबल सॉल्ट डालें और एक पहचान टेप लगाएं जिससे पता चल सके कि कौन सा नमकीन है।
- कांच के कंटेनर में कुटी हुई बर्फ भरें और थोड़ा नमक डालें।
- दो ट्यूबों को एक साथ बर्फ में रखें और देखें कि क्या होता है।
- प्रत्येक स्थिति के लिए ठंडे तापमान को रिकॉर्ड करें।
परिणाम
पानी में विलेय मिलाने से जमने वाला तापमान कम हो जाता है। इसलिए, समान परिस्थितियों के संपर्क में आने पर सादा पानी नमक और पानी के घोल की तुलना में बहुत तेजी से जम जाता है।
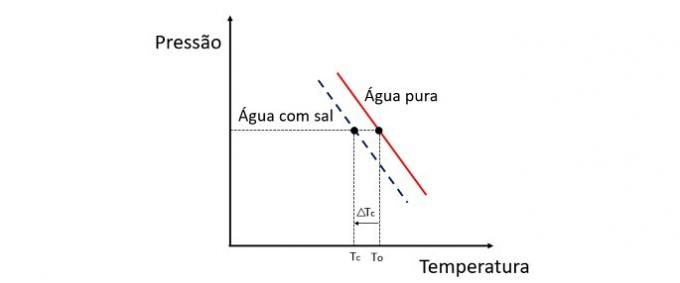
व्याख्या
क्रायोस्कोपी एक संपार्श्विक गुण है जो एक विलायक के तापमान में भिन्नता का अध्ययन करता है जब इसमें विभिन्न मात्रा में विलेय घुल जाते हैं।
पानी का जमने का तापमान कम होना एक गैर-वाष्पशील विलेय के कारण होता है और इस घटना के कई व्यावहारिक अनुप्रयोग हैं। इसलिए, घोल में विलेय की सांद्रता जितनी अधिक होगी, क्रायोस्कोपिक प्रभाव प्रभावित होगा।
यदि, उदाहरण के लिए, पानी 0 डिग्री सेल्सियस पर जम जाता है और हम इसमें नमक मिलाते हैं, तो चरण परिवर्तन तापमान नकारात्मक होगा, अर्थात बहुत कम।
यही कारण है कि समुद्र का पानी 0°C से कम तापमान वाले स्थानों पर नहीं जमता। पानी में घुलने वाला नमक ठंड के तापमान को और कम कर देता है। जिन जगहों पर बर्फ होती है, वहां बर्फ पिघलने और दुर्घटनाओं से बचने के लिए सड़कों पर नमक फेंकना भी आम बात है।
के बारे में अधिक जानने अनुबंधित विशेषताएं.
चौथा प्रयोग - हाइड्रोजन पेरोक्साइड का अपघटन of
शामिल अवधारणाएं: रासायनिक प्रतिक्रिया और उत्प्रेरक
सामग्री
- आधा कच्चा आलू और आधा पका हुआ
- कच्चे कलेजे का एक टुकड़ा और दूसरा पका हुआ टुकड़ा
- हाइड्रोजन पेरोक्साइड
- २ व्यंजन
कैसे बनाना है
- प्रत्येक व्यंजन में भोजन, आलू एक साथ और कलेजी एक साथ डालें।
- चार सामग्रियों में से प्रत्येक में हाइड्रोजन पेरोक्साइड की 3 बूंदें मिलाएं।
- देखें कि क्या होता है और परिणामों की तुलना करें।
परिणाम
हाइड्रोजन पेरोक्साइड, एक हाइड्रोजन पेरोक्साइड समाधान, जब कच्चे खाद्य पदार्थों के संपर्क में आता है, तो लगभग तुरंत ही बुदबुदाहट शुरू हो जाती है।
प्रतिक्रिया को अधिक ध्यान देने योग्य बनाने के लिए हाइड्रोजन पेरोक्साइड के साथ एक कंटेनर में भोजन का एक टुकड़ा जोड़कर भी यह प्रयोग किया जा सकता है।
व्याख्या
कच्चे खाद्य पदार्थों के संपर्क में आने पर हाइड्रोजन पेरोक्साइड द्वारा प्रस्तुत किया गया पुतला किसकी विशेषता है? एक रासायनिक प्रतिक्रिया की घटना, जो हाइड्रोजन पेरोक्साइड का अपघटन और गैस की रिहाई है ऑक्सीजन।
हाइड्रोजन पेरोक्साइड का अपघटन कैटलस एंजाइम की क्रिया के माध्यम से होता है, जो जानवरों और पौधों की कोशिकाओं में मौजूद पेरोक्सीसोम ऑर्गेनेल में पाया जाता है।
यह ध्यान रखना महत्वपूर्ण है कि हाइड्रोजन पेरोक्साइड का अपघटन सूर्य के प्रकाश की उपस्थिति में अनायास होता है, लेकिन बहुत धीमी प्रतिक्रिया में। हालांकि, उत्प्रेरक के रूप में कार्य करता है, रासायनिक प्रतिक्रिया की गति को बढ़ाता है।
हाइड्रोजन पेरोक्साइड कोशिकाओं के लिए एक विषैला पदार्थ हो सकता है। इसलिए, कैटेलेज यौगिक को तोड़ता है और पानी और ऑक्सीजन का उत्पादन करता है, दो पदार्थ जो शरीर को नुकसान नहीं पहुंचाते हैं।
जब भोजन पकाया जाता है, तो उसके घटकों में परिवर्तन होता है। खाना पकाने के कारण होने वाले संशोधन भी प्रोटीन को विकृत करके उत्प्रेरित करने की क्रिया से समझौता करते हैं।
भोजन के साथ हम वही क्रिया देखते हैं जो घाव पर हाइड्रोजन पेरोक्साइड डालने पर होती है। कैटालेज कार्य करता है और बुलबुले का निर्माण होता है, जिसमें ऑक्सीजन की रिहाई होती है।
के बारे में अधिक जानने रसायनिक प्रतिक्रिया.
ग्रंथ सूची संदर्भ
सेंट्स, डब्ल्यू। एल पी.; एमओएल, जी. एस (कोर्ड्स।) नागरिक रसायन। 1. ईडी। साओ पाउलो: नई पीढ़ी, 2011। वी 1, 2, 3.
ब्राज़ीलियाई केमिकल सोसाइटी (संगठन) २०१०। आपके पास रसायन विज्ञान: K-12 कक्षा के लिए कम लागत वाले प्रयोग। 1. ईडी। साओ पाउलो।