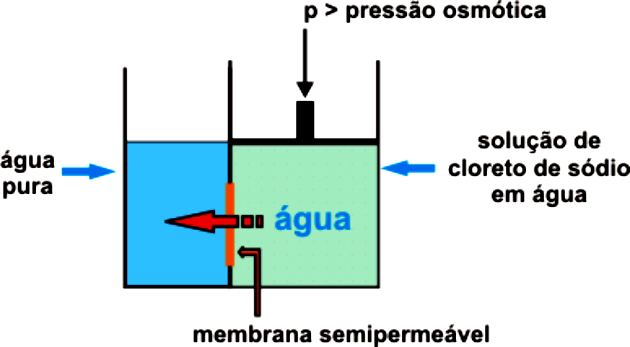
परासरण दाब यह एक संपार्श्विक गुण है जो उस दबाव से मेल खाता है जिसे परासरण को अनायास होने से रोकने के लिए एक प्रणाली पर डाला जाना चाहिए।
ऑस्मोसिस एक अर्धपारगम्य झिल्ली के माध्यम से एक कम केंद्रित (हाइपोटोनिक) से एक अधिक केंद्रित (हाइपरटोनिक) माध्यम से संतुलन तक पहुंचने तक पानी का मार्ग है।
ऑस्मोसिस को स्वाभाविक रूप से शुरू होने और होने से रोकने के लिए, अधिक केंद्रित समाधान पर बाहरी दबाव लागू करना आवश्यक है, जिससे विलायक को अधिक केंद्रित माध्यम में जाने से रोका जा सके। वह आसमाटिक दबाव है।
समाधान जितना अधिक केंद्रित होगा, आसमाटिक दबाव उतना ही अधिक होना चाहिए। इसलिए, आसमाटिक दबाव विलेय सांद्रता के समानुपाती होता है।
आसमाटिक दबाव की गणना कैसे करें?
प्रत्येक समाधान का एक अलग आसमाटिक दबाव मान होता है। आसमाटिक दबाव की गणना निम्न सूत्र से की जा सकती है:
= एम। ए। टी मैं
जहां, हमारे पास निम्नलिखित चर हैं:
π = आसमाटिक दबाव;
एम = मोल/एल में एकाग्रता;
आर = सार्वभौमिक गैस स्थिरांक, जिसका मान 0.082 एटीएम से मेल खाता है। एल मोल
टी = निरपेक्ष पैमाने पर तापमान (केल्विन);
i = वैन्ट हॉफ कारक, जिसमें आयनिक विलयनों में अंतिम और प्रारंभिक कणों की कुल संख्या के बीच संबंध शामिल है।
व्यायाम हल
1. (पक्कैम्प-एसपी) कभी-कभी, 0.30 एम ग्लूकोज समाधान का उपयोग अंतःशिरा इंजेक्शन में किया जाता है, क्योंकि इसमें रक्त के आसमाटिक दबाव होता है। 37°C पर उक्त विलयन का आसमाटिक दाब, वायुमंडल में क्या है?
ए) 1.00।
बी) 1.50।
ग) 1.76।
घ) 7.63।
ई) 9.83।
प्रश्न द्वारा प्रदान किए गए आंकड़ों को ध्यान में रखते हुए, हमारे पास है:
एम = ०.३० मोल/एल;
आर = 0.082 एटीएम। एल मोल-1. के-1
टी = 37° + 273 = 310 के
आसमाटिक दबाव की गणना के लिए अब आपको इन मानों को सूत्र पर लागू करना होगा:
= एम। ए। टी मैं
π = 0,30. 0,082. 310
= 7.63 एटीएम (विकल्प)
समाधानों का वर्गीकरण
आसमाटिक दबाव के अनुसार समाधानों को तीन प्रकारों में वर्गीकृत किया जा सकता है:
- हाइपरटोनिक समाधान: उच्च आसमाटिक दबाव और विलेय सांद्रता है।
- आइसोटोनिक समाधान: जब विलयनों का परासरण दाब समान हो।
- हाइपोटोनिक समाधान: कम आसमाटिक दबाव और विलेय सांद्रता है।

जीवित प्राणियों के लिए आसमाटिक दबाव का महत्व
खारा आसमाटिक दबाव के सिद्धांतों के आधार पर तैयार किया गया पदार्थ है। इसे शरीर में पाए जाने वाले आसमाटिक दबाव के बराबर लागू किया जाना चाहिए, यह रोकता है लाल कोशिकाओं हेमोलिसिस से पीड़ित न हों या सिकुड़े हुए न हों।
रक्त का आसमाटिक दबाव लगभग 7.8 एटीएम है। इसलिए, जीव के सही कामकाज के लिए, लाल रक्त कोशिकाओं में समान आसमाटिक दबाव होना चाहिए, जिससे कोशिकाओं के अंदर और बाहर पानी का सामान्य प्रवाह सुनिश्चित हो सके।
निर्जलीकरण के मामलों में, उदाहरण के लिए, खारा समाधान के उपयोग का संकेत दिया जाता है, जो रक्त कोशिकाओं और शरीर के अन्य तरल पदार्थों के संबंध में आइसोटोनिक होना चाहिए।
खारा समाधान शरीर के अंदर आसमाटिक संतुलन को वापस करने का कार्य करता है। ऐसा इसलिए है क्योंकि निर्जलीकरण के दौरान, रक्त कोशिकाओं के अंदर की तुलना में अधिक केंद्रित हो जाता है, जिससे वे मुरझा जाते हैं।
ऑस्मोसिस और रिवर्स ऑस्मोसिस
जैसा कि हमने देखा है, असमस यह हाइपोटोनिक से हाइपरटोनिक वातावरण में पानी को अर्ध-पारगम्य झिल्ली के माध्यम से पारित करने की प्रक्रिया है, जब तक कि सांद्रता के बीच संतुलन नहीं हो जाता है।
इस बीच, विपरीत परासरण यह एक झिल्ली के माध्यम से पदार्थों को अलग करने की एक प्रक्रिया है जो विलेय को बरकरार रखती है। विलायक अधिक सांद्र माध्यम से कम सांद्रित माध्यम में प्रवाहित होता है और एक झिल्ली द्वारा विलेय से पृथक होता है जो इसके पारित होने की अनुमति देता है।
यह केवल लगाए गए दबाव के कारण होता है, अर्ध-पारगम्य झिल्ली को केवल पानी के पारित होने की अनुमति देता है, विलेय को बनाए रखता है। यह दबाव प्राकृतिक आसमाटिक दबाव से अधिक होना चाहिए।
उदाहरण के लिए, यदि लागू किया गया आसमाटिक दबाव आवश्यकता से अधिक है, तो रिवर्स ऑस्मोसिस होगा। इस प्रकार, प्रवाह उच्चतम सांद्रता वाले माध्यम से सबसे कम सांद्रता वाले माध्यम से गुजरेगा।