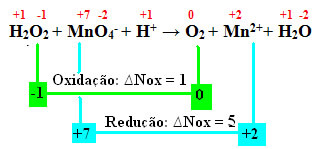
रेडॉक्स प्रतिक्रियाओं में परमाणुओं, आयनों या अणुओं के बीच इलेक्ट्रॉनों का स्थानांतरण शामिल होता है।
ऑक्सीकरण-कमी प्रतिक्रिया में, ऑक्सीकरण संख्या (nox) में परिवर्तन होते हैं। ऑक्सीकरण में ऑक्सीकरण और कमी प्रक्रियाएं होती हैं:
- ऑक्सीकरण: का परिणाम इलेक्ट्रॉन हानि और बढ़ी हुई नक्स।
- कमी: का परिणाम इलेक्ट्रॉन लाभ और घट गया नॉक्स।
जैसे ही एक तत्व इलेक्ट्रॉनों को छोड़ता है, दूसरा उन्हें प्राप्त करेगा। इस प्रकार, प्राप्त इलेक्ट्रॉनों की कुल संख्या खोए हुए इलेक्ट्रॉनों की कुल संख्या के बराबर है।
दहन, क्षरण और प्रकाश संश्लेषण के लिए रेडॉक्स प्रतिक्रियाओं के उदाहरण।
उदाहरण
इलेक्ट्रॉनों को प्राप्त करने या दान करने वाले तत्व के आधार पर, हमारे पास निम्नलिखित नाम हैं:
- अपचायक कारक: जो ऑक्सीकरण से गुजरता है वह कमी का कारण बनता है और इसकी nox संख्या बढ़ाता है। यह वही है जो इलेक्ट्रॉनों को खो देता है।
- ऑक्सीकरण एजेंट: जो अपचयन से गुजरता है वह ऑक्सीकरण का कारण बनता है और इसकी नॉक्स संख्या में कमी आती है। यह वही है जो इलेक्ट्रॉनों को प्राप्त करता है।
हे ऑक्सीकरण संख्या एक तत्व के विद्युत आवेश को उस समय दर्शाता है जब वह भाग लेता है a रासायनिक बंध.
यह स्थिति से संबंधित है वैद्युतीयऋणात्मकता, जो कुछ तत्वों की इलेक्ट्रॉनों को प्राप्त करने की प्रवृत्ति है।
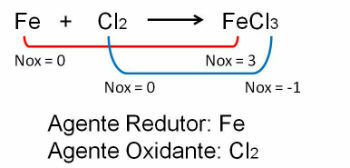
1. पहला उदाहरण देखें, ध्यान दें कि आयरन और क्लोरीन के बीच प्रतिक्रिया में ऑक्सीकरण संख्या में परिवर्तन होता है। हे क्लोरीन अधिक विद्युत ऋणात्मक होने के कारण, यह इलेक्ट्रॉनों को प्राप्त करता है:
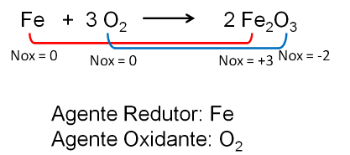
2. आयरन और ऑक्सीजन के बीच प्रतिक्रिया। ऑक्सीजन अधिक विद्युत ऋणात्मक है और अंत में इलेक्ट्रॉनों को प्राप्त करती है और उनकी ऑक्सीकरण संख्या को कम करती है।
और जानें, ये भी पढ़ें:
- ऑक्सीकरण
- दहन
- रसायनिक प्रतिक्रिया
- इलेक्ट्रॉनों
व्यायाम हल
1. (पीयूसी-आरएस) ऑक्सीकरण समीकरण के संबंध में - असंतुलित कमी Fe0 + CuSO4 → फे2(केवल4)3 + Cu0, यह कहा जा सकता है कि:
a) क्यूप्रिक सल्फेट में कॉपर की ऑक्सीकरण संख्या +1 होती है।
b) लौह परमाणु 2 इलेक्ट्रॉनों को खो देता है।
c) कॉपर का ऑक्सीकरण होता है।
d) लोहा एक ऑक्सीकरण एजेंट है।
ई) लोहे का ऑक्सीकरण होता है।
संकल्प:
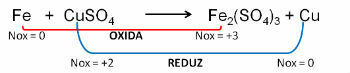
जवाब दे दो:
ई) लोहे का ऑक्सीकरण होता है।
अभ्यास
1. (UFAC-AC) निम्नलिखित रासायनिक समीकरण में: Zn + 2 HCℓ → ZnCℓ2 + एच2
a) तत्व Zn ऑक्सीकरण करता है और ऑक्सीकरण एजेंट के रूप में प्रतिक्रिया करता है।
b) Zn तत्व एक अपचायक के रूप में ऑक्सीकरण और प्रतिक्रिया करता है।
c) Zn तत्व अपचायक के रूप में अपचयित और अभिक्रिया करता है।
डी) एचसीℓ एक कम करने वाला एजेंट है।
ई) समीकरण को प्रतिवर्ती के रूप में वर्गीकृत किया गया है।
b) Zn तत्व एक अपचायक के रूप में ऑक्सीकरण और प्रतिक्रिया करता है।
2. (ITA-SP) आयनिक अभिक्रिया में Ni(s) + Cu2+(एक्यू) → नि2+(एक्यू) + घन (एस)
a) निकेल ऑक्सीकारक है क्योंकि यह ऑक्सीकृत होता है।
बी) निकल रेड्यूसर है क्योंकि यह ऑक्सीकृत है।
c) क्यूप्रिक आयन ऑक्सीकारक है क्योंकि यह ऑक्सीकृत होता है।
d) क्यूप्रिक आयन रिड्यूसर है क्योंकि यह कम हो जाता है।
ई) यह रेडॉक्स प्रतिक्रिया नहीं है, इसलिए कोई ऑक्सीडेंट या रेड्यूसर नहीं है।
बी) निकल रेड्यूसर है क्योंकि यह ऑक्सीकृत है।
3. (UFRGS) घरेलू ब्लीच में सक्रिय एजेंट हाइपोक्लोराइट आयन, ClO- है। विरंजन प्रक्रियाओं में, यह आयन कम हो जाता है; इस का मतलब है कि:
a) हाइपोक्लोराइट की क्रिया से गुजरने वाला पदार्थ इलेक्ट्रॉन प्राप्त करता है।
b) इसकी संरचना में इलेक्ट्रॉनों की संख्या में कमी होती है।
c) ClO- एक अपचायक है।
d) ClO- को मौलिक क्लोरीन या क्लोराइड आयन में बदल दिया जाता है।
ई) कोई इलेक्ट्रॉन हस्तांतरण नहीं होता है।
d) ClO- को मौलिक क्लोरीन या क्लोराइड आयन में बदल दिया जाता है।