एसपी-टाइप कार्बन का संकरण2 यह तब होता है जब इसमें एक डबल बॉन्ड और दो सिंगल बॉन्ड या एक पाई बॉन्ड (π) और तीन सिग्मा बॉन्ड (σ) होते हैं। वास्तव में, सपा संकरण2 यह उन परमाणुओं के बीच लाया जाता है जो दोहरा बंधन स्थापित करते हैं।
ऐसे अणु का एक उदाहरण फॉर्मलाडेहाइड (CH .) है2ओ)। इसकी संरचना नीचे नोट करें:
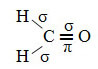
जैसा कि पाठ में देखा गया है "सपा प्रकार संकरण3”, कार्बन संकरण तब होता है जब सबलेवल 2s से एक इलेक्ट्रॉन ऊर्जा प्राप्त करता है और उसे "परिवहन" किया जाता है 2p सबलेवल और, इस प्रकार, परमाणु ऑर्बिटल्स के "मिक्स" से 4 हाइब्रिडाइज्ड ऑर्बिटल्स की उत्पत्ति होती है शुद्ध।
फॉर्मल्डेहाइड के मामले में, हम जानते हैं कि एक पीआई बंधन होगा, इसलिए इन संकरित कक्षाओं में से एक इस बंधन के लिए आरक्षित है, जबकि अन्य तीन सिग्मा बंधन लेते हैं:
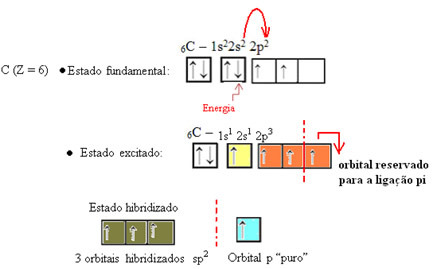
हाइड्रोजन परमाणु जो कार्बन के साथ एकल बंधन बनाते हैं, इसे अपने कक्षीय के साथ बनाते हैं:
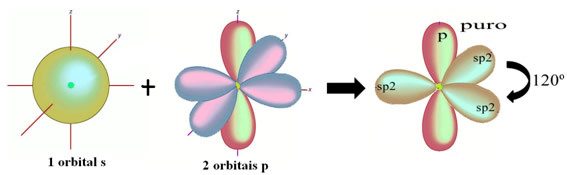
शेष "शुद्ध" पी कक्षीय ऑक्सीजन परमाणु को डबल-बॉन्ड करता है और फॉर्मल्डेहाइड अणु में निम्नलिखित संरचना होती है:
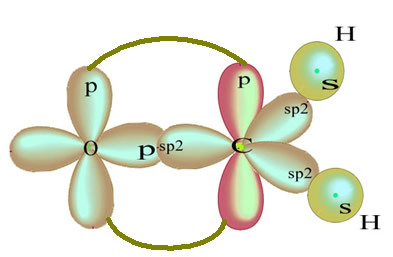
इस फॉर्मलाडेहाइड संरचना में मौजूद बांडों के प्रकार के लिए, हमारे पास है:

सम्बन्ध: 1 = 2 = σएस-एसपी2
3 = σपी-एसपी2
4 =πपी-पी
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp2.htm

