रासायनिक तत्वों को व्यवस्थित करने के तरीकों में से एक परिवारों के माध्यम से होता है, जो आवर्त सारणी के ऊर्ध्वाधर अनुक्रमों के अनुरूप होता है।
पर १८ कॉलम तालिका में तत्वों को रासायनिक गुणों में समानता के अनुसार समूहित किया जाता है।
रासायनिक तत्वों को परिवारों में व्यवस्थित करना विभिन्न सूचनाओं को सरल तरीके से व्यवस्थित करने और उन्हें प्रस्तुत करने का एक व्यावहारिक तरीका था।
एक रासायनिक तत्व के स्थान को सुविधाजनक बनाने के लिए, परिवारों को 1 से 18 तक की संख्या में नामित किया गया था जैसा कि नीचे दिखाया गया है:
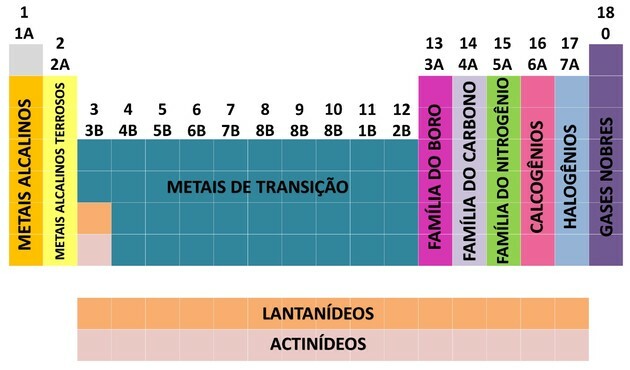
कई वैज्ञानिकों के योगदान और डेटा को व्यवस्थित करने के विभिन्न प्रयासों के माध्यम से, आवर्त सारणी विकसित हुई, जिससे तत्वों को व्यवस्थित करने का क्रम स्थापित हुआ।
परिवारों का नामकरण
- तालिका में परिवारों को ए (प्रतिनिधि) और बी (संक्रमण) में विभाजित किया गया था, जिन्हें अक्षरों और संख्याओं द्वारा पहचाना जा रहा था।
- आप प्रतिनिधि तत्व परिवार 0, 1A, 2A, 3A, 4A, 5A, 6A और 7A के अनुरूप हैं।
- आप संक्रमण तत्व परिवार 1B, 2B, 3B, 4B, 5B, 6B, 7B और 8B मेल खाते हैं।
- इंटरनेशनल यूनियन ऑफ प्योर एंड एप्लाइड कैमिस्ट्री (आईयूपीएसी) के निर्धारण से परिवारों की पहचान की गई 1 से 18. तक के समूह.
आवर्त सारणी और इलेक्ट्रॉनिक वितरण
एक ही परिवार के तत्वों के बीच समानताएं इसलिए होती हैं क्योंकि एक निश्चित समूह के सदस्यों के लिए जमीनी अवस्था में परमाणु के वैलेंस इलेक्ट्रॉनों की संख्या समान होती है।
उदाहरण के लिए:
| समूह 1 | इलेक्ट्रॉनिक वितरण |
|---|---|
| 3पढ़ना | 2-1 |
| 11पर | 2-8-1 |
| 19क | 2-8-8-1 |
| 37आरबी | 2-8-18-8-1 |
| 55सी | 2-8-18-18-8-1 |
| 87फादर | 2-8-18-32-18-8-1 |
समूह 1 परमाणुओं में उनके इलेक्ट्रॉनों को एक से अधिक ऊर्जा स्तरों पर वितरित किया जाता है, लेकिन सभी में एक वैलेंस इलेक्ट्रॉन होता है।
इसके साथ, हम देखते हैं कि बनाना इलेक्ट्रॉनिक वितरण जमीनी अवस्था में परमाणु की, हम आवर्त सारणी पर इसकी स्थिति पाते हैं।
प्रतिनिधि तत्व
प्रतिनिधि तत्व संक्रमण तत्वों की तुलना में अपेक्षाकृत कम जटिल रासायनिक व्यवहार प्रदर्शित करते हैं और हमारे चारों ओर अधिकांश पदार्थ बनाते हैं।
कुछ प्रतिनिधि तत्व परिवारों को विशेष नाम दिए गए हैं, जैसा कि नीचे दिखाया गया है:
समूह |
परिवार | विशिष्ट नाम | नाम मूल | तत्वों | इलेक्ट्रोनिक विन्यास |
|---|---|---|---|---|---|
| 1 | 1 क | क्षारीय धातु | लैटिन से क्षार, जिसका अर्थ है "पौधों का धूसर"। | ली, ना, के, आरबी, सीएस और फ्रू | अमेरिका1 |
| 2 | 2ए | क्षारीय पृथ्वी धातु | "सांसारिक" शब्द का अर्थ "पृथ्वी पर विद्यमान" है। | Be, Mg, Ca, Sr, Ba और Ra | अमेरिका2 |
| 13 | 3 ए | बोरॉन परिवार | परिवार के प्रथम तत्व का नाम। | बी, अल, गा, इन, टीएल और एनएच। | अमेरिका2एनपी1 |
| 14 | 4 ए | कार्बन परिवार | परिवार के प्रथम तत्व का नाम। | सी, सी, जीई, एसएन, पीबी और फ्लो। | अमेरिका2एनपी2 |
| 15 | 5ए | नाइट्रोजन परिवार | परिवार के प्रथम तत्व का नाम। | एन, पी, एएस, एसबी, बीआई और मैक। | अमेरिका2एनपी3 |
| 16 | 6ए | काल्कोजन | ग्रीक से खल्क्स, क्योंकि वे तांबे के अयस्कों में पाए जाने वाले तत्व हैं। | ओ, एस, से, ते, पो और लव। | अमेरिका2एनपी4 |
| 17 | 7ए | हैलोजन | ग्रीक अभिव्यक्ति का अर्थ है नमक बनाने वाला। | F, Cl, Br, I, At और Ts। | अमेरिका2एनपी5 |
| 18 | 0 | उत्कृष्ट गैस | इसे अन्य पदार्थों के साथ प्रतिक्रिया नहीं करने के लिए माना जाता था। | हे, ने, अर, क्र, ज़ी, रे और ओग। | 1s2 (वह) या हम2एनपी6 |
तालिका के माध्यम से, हम देख सकते हैं कि:
- ऊपर प्रस्तुत तत्वों को प्रतिनिधि के रूप में वर्गीकृत किया गया है क्योंकि उनके पास एस या पी सबलेवल में सबसे ऊर्जावान इलेक्ट्रॉन है।
- इलेक्ट्रॉनों को ऊर्जा स्तरों पर वितरित किया जाता है और n जमीनी अवस्था में परमाणु के सबसे बाहरी स्तर का प्रतिनिधित्व करता है।
- आईयूपीएसी की सिफारिश के अनुसार प्रतिनिधि तत्व, समूहों या परिवारों से संबंधित हैं 1,2,13,14,15,16,17 और 18।
हे हाइड्रोजन इसे अन्य तत्वों से अलग वर्गीकृत किया गया है। 1s इलेक्ट्रॉनिक कॉन्फ़िगरेशन के साथ भी1, वह एक विलक्षण व्यवहार प्रस्तुत करने के लिए समूह 1 का हिस्सा नहीं है।
संक्रमण तत्व
संक्रमण तत्व समूह 3 से 12 के अनुरूप हैं। उन्हें यह नाम इसलिए मिला है क्योंकि उनके पास समूह 1 और 2 और प्रतिनिधि गैर-धातु तत्वों के बीच मध्यवर्ती विशेषताएं हैं।
आप संक्रमण धातुओं IUPAC द्वारा परिभाषित किया गया है:
एक संक्रमण तत्व में अपूर्ण d उप-स्तर होता है या अपूर्ण d उप-स्तर के साथ धनायन बना सकता है।
जब जमीनी अवस्था परमाणु का सबसे ऊर्जावान इलेक्ट्रॉन अपूर्ण डी सबलेवल में होता है, तो इसे बाहरी संक्रमण के रूप में जाना जाता है।
लैंथेनाइड्स और एक्टिनाइड्स आंतरिक संक्रमण तत्व हैं क्योंकि उनके पास कम से कम एक अधूरा f सबलेवल है।
जब तत्वों में इलेक्ट्रॉन होते हैं जो d या f कक्षकों को भरते हैं, तो वे समान गुण प्रदर्शित करते हैं और उन्हें d या f कक्षीय तत्वों में वर्गीकृत किया जा सकता है। बाहरी या आंतरिक संक्रमण.
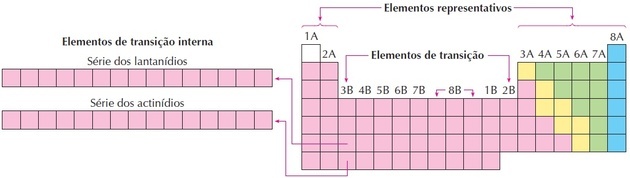
जैसा कि हम छवि में देख सकते हैं, परिवार ८बी ३ स्तंभों से मेल खाता है, वे समूह ८, ९ और १० हैं, जिन्हें इस तरह समूहीकृत किया गया था क्योंकि उनकी समान विशेषताएं हैं।
परिवारों की मुख्य विशेषताएं
नीचे दी गई तालिका आवर्त सारणी में समूहों के मुख्य गुणों को दर्शाती है:
| समूह | विशेषताएं | यौगिक पदार्थ और भी आम |
घटनाओं |
|---|---|---|---|
| 1 | परिवेश की स्थितियों में ठोस और चमकदार। बहुत प्रतिक्रियाशील, मुलायम और बिजली के अच्छे संवाहक। | लवण, हाइड्रॉक्साइड और ऑक्साइड |
हैलोजन के साथ अभिक्रिया करके लवण बनाते हैं। |
| 2 | समूह 1 की तुलना में कम प्रतिक्रियाशील और कठिन। अच्छी चालकता के साथ चांदी के ठोस। | लवण, हाइड्रॉक्साइड और ऑक्साइड |
लवण और ऑक्साइड बनाना। |
| 3 से 12 | वे कॉम्प्लेक्स बनाते हैं। वे पारे के अपवाद के साथ, जो एक तरल है, धातु के ठोस, कठोर और भंगुर होते हैं। | लवण, ऑक्साइड और परिसरों। उदा: AgNO3, TiO और [Cr(OH)3(एच2ओ)3] |
खनिजों में ऑक्साइड के रूप में। |
| 13 | परिवेशी परिस्थितियों में ठोस, चांदी, बोरॉन को छोड़कर। | आक्साइड उदाहरण: बी2हे3 |
खनिजों में ऑक्साइड के रूप में। |
| 14 | परिवेश की स्थिति में ठोस। | C और Si के परमाणु स्वयं को जंजीरों में व्यवस्थित कर सकते हैं और विभिन्न प्रकार के पदार्थ उत्पन्न कर सकते हैं। | जीवित जीवों में और सिलिकेट या ऑक्साइड के रूप में। |
| 15 | ठोस, नाइट्रोजन को छोड़कर, जो परिवेशी परिस्थितियों में गैसीय है। | ऑक्साइड और एसिड उदाहरण: नहीं2 और वह3धूल4 |
वायुमंडल, जीवित जीव और खनिज। |
| 16 | ठोस, ऑक्सीजन को छोड़कर, जो परिवेशी परिस्थितियों में गैसीय है। | सल्फाइड और ऑक्साइड उदाहरण: ZnS और SiO2 |
वायुमंडल, जीवित जीव और खनिज। |
| 17 | वे द्विपरमाणुक अणु बनाते हैं और बहुत प्रतिक्रियाशील होते हैं। ये बिजली और गर्मी के कुचालक होते हैं। वे जीवित प्राणियों और पर्यावरण के प्रति आक्रामक हैं। | अम्ल और लवण। उदाहरण: एचसीएल और केबीआर |
पदार्थों में मौजूद हैं कार्बनिक और खनिज। |
| 18 | वे बहुत स्थिर होते हैं और गैसों के रूप में पाए जाते हैं। | वे मुश्किल से यौगिक पदार्थ बनाते हैं। | वायुमंडल में गैसें। |
रासायनिक और भौतिक गुण एक परिवार को दूसरे परिवार से अलग करते हैं। जैसा कि हमने देखा, रासायनिक गुण किससे संबंधित हैं? इलेक्ट्रॉनों वैलेंस का, और उनके माध्यम से, एक परमाणु दूसरे के साथ बातचीत करता है, रासायनिक व्यवहार के लिए जिम्मेदार होता है और रासायनिक बन्ध गठित।
एक ही समूह के तत्वों के भौतिक गुण परमाणु क्रमांक और द्रव्यमान के अनुसार भिन्न हो सकते हैं।
अभ्यास
अब जब आप आवर्त सारणी परिवारों के बारे में कुछ और जानते हैं, तो अपने ज्ञान का परीक्षण करें और देखें कि आपने क्या सीखा है।
1) आवर्त सारणी से निम्नलिखित उद्धरण पर विचार करें।
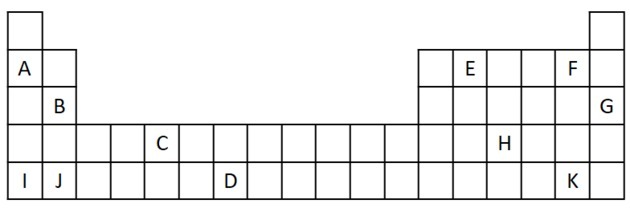
क) ऐसे दो तत्वों के नाम लिखिए जिनमें दो संयोजकता इलेक्ट्रॉन हों।
b) एक ऐसे तत्व को इंगित करें जो पानी के साथ हिंसक रूप से प्रतिक्रिया करता है, जिससे धातु हाइड्रॉक्साइड बनता है।
सी) एक गैर प्रतिक्रियाशील तत्व इंगित करें।
d) दो तत्वों को इंगित करें जो क्षार धातुओं के साथ मिलकर लवण बनाते हैं।
जवाब दे दो:
ए) बी और जे
दो वैलेंस इलेक्ट्रॉन समूह 2 के अनुरूप होते हैं, जिसमें एक एनएस इलेक्ट्रॉन विन्यास होता है2 और अभ्यास में B और J द्वारा निरूपित किए जाते हैं।
बी) ए, बी, आई या जे।
ए और मैं परिवार 1 के तत्वों का प्रतिनिधित्व करते हैं; B और J परिवार 2 से हैं। जैसा कि हमने गुण तालिका में देखा, समूह 1 और 2 तत्व बहुत प्रतिक्रियाशील हैं और हाइड्रॉक्साइड बना सकते हैं, जैसा कि दिए गए उदाहरणों में है: KOH और Mg (OH)2.
ग) जी
महान गैसें बहुत स्थिर होती हैं और इसलिए बहुत प्रतिक्रियाशील नहीं होती हैं। इस परिवार के तत्व के रूप में G अक्षर को तालिका में डाला गया है।
डी) एफ और के
हैलोजन क्षार धातुओं के साथ क्रिया करके लवण बनाते हैं। इसका सबसे आम उदाहरण टेबल सॉल्ट, NaCl है।
2) निम्नलिखित आंकड़ा तीन रासायनिक तत्वों को दिखाता है, बाएं से दाएं, लिथियम, सोडियम और पोटेशियम।

उस विकल्प का चयन करें जो निम्नलिखित में से प्रत्येक कथन को सही ढंग से पूरा करता है।
१.१) "हम कह सकते हैं कि लिथियम, सोडियम और पोटेशियम...
(ए)... उसी अवधि के हैं।"
(बी)... की परमाणु संख्या समान है।"
(सी)... एक ही समूह से संबंधित हैं।"
(डी)... समान द्रव्यमान संख्या है।"
१.२) "तत्व लिथियम, सोडियम और पोटेशियम ...
(ए)... में बहुत समान रासायनिक गुण हैं।"
(बी)... में बहुत अलग रासायनिक गुण हैं।"
(सी)... अधातु हैं।"
(डी)... अम्लीय समाधान बनाने के लिए पानी के साथ प्रतिक्रिया करें।"
उत्तर:
१.१) (सी) एक ही समूह से संबंधित हैं।
१.२) (ए) में बहुत समान रासायनिक गुण हैं।
हम यह जानकारी आवर्त सारणी से परामर्श करके या लिथियम, सोडियम और पोटेशियम तत्वों का इलेक्ट्रॉनिक वितरण करके प्राप्त कर सकते हैं। हम देखेंगे कि संयोजकता कोश में तीनों के पास एक इलेक्ट्रॉन होता है और क्योंकि वे एक ही समूह के भाग होते हैं, रासायनिक गुण बहुत समान होते हैं।
3) निम्नलिखित तालिका पर विचार करें, जहां कुछ रासायनिक तत्वों के परमाणु क्रमांक और इलेक्ट्रॉनिक वितरण का प्रतिनिधित्व किया जाता है।
| तत्त्व | रासायनिक प्रतीक | परमाणु क्रमांक | इलेक्ट्रॉनिक वितरण |
|---|---|---|---|
| लिथियम | पढ़ना | 3 | 2,1 |
| फीरोज़ा | होना | 4 | 2,2 |
| एक अधातु तत्त्व | एफ | 9 | 2,7 |
| नीयन | हुह | 10 | 2,8 |
| क्लोरीन | क्लोरीन | 17 | 2,8,7 |
| आर्गन | वायु | 18 | 2,8,8 |
| पोटैशियम | क | 19 | 2,8,8,1 |
| कैल्शियम | यहाँ | 20 | 2,8,8,2 |
प्रत्येक तत्व के समूह को इंगित करें।
जवाब दे दो:
लिथियम और पोटेशियम: समूह 1. (उनके संयोजकता कोश में एक इलेक्ट्रॉन होता है)।
बेरिलियम और कैल्शियम: समूह 2. (उनके संयोजकता कोश में दो इलेक्ट्रॉन होते हैं)।
फ्लोरीन और क्लोरीन: समूह 17. (उनके संयोजकता कोश में सात इलेक्ट्रॉन होते हैं)।
नियॉन और आर्गन: समूह 18। (उनके संयोजकता कोश में आठ इलेक्ट्रॉन होते हैं)।
एक टिप्पणी संकल्प के साथ प्रवेश परीक्षा के प्रश्नों की जाँच करें आवर्त सारणी पर व्यायाम और इस विषय पर अप्रकाशित प्रश्न आवर्त सारणी के आयोजन पर अभ्यास.


