कार्बनिक यौगिक आणविक होते हैं, अर्थात उनके परमाणु एक दूसरे के साथ सहसंयोजक बंधन रखते हैं। जब हम कार्बन के बीच के बंधनों का विश्लेषण करते हैं, जो सिंगल, डबल या ट्रिपल हो सकते हैं, तो हम देखते हैं कि वे हैं गैर-ध्रुवीय बंधन, क्योंकि परमाणुओं के बीच वैद्युतीयऋणात्मकता में कोई अंतर नहीं है, क्योंकि वे एक ही हैं तत्व।
इसके अलावा, चूंकि हाइड्रोजन और कार्बन में बहुत कम इलेक्ट्रोनगेटिविटी अंतर होता है, इसलिए उनके बीच के बंधन भी गैर-ध्रुवीय होते हैं।
गैर-ध्रुवीय कनेक्शन:
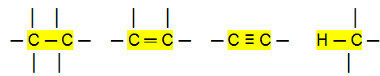
इससे हम यह निष्कर्ष निकाल सकते हैं कि हाइड्रोकार्बन (कार्बनिक यौगिक जिनमें केवल कार्बन और हाइड्रोजन परमाणु होते हैं) गैर-ध्रुवीय अणु हैं. इन यौगिकों में, अंतःक्रियात्मक अंतःक्रिया प्रेरित द्विध्रुवीय प्रकार की होती है, जो कि मौजूद सबसे कमजोर है।
चूंकि वे कमजोर हैं, इसलिए इन इंटरैक्शन को तोड़ना आसान है। जिसके परिणामस्वरूप, हाइड्रोकार्बन का क्वथनांक और गलनांक अन्य कार्यों की तुलना में कम होता है।

हाइड्रोकार्बन की तुलना, क्वथनांक बढ़ जाएगा क्योंकि दाढ़ द्रव्यमान भी बढ़ता है।
उदाहरण के लिए, ईथेन और ब्यूटेन दोनों अल्केन हैं। प्रयोगात्मक रूप से निर्धारित प्रत्येक के क्वथनांक देखें:
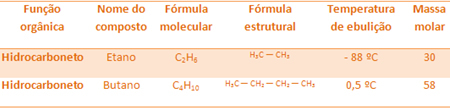
ध्यान दें कि ब्यूटेन का क्वथनांक ईथेन की तुलना में बहुत अधिक होता है, क्योंकि इसका दाढ़ द्रव्यमान भी अधिक होता है।
अब जब हम उन हाइड्रोकार्बन की तुलना करते हैं जिनका दाढ़ द्रव्यमान समान होता है (वे समावयवी होते हैं), लेकिन उनमें विभिन्न प्रकार की कार्बन शृंखलाएँ होती हैं, तो हमें पता चलता है कि शाखाओं की संख्या जितनी अधिक होगी, उबलते तापमान उतना ही कम होगा, क्योंकि अणु की संरचना अधिक सघन हो जाती है, अर्थात इसकी सतह कम हो जाती है।
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
नीचे दिए गए सभी अल्केन्स का आणविक सूत्र समान है, C5एच12, लेकिन उनके उबलते तापमान अलग हैं:
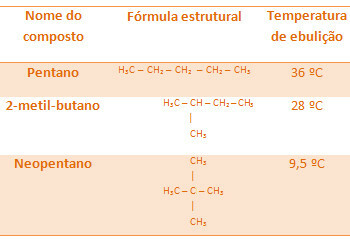
ध्यान दें कि नियोपेंटेन का क्वथनांक सबसे कम है क्योंकि इसकी शाखाएँ अधिक हैं।
हम विचार कर सकते हैं कि अन्य कार्बनिक कार्य हाइड्रोकार्बन से प्राप्त होते हैं, एक या एक से अधिक हाइड्रोजन के परमाणुओं या अन्य तत्वों के परमाणुओं के समूहों द्वारा प्रतिस्थापन के माध्यम से। आम तौर पर, अन्य कार्बनिक कार्यों में ऑक्सीजन या नाइट्रोजन होता है, जो कार्बन की तुलना में अधिक विद्युतीय तत्व होते हैं। वे कार्बन के साथ साझा किए गए इलेक्ट्रॉनों की जोड़ी को अधिक मजबूती से आकर्षित करते हैं और इसलिए, अणु को ध्रुवीय बनाते हैं:
ध्रुवीय कनेक्शन:
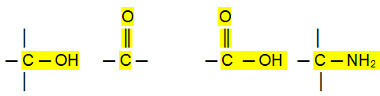
एल्डिहाइड, कीटोन और कार्बनिक हैलाइड के क्वथनांक. से अधिक होते हैं हाइड्रोकार्बन, क्योंकि उनकी अंतःक्रियात्मक बातचीत स्थायी द्विध्रुवीय है, जो कि से अधिक मजबूत है प्रेरित द्विध्रुवीय।
दूसरी ओर, अल्कोहल, कार्बोक्जिलिक एसिड और एमाइन का क्वथनांक भी अधिक होता है, क्योंकि वे हाइड्रोजन बांड को पूरा करते हैं, जो सबसे तीव्र प्रकार की अंतःक्रियात्मक बातचीत है।
इन सभी कार्यों के यौगिकों में, वही लागू होता है जैसा हमने हाइड्रोकार्बन के लिए देखा था:

जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? देखो:
FOGAÇA, जेनिफर रोचा वर्गास। "कार्बनिक यौगिकों की ध्रुवीयता और उबलते तापमान"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/quimica/polaridade-temperatura-ebulicao-dos-compostos-organicos.htm. 28 जून, 2021 को एक्सेस किया गया।



