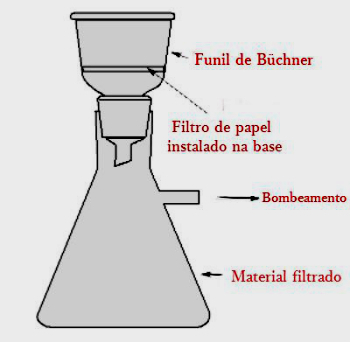
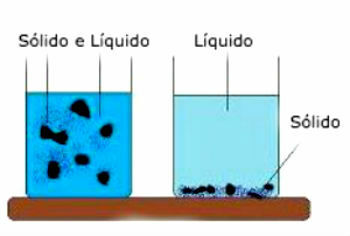
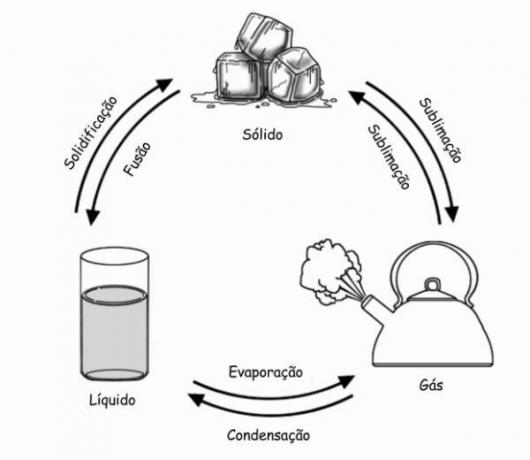
1960 में लिनुस पॉलिंग द्वारा बनाए गए ऑर्बिटल्स के मॉडल के अनुसार, सहसंयोजक बंधन जो बनाता है अणु में शामिल तत्वों के अधूरे कक्षकों के संलयन या अंतर्प्रवेश द्वारा होता है संपर्क। इस प्रकार, यह निष्कर्ष निकाला जाता है कि यदि तत्व में अपूर्ण कक्षीय (केवल एक इलेक्ट्रॉन के साथ) है, तो यह केवल सहसंयोजक बंधन बना सकता है। यदि इसके दो अपूर्ण कक्षक हैं, तो यह अधिकतम दो संयोजन कर सकता है, इत्यादि।
हालांकि, तत्व कार्बन परमाणु के परमाणु कक्षकों को देखें, जिनकी परमाणु संख्या 6 (Z = 6) के बराबर है:
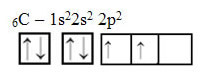
ध्यान दें कि इसकी दो अपूर्ण कक्षाएँ हैं, इसलिए इसे अधिकतम दो बाइंडिंग ही करनी चाहिए। हालाँकि, उसके साथ ऐसा नहीं होता है। जैसा कि बहुत से लोग जानते हैं, कार्बन चार बंधन बनाता है (यह टेट्रावैलेंट है), इसलिए ऑर्बिटल्स का यह मॉडल कार्बन के मामले की व्याख्या नहीं करता है।
इस गतिरोध को समाप्त करने के लिए, एक नया सिद्धांत बनाया गया जिसने इस मुद्दे को बेहतर ढंग से समझाया: संकरण सिद्धांत।

इसका अर्थ है कि संकरण शुद्ध कक्षकों का "मिश्रण" है।
कार्बन के लिए तीन प्रकार के संकरण हैं, जो हैं: sp3, स्पा2 और सपा
यह समझने के लिए कि संकरण कैसे होता है, आइए पहले प्रकार के कार्बन संकरण को देखें, sp प्रकार।3:
इस प्रकार का संकरण मीथेन अणु (CH .) में होता है4). ध्यान दें कि कार्बन, जो केंद्रीय तत्व है, और चार हाइड्रोजन के बीच चार समान सहसंयोजक बंधन हैं। तो, देखें कि अधूरा हाइड्रोजन कक्षीय क्या है:
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
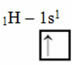
चूंकि प्रत्येक हाइड्रोजन में एक अपूर्ण एस-प्रकार का कक्षक होता है, इसलिए एक और इलेक्ट्रॉन प्राप्त करना आवश्यक होता है, अर्थात प्रत्येक कार्बन के साथ केवल एक सहसंयोजक बंधन बनाता है। इसलिए कार्बन के चार अधूरे ऑर्बिटल्स होने चाहिए। यह कैसे होता है? संकरण के माध्यम से।
जब 2s कक्षक से एक इलेक्ट्रॉन ऊर्जा को अवशोषित करता है, तो वह खाली 2p कक्षक में चला जाता है। इस प्रकार, हम कहते हैं कि 2s से 2p सबलेवल तक इलेक्ट्रॉन की यह छलांग इलेक्ट्रॉन का "प्रमोशन" है। इस तरह, कार्बन अपनी उत्तेजित या सक्रिय अवस्था में रहता है, सहसंयोजक बंधों को पूरा करने के लिए चार संकरित कक्षाएँ उपलब्ध होती हैं:
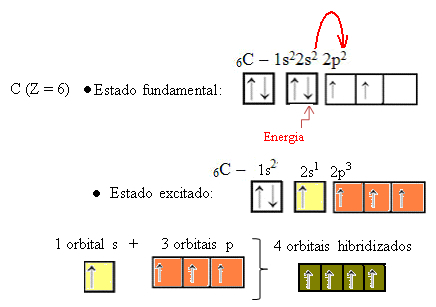
ध्यान दें कि गठित हाइब्रिड ऑर्बिटल्स एक दूसरे के समतुल्य हैं, लेकिन मूल शुद्ध ऑर्बिटल्स से अलग हैं।
इस प्रकार, चार हाइड्रोजन परमाणुओं में से प्रत्येक के s कक्षक के बीच का बंधन इन चार संकरित कार्बन कक्षकों के साथ होता है:
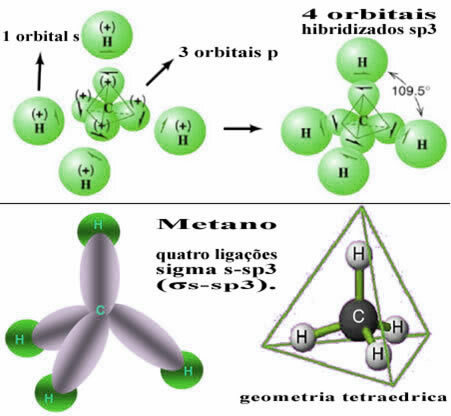
जैसा कि ऊपर देखा गया है, मीथेन अणु में एक नियमित टेट्राहेड्रोन संरचना होती है, जिसमें प्रत्येक शीर्ष पर चार इलेक्ट्रॉन बादल होते हैं और 109 ° 28 'के आसन्न कोण होते हैं। चूँकि आबंध प्रत्येक हाइड्रोजन के s कक्षक और संकरित sp कक्षक के बीच बना था3 प्रत्येक कॉल के लिए, तो हमारे पास है कि वे हैं फोर सिग्मा एस-एसपी लिंक3 (σएस-एसपी3).
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? देखो:
FOGAÇA, जेनिफर रोचा वर्गास। "Sp3 प्रकार संकरण"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp3.htm. 28 जून, 2021 को एक्सेस किया गया।