बंधन ऊर्जा शामिल है ब्रेक मेंयाप्रशिक्षण में हूं एक अणु के परमाणुओं के बीच एक या एक से अधिक बंधन। उदाहरण के लिए, हाइड्रोजन गैस अणु में शामिल परमाणुओं के बीच एक एकल बंधन (सिग्मा) होता है:

हाइड्रोजन गैस संरचनात्मक सूत्र
इस अणु की उत्पत्ति के लिए, इसके परमाणुओं के बीच एकल बंधन बनाया गया था। जब यह अणु क्लोरीन गैस (Cl .) के साथ रासायनिक अभिक्रिया में भाग लेता है2), उदाहरण के लिए, हाइड्रोक्लोरिक एसिड (HCl) के निर्माण के लिए, H. में मौजूद एकल बांड2 और क्लू में2 एचसीएल में एक एकल बंधन के परिणामी गठन के साथ तोड़ा जाना चाहिए।
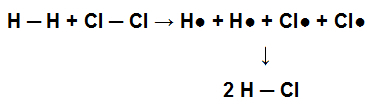
अभिकर्मक में एकल बंधनों के टूटने और उत्पाद में एकल बंधन के गठन का प्रतिनिधित्व
परमाणु अपनी प्राप्ति के लिए एक साथ बंधते हैं इलेक्ट्रॉनिक स्थिरताअर्थात्, वे उच्च ऊर्जा स्थिति से निम्न ऊर्जा स्थिति में चले जाते हैं। इस प्रकार, हम कह सकते हैं कि जब परमाणुओं के बीच बंधन बनता है, तो ऊर्जा निकलती है; इसलिए, परिणामस्वरूप, इसका टूटना ऊर्जा अवशोषण पर निर्भर करता है।
अगर हम समझते हैं कि अलग होना एक रासायनिक बंधन का (तोड़ना) तब होता है जब इसे इसकी आपूर्ति की जाती है ऊर्जा की मात्रा (xKcal)
, हमने निष्कर्ष निकाला कि यह एक प्रक्रिया है एन्दोठेर्मिक. इसके विपरीत, एक बंधन बनाने में शामिल होगा रिहाई देता है ऊर्जा की समान मात्रा (-xkcal), होने के नाते, फिर, एक प्रक्रिया एक्ज़ोथिर्मिक.पसंद रासायनिक प्रतिक्रियाओं को वर्गीकृत किया जाता है एंडोथर्मिक या एक्ज़ोथिर्मिक, हम रासायनिक प्रक्रिया की ऊर्जा (H) में परिवर्तन को निर्धारित करने के लिए अभिकारकों और उत्पादों के अणुओं की बाध्यकारी ऊर्जाओं के ज्ञान का उपयोग कर सकते हैं और फिर इसे वर्गीकृत कर सकते हैं।
उदाहरण के लिए, नीचे दिए गए समीकरण को देखें:
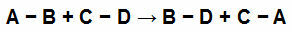
रासायनिक समीकरण में प्रतिभागियों में रासायनिक बांड Bond
प्रतिक्रिया प्रतिभागियों में से प्रत्येक में हमारे पास सरल लिंक हैं। उनके पास निम्नलिखित मूल्य हैं:
[ए-बी] = ५० किलो कैलोरी
[सीडी] = १०० किलो कैलोरी
[बी-डी] = 80 किलो कैलोरी
[ई.पू.] = 230 किलो कैलोरी
उपरोक्त मूल्यों के साथ, हम अभिकारकों के बंधनों को तोड़ने और उत्पादों के बंधन बनाने में शामिल ऊर्जा की गणना निम्नानुसार कर सकते हैं:
अभिकर्मकों में
AB बंधन को तोड़ने के लिए 50 किलो कैलोरी तथा सीडी बांड तोड़ने के लिए १०० किलो कैलोरीयानी रिएजेंट में बॉन्ड को तोड़ने के लिए 150 किलो कैलोरी का इस्तेमाल किया जाएगा।
उत्पादों में
बीडी बांड बनाने के लिए 80 किलो कैलोरी और एसी बांड बनाने के लिए 230 किलो कैलोरी, यानी बांड के गठन में उत्पाद में 310 किलो कैलोरी जारी किया जाएगा
अभिकारकों और उत्पादों में शामिल ऊर्जाओं के मूल्यों के साथ, यह जानना संभव है कि प्रतिक्रिया ने अवशोषित किया है या नहीं में जारी ऊर्जा से व्यवधान में उपयोग की गई ऊर्जा को घटाकर अधिक ऊर्जा जारी की गठन:
Δएच = अभिकर्मकों की ऊर्जा - उत्पादों की ऊर्जा
Δएच = 230 - 310
Δएच = -80 किलो कैलोरी
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
चूंकि प्रतिक्रिया में अवशोषण की तुलना में अधिक ऊर्जा रिलीज होती है, इसलिए नकारात्मक ΔH एक्ज़ोथिर्मिक है।
ध्यान दें: यदि प्रतिभागी का स्टोइकोमेट्रिक गुणांक 1 से भिन्न है, तो हमें गुणांक द्वारा कनेक्शन के ऊर्जा मान को गुणा करना चाहिए, उदाहरण के लिए:
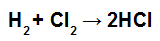
एचसीएल गठन समीकरण
चूंकि एचसीएल का गुणांक 2 है, हमें एचसीएल के बंधन के मूल्य को 2 से गुणा करना चाहिए।
अब रासायनिक अभिक्रिया में बाध्यकारी ऊर्जा पर एक अभ्यास के संकल्प का पालन करें:
उदाहरण: निम्नलिखित बाध्यकारी ऊर्जाओं को देखते हुए, किलोजूल प्रति मोल बांड (पूर्ण मान) में:
एच - एच = 436
एन एन = 945.6
एन - एच = 391
गर्मी की गणना करें (एनएच. के किलोजूल प्रति मोल में)3 (जी)) द्वारा प्रतिनिधित्व की गई प्रतिक्रिया में शामिल है:
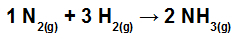
एनएच गठन प्रतिक्रिया में रासायनिक बंधन bonds3
संकल्प:
इस अभ्यास को हल करने में पहला कदम प्रत्येक अणु में मौजूद रासायनिक बंधों को प्रदर्शित करने वाले समीकरण को फिर से लिखना है:
नहीं नहीं2: हमारे पास एक ट्रिपल बॉन्ड है (क्योंकि N, नाइट्रोजन का परिवार, तीन बॉन्ड बनाना चाहिए क्योंकि इसमें वैलेंस शेल में पांच इलेक्ट्रॉन होते हैं);
H पर2: हमारे पास एक एकल बंधन है (क्योंकि एच को केवल एक बंधन बनाना चाहिए क्योंकि उसके पास वैलेंस शेल में केवल एक इलेक्ट्रॉन है);
एनएच में3: हमारे पास तीन सरल बंधन हैं (क्योंकि प्रत्येक एच को एक बंधन की जरूरत है, और एन, तीन बंधन)।
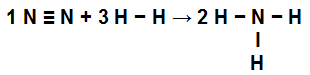
NH निर्माण में कड़ियों को प्रदर्शित करने वाला समीकरण3
चूंकि अभ्यास प्रत्येक बंधन के लिए मान प्रदान करता है, पहला कदम प्रत्येक प्रतिभागियों से संबंधित बाध्यकारी ऊर्जा का निर्धारण करना है:
- तो कैसे2
हमारे पास है १ मोल में नहीं2समीकरण में और, आपका कनेक्शन तोड़ने के लिए, हमें 945.4 KJ चाहिए, इसलिए:
1.945,4 = ९४५.४ केजे
- H के लिए2
हमारे पास है 3 मोल में एच2समीकरण में और, आपका कनेक्शन तोड़ने के लिए, हमें 436 KJ चाहिए, इसलिए:
3.346 = १०३८ केजे
- एनएच को3
हमारे पास है 2 mol NH3समीकरण में, लेकिन एन-एच बॉन्ड तीन गुना है, तो आइए उस बॉन्ड को बनाने में शामिल ऊर्जा की मात्रा को 2 से और 3 से गुणा करें:
2.3.391 = २३४६ केजे
अंत में, हम उत्पाद निर्माण में जारी ऊर्जा से अभिकारक को तोड़ने के लिए उपयोग की जाने वाली ऊर्जा को घटाकर प्रतिक्रिया में शामिल गर्मी का निर्धारण कर सकते हैं:
Δएच = अभिकारकों में ऊर्जा - उत्पादों में ऊर्जा
Δएच = (945.4 + 1038) - 2346
Δएच = 1983.4 - 2346
Δएच = - 362.6 केजे प्रति मोल NH3 (जी)
चूंकि भिन्नता ऋणात्मक थी, इसका अर्थ है कि उत्पादों में बंधों के निर्माण में जारी ऊर्जा अभिकारकों के बंधों को तोड़ने में अवशोषित ऊर्जा से अधिक थी, इसलिए, प्रतिक्रिया एक्ज़ोथिर्मिक है.
मेरे द्वारा। डिओगो लोपेज डायस

